
Бесплатный фрагмент - Старение и антиэйджинг: медико-биологические подходы к увеличению продолжительности жизни и активному долголетию
Об авторах

Андрей Степанович Брюховецкий — профессор, доктор медицинских наук, ветеран Министерства обороны РФ, полковник медицинской службы в запасе. В настоящее время является генеральным директором АО Клинический госпиталь «НейроВита». Врач-невролог высшей категории, вице-президент Международной ассоциации нейровосстановления (International Association of Neurorestoratology), член редколлегии ряда научных журналов: «Гены и клетки», Journal of Translational Neuroscience and Clinics, Journal of Neurorestoratology, Oncology Letter. С 1989 г. в рамках программ Министерства обороны РФ занимался применением двойных критических технологий в медицине. С 1996 по 2002 г. руководил лабораторией высоких технологий НИИ трансплантологии и искусственных органов им. акад. В. И. Шумакова Минздрава России. С 2003 по 2013 г. был координатором научной отраслевой программы РАМН «Новые клеточные технологии — медицине». С 2002 по 2006 г. возглавлял кафедру клеточной восстановительной медицины ГОУ ВПО «Российский государственный медицинский университет им. Н. И. Пирогова». С 2012 по 2015 г. — руководитель Центра биомедицинских технологий ФГБУ «Федеральный научно-клинический центр ФМБА России». С 2016 по 2019 г. — ведущий научный сотрудник научно-исследовательского отдела Центральной клинической больницы Российской академии наук. Автор 237 научных публикаций в рецензируемых национальных и международных специализированных научных журналах, 15 научных монографий в области регенеративной медицины, неврологии, онкологии и 15 глав в коллективных монографиях на русском и английском языках, а также автор 20 патентов РФ, 5 международных заявок PCT и патента США.

Михаил Аркадьевич Шурдов — биолог и биофизик. В 1975 г. закончил Новосибирский государственный университет, получив диплом физика со специализацией «квантовая оптика и радиофизика», принял предложение остаться стажером-исследователем в том же вузе. С 1975 по 1990 г. прошел все ступени научного работника: стажер-исследователь, инженер, младший научный сотрудник, научный сотрудник. В 1985 г. в Институте биофизики СО АН СССР (г. Красноярск) защитил диссертацию и стал кандидатом биологических наук. В настоящее время крупный предприниматель, председатель правления и главный акционер группы компаний «Чебоксарский электроаппаратный завод», председатель правления АО Клинический госпиталь «НейроВита». Автор более 30 научных публикаций и 15 патентов РФ. Меценат, финансирующий более 25 научных проектов в медицине и биологии.
Список условных сокращений и обозначений



Предисловие
Написать предисловие к научной монографии о старении, антистарении и новым подходам к активному долголетию меня попросили оба автора этой книги — профессор, доктор медицинских наук Андрей Степанович Брюховецкий, с которым мы знакомы более 30 лет, и биолог и биофизик, меценат и специалист в области молекулярной биологии, кандидат биологических наук Михаил Аркадьевич Шурдов, с которым мы знакомы тоже уже более 15 лет. Они хорошо знают мой давний научный интерес к этой проблеме и уже много лет пристально следят за проводимыми мною и сотрудниками нашего национального научного центра фундаментальными и клиническими исследованиями в этой области. Поэтому я с удовольствием отозвался на это предложение, так как мне самому было очень интересно почитать их всегда нестандартную и очень неоднозначную, но абсолютно авторскую точку зрения на столь сложную проблему, как старение, а также ознакомиться с их новаторским пониманием решения этой сложной проблемы. Оказалось, что в своих прогнозах на эту книгу я не ошибся и с удовольствием ознакомился с предложенной авторами клонально-кроветворной теорией старения человека, а также с их предложениями о создании национальной системы медико-биологической защиты населения от старения и о путях профилактики и терапии смертельных заболеваний цивилизации. Мои научные сотрудники, хорошо владеющие проблемой старения и имеющие авторитет в этой области, по-разному отреагировали на представленные в этой монографии теоретические и экспериментальные изыскания авторов, и диапазон их высказываний о книге был абсолютно полярен: от категорического отрицания и неприятия предложенной авторами концепции клональности гемопоэза постгеномного старения, обусловленного протеомным повреждением собственной гемопоэтической стволовой клетки, и формирования олигоклонального гемопоэза как системообразующего механизма старения человека до полного понимания и всестороннего одобрения предложенной авторами теории и их экспериментальных данных.
По-видимому, нецелесообразно критиковать или ругать предложенный авторами подход к проблеме старения и ее решение, так как я считаю, что данная научная, социальная и гражданская позиция авторов на подобные научно-теоретические аспекты старения имеет свое право на существование и, главное, открывает принципиально новые пути понимания и клинического применения этих новых знаний на практике. Предложенная авторами книги клонально-кроветворная теория старения явно неординарна и достаточно интересна открывающимися научными и практическими перспективами! Если обратиться к материалам ведущих мировых научных журналов, Nature и Nature Genomic, за 2022 год, то все их центральные статьи этого лета посвящены теме клонального гемопоэза как главного научного мирового тренда, которым авторы данной монографии занимаются более 20 лет. При этом представленный авторами взгляд на старость как на болезнь, изложенный в монографии, не является кардинально новым, а скорее лишь определяется новаторской точкой зрения авторов на нозологическую принадлежность этой возрастзависимой болезни путем отнесения ее к разновидностям постгеномных фатальных болезней крови и установления новых фундаментальных патогенетических фактов эпигеномных, протеомных и транскриптомных изменений, возникающих в собственных кроветворных стволовых клетках человека в процессе жизни.
Очевидно, что с увеличением продолжительности времени жизни дилемма проявлений собственной старости и борьбы с ней становится основной проблемой любого человека, живущего на этой Земле. Естественный процесс физиологического старения закономерно завершается смертью каждого индивидуума, и пока никого, кто бы смог преодолеть смерть и стать «бессмертным». Пока этот счастливый финал возможен только в сказках и современных научно-фантастических фильмах и некоторых книгах писателей-фантастов. При этом в ряду других живых существ, обитающих на нашей планете, существует множество видов растений и животных, которые вообще не стареют! В число «бессмертных» или, точнее, «не стареющих» живых существ попали такие животные, как гидра, рак-отшельник, большая синица, некоторые ящерицы и моллюски, красноногая лягушка, черепаха Gopherus agassizii, голый землекоп, ночница Брандта (летучая мышь) и др. То есть сам по себе научный факт возможности существования биологического живого существа без процесса старения, очевиден и реален, а значит, со временем и при появлении соответствующих технологий, наука сможет на практике воспроизвести этот существующий природный эксперимент и на человеке. Поэтому работать в этом научном направлении очень перспективно, нужно и должно. Те природные модели, в которых отсутствует старение в многоклеточном организме, заставляют ученых искать неизвестные нам пока механизмы регенерации и самовосстановления (саногенеза), подбирая для биологического совершенства природоподобные механизмы и инструменты.
Следует признать, что последние два десятилетия научная тематика физиологического старения человека и борьбы с этим неизбежным и фатальным явлением (антистарение, антиэйджинг, от англ. antiaging) является центральной проблемой большинства исследований современной зарубежной и отечественной науки. Старость как болезнь уже несколько десятилетий рассматривается многими зарубежными учеными как фундаментальный теоретический постулат, но авторами этих исследований это определение старости квалифицируется чисто теоретически и популистски. Под него не предлагалось никогда и никакого практического решения проблемы. Тот подход, который предприняли авторы этой книги, очень новаторский и практический, так как они предложили целую серию медико-биологических мероприятий и новых клинических и параклинических решений изучаемой проблемы.
Все исследователи процессов старения ищут «волшебную» молекулярно-биологическую «пулю», способную в одночасье сделать человека молодым, здоровым и бессмертным. Кто-то из ученых считает основным путем борьбы со старением необходимость осуществлять управление определенными молекулярными процессами биологии старения и их регуляцию, например добиться увеличения длины теломер, или удалить из стареющей клетки и (или) из межклеточного пространства патологические специфические белки, или осуществить в поврежденных клетках организма животных и человека репарацию ДНК и т. д.
Действительно, авторами показано, что существует зависимость между долголетием и репарацией поврежденной ДНК, как это было продемонстрировано на примере фермента поли (АДФ-рибоза) полимеразы-1 (PARP-1), важного игрока в клеточном ответе на вызванное стрессом повреждение ДНК. Работы, организованные и профинансированные М. А. Шурдовым и коллективом его единомышленников под руководством молекулярного биолога и генетика д. б. н. С.С. Богачева и его команды из молодых ученых из Новосибирского ФГБУН НИИ цитологии и генетики СО РАН, по реставрации поврежденной ДНК привели к созданию, патентованию и получению государственной регистрации лекарственной субстанции «Панаген» в 2008 г. В 2021 г. научные работы по «Панагену» удостоены премии президента РФ молодым ученым. Однако нестандартное применение разработанной ими субстанции «Панаген» для реставрации гемопоэтических стволовых клеток человека и млекопитающих, получивших возрастные протеомные изменения в результате процесса старения и при повреждении генома в результате химио- и лучевой терапии, дало ошеломительные результаты как на экспериментальных животных, получивших 2–3 смертельные дозы радиоактивного излучения, так и на выживании пациентов с онкологическими заболеваниями. Тем не менее тот факт, что лекарственная субстанция «Панаген» способна увеличить длину теломерных участков ДНК хромосом гемопоэтических стволовых клеток в 1,5–2 раза, для меня был откровением и полной неожиданностью. Этот молекулярный факт полностью объясняет увеличение выживаемости старых крыс по сравнению с группой контроля на 57% и дает понимание феномена улучшения качества их жизни после введения им костного мозга крыс этой же линии, предобработанных лекарственной субстанцией «Панаген» в специальных базовых условиях.
К сожалению, клинические эффекты увеличения продолжительности жизни у различных живых существ и млекопитающих путем молекулярно-биологических инженерных подходов работают только в эксперименте, но они пока не имеют клинического выхода. Кто-то из исследователей убежден, что нужно бороться исключительно с возраст-ассоциированными заболеваниями, так как чем старше люди, тем меньше у них рисков получить новые заболевания. В возрасте 110 лет люди вообще практически перестают болеть, хотя до такого возраста мало кто доживает. Инфекционные заболевания и почти все болезни цивилизации (кардиологические заболевания, сердечно-сосудистые катастрофы или онкологические болезни) не встречаются у людей после 110 лет, так как эти люди находятся в зоне пренебрежимого старения. Тогда от чего же умирают эти люди? А умирают они от банальной простуды и трахеобронхитов, завершающихся тяжелой пневмонией или другим системным воспалительным инфекционным процессом, с которым их организм легко бы справился в молодом возрасте. Главной причиной их смерти в столь почтенном возрасте, по мнению авторов этой книги, является неспособность (недостаточность) их иммунной системы и системы кроветворения к формированию системного специфического клеточно-гуморального иммунного ответа из-за дефицита и структурных патоморфологических изменений собственных ГСК и их потомков, обусловленная хронической недостаточностью собственного костного мозга.
В настоящее время в современной отечественной и зарубежной научной литературе по проблеме геронтологии (науки о старении) мелькает целый калейдоскоп из открытий и научных фактов о новейших молекулярно-биологических достижениях мировых ученых в области продления жизни, антиэйджинговых исследованиях и проблемах здорового активного долголетия. Наличие более чем 300 теорий старения говорит лишь о том, что ни одна из них пока не отвечает на вопросы исследователей и практически не работает. Они не позволяют увеличить среднюю продолжительность жизни настоящей популяции людей и достичь бессмертия человека. Однако успехи этих теоретических исследований и экспериментальных изысканий позволили увеличить продолжительность жизни различных живых существ в 10 раз и более. И это не просто так, ведь геронтология и возможность значительного увеличения продолжительности жизни человека — это самый передовой край современной науки, инновационное понимание процессов старения и физиологической возрастной дегенерации органов, тканей и клеток человека, и одна из самых актуальных проблем современности — в поиске спасения от фатальных заболеваний цивилизации, сокращающих наши дни на этой земле.
Решение проблемы долгожительства и активного здорового долголетия стало основным мировым трендом большинства социально-экономических программ мэрий городов и администраций крупных мегаполисов в высокоразвитых зарубежных странах. Системы мероприятий здорового долголетия стали основой стратегической политики по улучшению демографии в этих странах. Например, социальная программа мэрии г. Москвы «Московское долголетие» известна почти каждому жителю нашей страны и является образцовым «социально-экономическим продуктом» национального государственного подхода к улучшению качества жизни пожилых людей. Наибольшее количество людей-долгожителей сегодня живет в Японии и в Швейцарии, и это связано с целенаправленной государственной политикой этих стран в области улучшения в них демографии.
Российское государство также уделяет этим проблемам центральное значение, и одним из национальных проектов страны стал проект «Демография». На реализацию этого нацпроекта государство выделило почти 3,3 трлн руб. Этот факт свидетельствует о том, что проблема увеличения продолжительности жизни населения в нашей стране находится в главном фокусе заботы нашего государства и его правительства. Насколько эффективно она будет решена, покажет только время. Но уже сейчас очевидно, что нужны нестандартные и асимметричные подходы и инновационные стратегии в решении демографических проблем государства. И представленная книга демонстрирует, что эти инновационные и асимметричные подходы у нас есть.
Взгляд на старость как на постгеномное наследственное заболевание СК человека, предложенный авторами книги, мне понравился, так как в настоящее время исследователи всего мира все больше задаются вопросом, как происходит старение на уровне одной клетки. С системных позиций в организме человека старение на уровне СК особо актуально, так как СК считается нестареющей и бессмертной клеткой и способна в определенных условиях делиться симметрично (на две одинаковые СК) и ассиметрично (на СК и клетку, способную стать любой соматической клеткой организма). Давно известно, что у многоклеточных организмов есть потенциально бессмертные клетки — половые клетки и СК, а вот соматические клетки как результат их асимметричного деления запрограммированы на смерть. Одной из важных черт старения у всех многоклеточных организмов является постепенная утрата в процессе жизни тканеспецифичных СК, которые способны к самообновлению и в ходе дифференцировки могут превращаться во все другие виды соматических клеток. Мы прекрасно знаем, что количество СК в костном мозге 60-летнего человека уменьшается на 60–70%, а к 80 годам их количество в костном мозге единично и способно лишь обеспечить собственное кроветворение. Поэтому утрата СК очень замедляет или делает невозможным системное обновление различных тканей организма и нарушает иммунный контроль и надзор за клетками организма. Старение гемопоэтических, мезенхимальных стромальных и нейральных СК происходит в результате нарушения первичной молекулярно-биологической структуры ГСК и эпигенетического статуса геномной ДНК в них. Огромное количество как внешних, так и внутренних факторов окружающей среды и гемостаза организма влияет на геном каждой клетки, в том числе СК, вызывая в ней множество мутаций ДНК: точечные замены отдельных нуклеотидов, двухцепочечные разрывы, хромосомные перестройки (например, инверсии — поворот участка хромосомы на 180°), укорочение концевых (теломерных) районов хромосом и т. д. Итогом этого феномена становятся постгеномные, а преимущественно транскриптомно-протеомные изменения в тканеспецифичных мультипотентных СК. Протеомные эпигенетические изменения в СК являются важным механизмом их старения и проявляются накоплением белков с неправильной структурой. Появление онкоспецифических белков в тканеспецифичных СК приводят к формированию опухолевой СК и возникновению и манифестации рака и других злокачественных новообразований. Считается, что каждый человек способен дожить до своего рака! Критическое накопление онкоспецифичных белков в ГСК приводит к формированию ОСК крови, приводящих к возникновению гемобластозов (лимфом, лейкозов, миеломной болезни и т.д.), а наличие патоспецифических белков в ГСК становится причиной формирования аутоагрессии ее потомков (иммунокомпетентных клеток) к собственным высокодифференцированным клеткам, запуская аутоиммунные системные и локальные воспалительные и аутоиммунные процессы в органах и тканях. Они являются причиной целого ряда фатальных болезней цивилизации, таких как сахарный диабет I типа, обусловленный повреждением бета-клеток поджелудочной железы, аутоиммунный тиреоидит — повреждение в клетках щитовидной железы, рассеянный склероз, манифестирующий в виде очагов демиелинизации в белом веществе нервной ткани головного и спинного мозга, и т. д. В большинстве случаев аутоиммунные процессы, обусловленные постгеномными изменениями ГСК, запускают и приводят к формированию в тканях дистрофических и атрофических процессов и к появлению дегенеративных заболеваний. Агрегация белков, неправильно свернутых в высокодифференцированной клетке, с образованием амилоидов, например в нейронах, связана с развитием возрастных прогрессирующих нейродегенеративных расстройств, таких как болезнь Альцгеймера и болезнь Паркинсона. А накопление FUS-белков и SOD1-белков в мотонейронах ЦНС формирует боковой амиотрофический склероз. С этих позиций, как утверждают авторы монографии, только скорость и время формирования постгеномных протеомных нарушений в тканеспецифичных СК во многом определяет расстояние человека до смерти! В случае высокой скорости формирования постгеномных нарушений в СК и краткосрочности процесса постгеномного перерождения ГСК время приводит к возникновению у человека основных симптомов фатальных болезней цивилизации (сердечно-сосудистых, нейродегенеративных, аутоиммунных, эндокринных и т.д.), которые становятся причиной его смерти от быстро возникающих витальных осложнений, к которым они приводят. При клеточном старении СК существенно изменяются внутриклеточные пути сигнальной трансдукции — молекулярно-биологические механизмы, обеспечивающие правильную передачу сигналов внутри клетки. Степень нарушения внутриклеточного сигналинга в тканеспецифических СК в результате протеомных мембранных, цитоплазматических и внутриядерных повреждений ДНК и белков определяет скорость течения всех биохимических процессов, приводящих к программной гибели (апоптозу) или смерти мультипотентной СК, так как влияет на множество клеточных процессов, таких как энергетический обмен, ответ на оксидативный стресс и другие патогенетические факторы.
Как показали авторы данной монографии в своей работе, если молекулярно-биологические процессы постгеномного изменения проистекают медленно и постепенно во временном континууме жизни человека, то ученые и врачи расценивают дегенерацию и атрофические процессы в органах и тканях как естественную физиологическую старость и естественное изнашивание органов и тканей. В результате медленного процесса повреждения СК в процессе жизни человека их количество в органах и тканях постепенно сокращается и к возрасту 60–70 лет становится критическим и недопустимо низким для соответствующей системной репарации клеток органов и тканей. Весь механизм репарации поврежденных органов и тканей при медленном снижении количества и функциональной значимости тканеспецифических СК приходит в упадок, что приводит к грубым нарушениям иммунопоэза и кроветворения. Именно поэтому, по мнению авторов книги, каждый человек «доживает до своего рака» и других болезней цивилизации только тогда, когда количество и качество его системообразующих клеток иммунопоэза и гемопоэза становятся критическими и в крови формируется клональный гемопоэз. Авторы книги пришли к заключению, что фундаментальной основой старости человека и основных фатальных заболеваний цивилизации является единый системообразующий процесс патологической клональности, обусловленной геномно-постгеномными повреждениями тканеспецифических СК организма, и в первую очередь ГСК, и только скорость этого процесса и время на его завершение определяют расстояние до его закономерного финала, формируют биологические часы и сроки жизни человека. Это натолкнуло их на новые организационно-методические подходы к молекулярно-биологической профилактике старения и борьбе с естественным физиологическим старением.
Сегодня стало понятно, что только уменьшение числа абортов, снижение младенческой смертности и улучшение постнатального и педиатрического медицинского обслуживания, достигнутые нашей страной за последние годы, глобально не могут решить проблемы значимого увеличения продолжительности жизни взрослого населения страны, если для этого не будет предпринят ряд инфраструктурных социальных, структурно-организационных и медико-биологически обоснованных мероприятий. Должны быть отработаны системные медико-биологические мероприятия по здоровому образу жизни и активному долголетию у лиц среднего и пожилого возраста. Необходимо разработать национальную научно-технологическую базу биотехнологий увеличения продолжительности жизни и активного долголетия трудоспособного населения России. Нужна централизованная система биотехнологических мероприятий защиты человека от старения. Необходимы разработка и создание национальной системы персонализированной медико-биологической защиты каждого отдельного человека и алгоритма обеспечения коллективной биобезопасности жизни и выживания всего населения России. Эти подходы становятся особенно актуальными при возникновении реальных угроз российской цивилизации и (или) воздействии поражающих факторов любых планетарных или континентальных техногенных катастроф, стихийных бедствий, мировых войн и локальных военных конфликтов с применением оружия массового поражения или всемирных экологических бедствий.
Как предполагают авторы книги, для увеличения средней продолжительности жизни каждого трудоспособного человека в России на 15–20 лет нужно побеспокоиться об этом в молодом возрасте и из общего процесса старения конкретного организма человека «вывести» (собрать и криоконсервировать) его собственные кроветворные стволовые клетки костного мозга. Реинфузия этих клеток в пожилом возрасте позволит сохранить человеку его активный иммунитет и здоровое кроветворение, восстановить творческий интеллектуальный потенциал и физическое долголетие. Очевидно, что реализация этих системных биомедицинских мероприятий, обеспечивающих своевременную ультрараннюю молекулярно-биологическую и иммунологическую диагностику, лечение и профилактику преждевременной старости и фатальных (сердечно-сосудистых, онкологических, аутоиммунных, нейродегенеративных, эндокринологических) болезней цивилизации, позволит создать всероссийскую сеть безопасного криобанкинга и надежного хранения персонифицированных биологических образцов клеток костного мозга всего взрослого населения страны, разработки и создания биологически надежной системы биотехнологического страхования населения от фатальных заболеваний цивилизации за счет сбора и криохранения биоматериала костного мозга всего населения страны. Да, это дорого, но это важно и необходимо!
Обеспечение возможности клинического применения (реинфузии) клеток пуповинной крови, собранной при рождении человека, и ГСК, заготовленных в молодом возрасте (до 25–30 лет), в позднем возрастном периоде жизни может стать биологическим залогом увеличения продолжительности жизни самого донора, его выживания и полного излечения при возникновении у него болезней цивилизации. Для сохранения большей части населения всей страны эти технологии увеличения продолжительности жизни могут быть применены при возникновении любых необратимых повреждений органов и тканей человека при экологических катаклизмах (землетрясениях, наводнениях, критическом изменении климата и т.д.) мирового масштаба, локальных военных или глобальных конфликтах или всемирных бедствиях, приводящих к массовой гибели населения вследствие их губительного воздействия на природу и экологию Земли, как в результате последствий жизнедеятельности человека, так и не зависящих от него. Мне в целом очень понравился клеточно-инженерный подход к реставрации аутологичных гемопоэтических клеток самого пациента с использованием лекарственной субстанции «Панаген», но, на мой взгляд, этот подход требует очень серьезной системной проработки и большого финансирования дальнейшего исследования столь сложных проектов. Он не менее сложен в объяснении его эффективности, чем проекты по редактированию генома. Более того, по мнению авторов монографии, они создали технологию геномного балансирования, которая может стать альтернативной технологии геномного редактирования и по ряду параметров превзойти ее. Методологический подход геномного балансирования хроматина в патоспецифических клонах ГСК с использованием двухцепочечных ДНК или РНК мне понравился, так как он является менее дорогостоящим и более биобезопасным, чем геномное редактирование. Стране очень нужны подобные нелинейные подходы в науке, и их надо искать, и очень важно, что первые серьезные шаги в этом направлении уже предприняты в эксперименте и клинике! Пожелаю книге доброго пути, а ее авторам — новых творческих успехов и новых научных свершений!
Директор ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. В. И. Кулакова Минздрава России», акад. РАН, проф., д.м. н. Г.Т. Сухих
Введение
К сожалению, человек смертен и любая человеческая жизнь на земле заканчивается смертью, или так называемым закономерным физиологическим концом земного существования каждого человека. Всю свою жизнь мы живем с пониманием того, что в определенный период нашей жизни все закончится и нам придется умирать и «навсегда уйти» из этой жизни. Мы стараемся об этом не думать, т.к. сама мысль об этом неизбежном фатальном финале жизни делает достаточно бессмысленным наше земное существование. Мы постоянно задаем себе вопросы: зачем и для чего мы приходим в этот мир и почему так мало отведено нам пожить в нем? Религия помогает многим из нас смиренно принимать этот скоротечный исход нашей бренной жизни, но сжиться с этой мыслью о «бессмысленности нашего существования» достаточно трудно. Неужели мы приходим в этот мир, чтобы воспроизвести себе подобных, и главная наша миссия — это обеспечение неугасания линии жизни людей на земле?!
Наряду с философскими вопросами «поиска смысла жизни» существуют еще вопросы практические и повседневные, связанные с процессами старения нашего тела. Очень тяжело и грустно видеть, как увядает и стареет с возрастом собственное тело, как дрябнет, обвисает, морщинится и покрывается неэстетичными пигментными пятнами кожа, уходят ее тургор и эластичность, сгибается спина, дряхлеют и истощаются мышцы, заплывает жиром и обвисает складками живот, волосы тускнеют, седеют, становятся ломкими и выпадают, уходят «в никуда» силы, снижаются интеллект и память, улетучивается «жизненная энергия», которая была «мотором» и казалась «вечным двигателем» собственной физической и творческой активности, созидателем всего нового и прогрессивного в этой жизни. Вы все это видите, осознаете и понимаете, что ничего с этим сделать практически не можете. Наблюдая эти печальные факты собственного старения в зеркале и на фотографиях, вы приходите в отчаяние оттого, что на самом деле кардинально ничего нельзя изменить и исправить. Нужно лишь попытаться принять эту неизбежность и смириться с ней. Однако многие из нас пытаются все изменить и поправить, вступают в неравную схватку со временем и надвигающейся неизбежностью старости и смерти. При этом одни люди пытаются противопоставить старости и неизбежно приближающейся «женщине с косой» (смерти) жалкие попытки физической активности (бег трусцой, долгие пешие прогулки, физическую зарядку и т.д.), увеличение количества творческих упражнений и интеллектуально-мнестические потуги в виде запоминания новых стихов или изучения иностранных языков, посещения шахматных турниров, хождение на танцы и в клубы для проведения досуга пенсионеров, освоение новых музыкальных инструментов. Другие люди сражаются со старостью различными видами диетических истязаний своего тела, определяя их в обществе подобных себе системой активного долголетия. Они срочно начинают садиться на различные антикалорийные диеты, активно считать съеденные калории и заниматься спортом, чтобы «сжечь» их, хотя никогда ранее этим серьезно не занимались. Другие стареющие люди начинают ходить к косметологам, пластическим хирургам, геронтологам и другим медицинским специалистам, обещающим полное восстановление и обновление их «увядшего фасада» и сомнительное активное долголетие на гормональных лекарственных препаратах и биологически активных добавках к пище. Хирургические подтяжки лица делают нас похожими на сотни и тысячи других таких же жаждущих молодости людей, а введение различных коллагеновых гелей, золотых нитей и гиалуроновой кислоты в различные части кожи вашего тела, как и токсинов ботокса в лицо и руки, с целью разглаживания морщин обезличивает нашу индивидуальность и делает нас похожими на миллионы других молодящихся пожилых людей, пытающихся противостоять старости. Такова реальность, и считается, что современной биологии старения человека пока нечего противопоставить!
Психологи утверждают, что очень важно для того, чтобы жить комфортно, не думать об этом печальном конце и надвигающейся физической и интеллектуальной немощности. Кому-то философия старости и сам процесс собственного старения нисколько не мешают и даже помогают легко принять эту неизбежность собственного летального конца и радоваться жизни до последней ее капли. Для других, наоборот, основным путем борьбы с инволюцией и старостью организма являются уход в традиционную религию (христианство, мусульманство, буддизм) или сектанство и соответствующие альтернативные проявления веры в бога, направленные на спасение собственной бессмертной души. Кому-то в борьбе со старением оказывают помощь абсолютный атеизм или собственное безразличное отношение к жизни или окружающим. Другим людям выход из этого психологического тупика «никчемности жизни» и неизбежности смерти видится в уходе в экзотические религии, например, они принимают религиозные представления индусов о возможном переселении души в другие живые существа и неживые предметы. Кому-то из людей помогают не принимать близко к сердцу эту истину врожденный фатализм, собственный эгоизм или просто нежелание думать по этому поводу.
Испокон веков люди пытались бороться с нарастающим процессом старения. Еще фараоны Древнего Египта искали Грааль вечной молодости, чтобы остановить процесс своего возрастного увядания и найти универсальное средство против старения. Все, что им удалось, так это сохранить на тысячелетия свое мертвое тело от гниения путем его мумификации. Древний Рим и Древняя Греция помнят Александра Македонского, поработившего полмира в поисках средства от старения и вечной жизни. Не найдя Грааля вечной молодости, он умер от банального панкреатита в результате отсутствия воды и необходимости злоупотребления вином для удовлетворения банальной жажды при возращении домой из своего победоносного похода.
Вся алхимия Средних веков была сосредоточена на поиске средства от старения и для увеличения продолжительности жизни. Но эти попытки так и не увенчались успехами. Химики XVIII–XIX вв. также пытались найти реальное средство для увеличения долголетия человека. Однако реальные успехи в увеличении продолжительности и улучшении качества жизни были достигнуты человечеством только в конце ХХ в., а самые разительные результаты были получены на животных за последние 20–30 лет. Именно комплексный системный подход к антистарению и реальные достижения научного прогресса общества в геномике, постгеномных и клеточных технологиях регенеративной медицины, а также меры государственной поддержки программ долголетия в развитых экономиках мира позволили достичь ощутимых результатов в увеличении продолжительности жизни и реализации концепции антистарения.
Последние 2–3 десятилетия проблема антистарения и активного долголетия стала центральной у населения, большую часть которого в XXI в. стали составлять преимущественно люди старше 55–60 лет в России и старше 75–80 лет в экономически развитых странах Европы и в США. Избыток в мире пожилых людей ищет реальный выход из проблемы старости путем продления активного физического и интеллектуального долголетия. Мировая индустрия антистарения и долголетия пытается сделать стариков красивыми и активными и предложить им различные программы антистарения, или, как модно сейчас говорить, антиэйджинга (от англ. pre-aging, antiaging — «против старения»).
Поисковая система Google в интернете нашла 122 млн сайтов о старении и об антиэйджинге с рекомендациями и советами разных специалистов. Это спектр самых различных советов, предложений и комплексных программ — от оздоровления кожи и тела человека с использованием нескольких миллионов рецептов диет, различных разрешенных к клиническому применению пищевых биологически активных добавок, минералов, витаминов и микроэлементов до программ изнуряющего бега, спортивной ходьбы, йоги, а также йогоподобных упражнений в качестве изматывающего жиросжигающего тренинга. Сюда же относятся различные косметические процедуры и питательные маски для лица и тела, аппаратная мезотерапия и криопроцедуры, сочетающиеся со специализированным фитнесом (физические нагрузки под контролем инструктора) и введением разных типов донорских стволовых клеток, при которых человек якобы оздоравливает основные части своего тела и естественным образом становится красивым, а процесс старения резко замедляется или вообще останавливается. В общем, арсенал средств для ревитализации (омоложения) и антистарения растет постоянно, и в настоящее время мировой рынок продуктов долголетия и антиэйджинга достигает сотен миллиардов долларов США и имеет отчетливую тенденцию к росту.
Еще одним направлением борьбы со старением является эстетическая и пластическая хирургия. Насколько она эффективна, мы видим с экранов телевизора и в интернете по внешнему виду телеведущих и по ряду программ, где бывшие пациенты пластических хирургов, очень похожие друг на друга, или выступают с претензиями к своим врачам, или с судебными исками к ним. Однако, к сожалению, эффективность борьбы со старостью и активного противостояния смерти у человечества существующими методами, а также технологии увеличения средней продолжительности жизни человека пока не столь удачны, как хотелось бы. Достичь каких-то реальных результатов на практике пока удалось только в экспериментах на животных, а реальных эффектов антистарения на людях, ко всеобщему разочарованию, пока не получено, хотя абсолютно точно, что продолжительность жизни человека существенно увеличилась за последние десятилетия.
Выяснилось, что средняя продолжительность жизни (СПЖ) населения в различных странах мира является важным показателем в оценке демографической ситуации в каждой стране. Для вычисления СПЖ используются формулы из теории вероятности и данные о смертности различных возрастных групп за год. Как показали эти исследования, качество жизни и долголетие человека напрямую зависят от условий проживания, климата, экологической обстановки в зоне проживания, состояния здоровья, а также от уровня заботы и лечения в случае заболеваний. Современная мировая медицина за последние 50 лет совершила качественный скачок в своем развитии. Так, продолжительность жизни в экономически развитых странах мира в 2019 г. стала существенно выше, чем в нач. и сер. ХХ в. Ориентироваться на среднюю продолжительность жизни в 2020–2021 гг. будет некорректно из-за мировой пандемии COVID-19. Если родившиеся в 1900 г. в среднем по миру доживали до 48–50 лет, то сейчас этот показатель в среднем по миру приближается к 70 годам.
Увеличение СПЖ по миру связано с иммунизацией населения от большинства инфекционных заболеваний с использованием прививок, искоренением случаев и профилактики эпидемий особо опасных инфекций и уменьшения младенческой смертности. Не менее важным в увеличении СПЖ населения является тот факт, что проблемами профилактики инфекционных процессов занимаются системно и глобально на уровне Всемирной организации здравоохранения, а также что иммунизацией населения в развитых странах мира занимаются на государственном уровне. В мировом рейтинге по СПЖ Япония занимает ведущее положение, т.к. она составляет 82,75 года (мужчины — 82,4, а женщины — 85,1). В списке стран, занимающих лидирующее положение по СПЖ, — Франция, Италия, Испания, а в арьергарде — африканские государства (Ангола, Замбия и др.), раздираемые военными конфликтами, где население проживает за чертой бедности, где средняя продолжительность жизни 40 лет. СПЖ в России в 2019 г. составляет 72,4 года (65 лет для мужчин и 80 лет для женщин).
Но так ли всё бесперспективно в борьбе со старением и можно ли реально увеличить свою продолжительность жизни на этом белом свете? На первый взгляд — нет, все фатально и давно за нас продумано и предрешено нашим Создателем (Природой, Эволюцией или Богом — кому как ближе). Любой пессимист вам скажет, что никаких шансов нет в принципе. Но это не совсем так и даже, наверное, совсем не так! Как все оптимисты, мы всегда знаем и помним, что всегда есть выход из любого самого трудного положения и надо только постараться его найти и не поддаваться отчаянию. А это иногда требует невероятных усилий!
У нашей небольшой научной группы существует свой авторский и достаточно альтернативный взгляд на эту проблему, и это исключительно наша точка зрения на процесс биологии старения. Она позволяет нам предположить, что человек теоретически способен жить до тысячи лет. Это концептуально и биотехнологически обусловлено тем, что все известные клетки организма человека, кроме клеток нервной ткани, способны к постоянному самообновлению; также к самообновлению, к системной регенерации и реставрации способны почти все органы и ткани, кроме головного и спинного мозга. Открытие стволовых клеток (СК) в органах и тканях человека и млекопитающих позволило понять и раскрыть сущность процессов регенерации органов и тканей организма и понять, что все клетки человека способны быть заменены на новые при их старении или повреждении, за исключением клеток центральной нервной системы (ЦНС). Оказалось, что клетки нервной системы млекопитающих и человека «одноразовые» и замена их очень ограничена в процессе жизни человека и крайне затруднена при повреждении, но частично тоже технически возможна! Открытие этой способности ограниченной регенерации нервной ткани стало возможным только в конце ХХ в., с открытием нейральных стволовых клеток (НСК). Поэтому проблема самообновления поврежденных и старых соматических клеток в организме человека фактически давно была решена Создателем путем наличия в организме бессмертных тканеспецифичных мультипотентных СК. Другое дело, что их количество, геномная и протеомная структура также меняются с возрастом, обусловлены наследственным генетическим заделом и фактическими экологическими условиями проживания человека. Оказалось, что теоретически бессмертные СК также стареют, изнашиваются и умирают. СК, как и весь организм человека, в процессе жизни подвергаются молекулярно-биологическому повреждению, особенно если они находятся в экстремальных условиях окружающей среды и подвержены частым встречам с новыми бактериальными и вирусными агентами. В неблагоприятном внутреннем и внешнем микромире СК человека и млекопитающих стареют и умирают. Сегодня установлены основные механизмы старения любой клетки, в т. ч. СК, и доказано, что регенерация клеток возможна во всех органах организма и даже немного в ЦНС. Показано, что в головном и спинном мозге млекопитающих и человека есть НСК, обеспечивающие незначительную регенерацию, но их количество достаточно ограничено спецификой функций нервной ткани. Невозможность и малая целесообразность физического самообновления клеток нервной ткани связаны с тем, что все процессы формирования нейронных сетей и функциональных связей и синапсов в мозге человека обусловлены исключительно экзогенными факторами (воспитанием, образованием, обучением в семье, школе и различных учебных заведениях или просто в процессе трудовой деятельности и жизни) и специфической анатомией. Человек рождается с маленькой головой, где, по общеустоявшемуся мнению ученых, имеется 100 млрд нейронов (по мнению Сюзанны Геркулано-Хаузел, их 86 млрд), и умирает, когда размеры его головы превышают первоначальный размер в 10 и более раз, но при этом количество нейронов его мозга уменьшается на порядок, а то и более. Количество нервных клеток за всю жизнь человека практически не увеличивается или увеличивается крайне незначительно, а вот размеры нервных клеток увеличиваются в несколько сотен раз, и размеры аксона моторного нейрона достигают длины до 1 м и более. Нейроматематика и математическое моделирование жизненного цикла нейрона и большинства клеток нервной ткани человека показали потенциальную возможность нейрона прожить до тысячи лет (Галушкин, 2015), если будет обеспечено его благоприятное клеточное и сосудистое микроокружение. Остальные же клетки организма способны к постоянному самообновлению и регенерации под контролем собственной иммунной системы и СК, что происходит в обычной жизни. Другими словами, организм человека имеет потенциальную биологическую возможность и морфологическую состоятельность своих клеточных систем, чтобы дожить до тысячи лет, т.к. системообразующие сознание нервные клетки мозга (нейроны) и их строма (астроциты, олигодендроциты, нейроглия и микроглия) физически способны прожить этот период без дополнительного деления, а вот деление и самообновление их приведет к разрушению аппарата поддержания сознания и нарушению структуры личности человека. Итак, нейроны, костные клетки и мышечные клетки человека физически способны и могут жить до тысячи лет, а все остальные клетки способны самообновляться из существующих ресурсов собственных тканеспецифических стволовых клеток. Гемопоэтические стволовые клетки способны трансформироваться в любые тканеспецифические стволовые клетки и стать родоначальниками любого из 220 типов тканей.
Да и наш Создатель не возражает против столь длительной жизни человека в этом мире. Первые люди на земле, согласно Библии, жили в среднем 960 лет. Так, Адам, первый человек на земле, прожил 930 лет, а его сын Мусфаил, рожденный от Евы, когда ей было около 600 лет, прожил 970 лет. А раз наш Создатель принципиально не против столь длительного проживания человека на земле, то и нам как людям разумным, по-видимому, имеет смысл задуматься над тем, как приблизиться к тем пределам жизни, которые рекомендованы божественным промыслом и естественной, биологически детерминированной нейрофизиологией человека. Согласно Библии, эти сроки жизни древних людей были реальны еще каких-то 3–4 тыс. лет назад. Но надо попытаться понять, что же нам мешает прожить этот генетически детерминированный срок жизни в тысячу лет, дарованный нам нашим Создателем при переселении на Землю!
То есть еще 2,5–3,5 тыс. лет назад (время, описанное в Библии) продолжительность жизни в 900 лет была реальным фактом жизни рядового человека и изменилась лишь за последние 2 тыс. или, возможно, даже меньшее количество лет существования человечества. Мы не знаем и вряд ли узнаем, что тогда произошло на земле и что так кардинально изменило сроки жизни человечества и уменьшило продолжительность жизни отдельно взятого человека в 10 и более раз. Мы можем лишь догадываться о том, что в результате какого-то планетарного катаклизма в космосе и как следствие, глобальной климатической катастрофы на Земле изменились экологическая ситуация и условия окружающей среды, в которой проживал древний человек. Движение ледника с Северного полюса на Европейскую часть Земли произошло внезапно и глобально изменило судьбу большинства видов живых существ на планете. Возможно, это было связано с тем, что изменилось атмосферное давление, или с насыщением кислородом воздуха из-за истончения озонового слоя биосферы. Возможно, изменился радиоактивный фон из-за повышения солнечной активности, поменялся астрономический наклон оси Земли и изменилась температура морей и океанов или существенно похолодало и глобально изменился климат на всей нашей планете из-за глобального ледникового периода на Земле. Но что бы ни произошло на Земле 2,5–3 тыс. лет назад, это событие существенно изменило и адаптировало программное биологическое обеспечение системообразующих механизмов гомеостаза организма человека и всех млекопитающих к новым условиям существования на нашей планете и привело к адаптированному и детерминированному изменению ограничения продолжительности человеческой жизни в этих конкретных условиях выживания и к необходимости приспособления. Возможно, что у человека произошли необратимые мутации в его геноме и протеоме клеток, что и привело формированию ограничений предела жизни всего организма до максимальных пределов в 100–120 лет к настоящему времени. Но чтобы понять, что произошло и что с этим делать, нужно фундаментально проанализировать сложившуюся ситуацию и разобраться в пестрой мозаике научных фактов и экспериментальных данных, уже накопленных за последние 2–3 десятилетия в области молекулярной биологии старения и генетики, исследований различных способов увеличения продолжительности жизни человека и долголетия. А их сегодня очень много, и они требуют систематизации и нового понимания и переосмысления.
Основной естественной причиной смертности населения в мире в сер. XX и нач. XXI в. является смерть от старости и от возрастзависимых болезней цивилизации (БЦ). Люди привыкли думать, что старение и смерть человеческого тела и вообще живых существ — это эволюционно обусловленный и закономерный процесс, он естественный и нормальный и по-другому быть не может, да и не должно. Однако ученые из разных стран мира уже показали обратное: оказалось, что на Земле существует множество видов растений и животных, которые не стареют! В число нестареющих и «бессмертных» попали такие животные, как гидра, рак-отшельник, большая синица, некоторые ящерицы и моллюски, красноногая лягушка, черепаха Gopherus agassizii, голый землекоп, ночница Брандта (летучая мышь) и др. Все больше ученых-биологов и генетиков приходят к выводу, что одряхление организма с возрастом — это вовсе не фатальный закон природы, а нарушение системных процессов регуляции иммунитета, гемопоэза и саногенеза организма человека. Европейскими учеными было высказано научно обоснованное мнение, что старение — это болезнь, которую можно лечить и профилактировать, как и любое заболевание. И это положение сегодня практически не оспаривается ведущими мировыми учеными — врачами-геронтологами и молекулярными биологами. Не очень понятно, о какой конкретно болезни идет речь в этих работах, но сам факт старости как проявления запрограммированного в геноме инволюционного процесса и системного общеорганизменного заболевания человека для большинства ученых очевиден и уже не вызывает сомнения в настоящее время.
Другой основной причиной высокой смертности населения в мире, кроме старения, стали сердечно-сосудистые, онкологические, нейродегенеративные и аутоиммунные болезни человека, до которых раньше не доживало большинство населения развитых государств, и это явление стало смертельным бичом современной цивилизации. Поэтому если в ближайшее время будут найдены способы ультраранней диагностики и лечения основных БЦ, то жизнь человека может быть увеличена очень значимо. Отсутствие способов ультраранней доклинической диагностики большинства БЦ приводит к тому, что из-за их бессимптомного течения обычные методы современной медицины позволяют их диагностировать только на самых поздних этапах патологического процесса, когда уже нельзя помочь пациенту с БЦ. Например, боковой амиотрофический склероз (БАС) или болезнь моторного нейрона (БМН) на современном этапе научного прогресса можно диагностировать только тогда, когда погибло уже более 70–80% мотонейронов головного и спинного мозга пациента и помочь такому человеку практически уже не представляется возможным (Брюховецкий, 2021). Аналогичная ситуация и с болезнью Альцгеймера (БА) и большинством злокачественных онкологических заболеваний и раков различной локализации, которые диагностируются на III и IV стадиях патологического процесса (Брюховецкий А. С., Брюховецкий И. С., 2020), когда эффективность патогенетической терапии практически сведена к нулю.
В этой книге мы бы хотели поговорить о реально существующем, но скрытом биологическом потенциале антиэйджинга у человека и тех достаточно простых инструментах для манипуляций с ним, которые были обнаружены нами в процессе изучения этой проблемы и в наших экспериментальных работах на животных и человеке. Оказалось, что реально продлить саногенетический функционал собственного организма человека достаточно просто. Например, если в молодом возрасте путем эксфузии костного мозга собрать небольшую часть ГСК и МССК из КМ или путем лейкоцитофереза собрать мобилизованные гранулоцитарным колониестимулирующим фактором (Г-КСФ) те же самые клеточные системы МНК из ПК и заморозить их в криопрофилактике типа жидкого азота с диметилсульфоксидом (ДМСО) по стандартной методике программного замораживания и затем провести их реинфузию в пожилом возрасте (65–70 лет), то это позволит их сохранить в неизменном виде и полностью исключить их из процесса общего старения организма. То есть эти клетки не накопят того закономерного количества дополнительных соматических мутаций, которые получат клетки, находящиеся в организме человека в процессе его жизни. Это позволит части собственных высокоактивных и биологически здоровых ГСК и МССК сохраниться в неизменном виде несколько десятилетий жизни, не подвергаясь процессам старения, и сохранить их до того периода, когда количество этих системообразующих регуляторных клеток уменьшится в КМ в 10 и 20 раз. А это происходит, как правило, уже к 60–65 годам у каждого. Банальная внутривенная реинфузия этих здоровых клеточных систем КМ и их приживление в собственном КМ способны восстановить поврежденный временем или болезнью цивилизации иммунопоэз, гемопоэз и саногенез человека и значимо продлить жизнь человека, почти на 20–30%. По крайней мере, на животных мы это убедительно показали, и далее в последующих главах этой монографии мы проиллюстрируем этот феномен на экспериментальных данных.
Сегодня найдено несколько новых путей реставрации поврежденных ГСК КМ, что также открывает пути увеличения продолжительности и улучшения качества жизни у человека, который не побеспокоился об этом заранее и не собрал в молодости свои клетки КМ. Перефразируя известную пословицу «Береги честь смолоду», можно утверждать: «Сохрани свое биологическое здоровье смолоду, собрав и заморозив свой КМ в возрасте до 25–30 лет!» Тогда вы на 15–20% можете увеличить продолжительность и качество своей жизни в старости и биологическим путем продлить свое активное физическое и творческое долголетие. Однако начнем по порядку, чтобы ничего не упустить и не создавать у читателя ощущения простоты и банальности этих высокотехнологических биомедицинских подходов к продлению активного долголетия человека, да и ко всей проблеме современного антиэйджинга.
Слово «антиэйджинг» очень широко используется в нашей стране еще с конца 90-х гг. прошлого века. Руководитель лаборатории иммунологии ГУ НИИ акушерства, гинекологии и перинатологии РАН, тогда уже профессор иммунологии, д.м. н. Геннадий Тихонович Сухих, ныне академик РАН и директор ФГБУ НМИНЦ акушерства, гинекологии и перинатологии им. В. И. Кулакова Минздрава России, одним из первых в нашей стране стал использовать этот зарубежный термин. Мы услышали от него этот термин в ноябре 1989 г. в его разговоре с прибывшим в Россию американским ученым профессором Майклом Молнером при обсуждении ими существующих на тот период научных взглядов на проблему антистарения и активного долголетия в мире. Тогда мы были сильно удивлены уже существующими методами и способами омоложения человека, разработанными в США с использованием впервые тогда появившихся в России клеточных технологий на основе применения фетальных клеток человека и животных. Майкл Молнер рассказывал о научной революции в геронтологии и буме ревитализации (омоложения) в США с использованием клеточных фетальных препаратов. Оказалось, что эта проблема занимает умы американской элиты Кремниевой долины, и М. Молнер предлагал применять фетальные клетки в России с целью улучшения качества жизни и внешнего вида наших пациентов. Из-за собственной молодости и абсолютного непонимания данной проблемы мы как-то не очень правильно среагировали тогда на эту беседу двух крупных ученых, и их перспективные проблемы нам показались абсолютно надуманными и несерьезными. Один из нас тогда был молодым и увлеченным ученым и военным врачом, которого беспокоили исключительно боевая травма мозга и все проблемы, связанные с ее решением, а другой видел будущее в понимании фундаментальной роли ДНК в процессах репарации и восстановления клеток и органов человека. Однако все 30 лет своего научного общения с акад. РАН, проф. Г. Т. Сухих мы постоянно слышали от него это раздражающее русское ухо слово «антиэйджинг». Иногда казалось, что это самое любимое научное слово акад. РАН, проф. Г. Т. Сухих! Сначала на слово «антиэйджинг» мы реагировали как на что-то инородное и малонаучное, но затем поняли, что не только акад. Г. Т. Сухих любит это определение антивозрастных манипуляций и процедур, но уже весь мир понимает это «странное английское» слово как определенную систему антивозрастных лечебных и профилактических мероприятий, как неотъемлемую часть огромной мировой медико-биологической индустрии красоты и долголетия. Именно системные мероприятия по антиэйджингу стали важным инструментом увеличения средней продолжительности жизни человека в экономически высокоразвитых странах. И только с возрастом каждый из нас стал задумываться о возможности увеличения собственной продолжительности жизни, о проблемах потенциального активного долголетия и антистарения; мы вспомнили об уроках акад. РАН Г. Т. Сухих и его антиэйджинговых программах. Более того, каждый из авторов этой книги стал интересоваться этими деликатными вопросами очень активно, и это для нас обоих оказалось настолько интересно и захватывающе здорово с современных научных медико-биологических позиций и экспериментальных достижений, что мы с головой ушли в изучение этой проблемы и даже написали монографию на эту тему.
Много позже, находясь в г. Орландо в США на одной научной конференции по регенеративной медицине, мы случайно попали в специализированный магазин товаров для антиэйджинга. Мы стояли как зачарованные перед прилавками этого потрясающего изобилием товаров магазина и вдруг осознали всю значимость и величие этого английского слова, и стало понятно, что нам не хватит жизни прочитать только названия и механизм действия этих чудодейственных средств и снадобий и, конечно, не хватит американских денег на то, чтобы попробовать хотя бы малую их эффективность на себе. Миллионы баночек, пузырьков, гранул, мазей и таблеток с блестящими этикетками и зазывными названиями обещали вечную жизнь, долгую молодость и активное долголетие, половую активность и вернуть потерянную энергию жизни. При этом огромное количество людей магазина как-то очень лихо ориентировалось в море информации об антистарении и долголетии. Они задавали консультантам-продавцам какие-то «очень правильные» вопросы, и продавцы этого магазина приносили им все новые и новые средства и снадобья, которые расходились среди покупателей, как горячие пирожки среди голодающих. Только тогда мы впервые обратили внимание на тот факт, что антиэйджинг — это очень серьезная мировая проблема, которая волнует миллионы людей и реально способна решить сложные демографические ситуации в разных странах мира, и сто́ит эта проблема каких-то немыслимых денег. В том же магазине антиэйджинга мы для себя поняли один очень важный научный факт: раз существует такое невероятное количество средств антистарения, значит реального средства от старости все-таки нет, и его надо попытаться найти. Раз каждое из этих средств как-то помогает и раз их так активно покупают, по-видимому, они работают не на причину старения, а направлены на нивелирование последствий процесса биологии старения. Чтобы бороться со старением, нужно понять системообразующие факторы процесса биологии старения и профилактировать их, а не пытаться ловить и лечить следовые последствия увядания организма в процессе старения.
Сначала у нас ничего не получалось, мы в своих исследованиях сваливались в мелочевку проблем биологии старения и были вынуждены на определенное время отказаться от этих важных исследований. Очень быстро мы увлеклись возрастзависимыми онкологическими заболеваниями, онкопротеомикой и постгеномными технологиями изучения рака и других злокачественных новообразований (ЗНО) и вдруг осознали, что в биологической основе формирования рака и других ЗНО, аутоиммунных и нейродегенеративных заболеваний лежит протеомное повреждение собственной ГСК и ее иммунокомпетентных потомков и как следствие — почти всех иммунокомпетентных клеток организма. Обсуждая между собой эту тематику, мы пришли к неожиданному выводу, что не столько геномные, сколько именно протеомные, транскриптомные, метаболомные и секретомные нарушения в костно-мозговых ГСК являются истинной причиной большинства болезней цивилизации. В итоге нам показалось, что мы уловили и поняли одну очень важную системную закономерность: нами был установлен научный факт геномно-протеомного переформатирования ГСК как фундаментальной основы нарушения иммунопоэза и гемопоэза организма не только при БЦ, но и в процессе старения. Стало очевидно, что в основе старения и возрастзависимых болезней цивилизации лежит формирование патологического моно- или олигоклонального гемопоэза (кроветворения), т.е. формирование собственных патоспецифических нозоспецифических клонов ГСК и ГПК. Так, в дальнейшем для себя мы сформулировали теорию старения как постгеномную клонально-кроветворную болезнь, в первую очередь болезнь клональной гемопоэтической стволовой клетки человека, а также постгеномного заболевания и других тканеспецифических стволовых клеток организма. Мы стали интересоваться научными исследованиями о долгожителях и читать литературу о биологии старения и нашли в них подтверждение своим предположениям и догадкам.
Можно сказать, что изначально история антиэйджинговых (антивозрастных) исследований в мире началась с того, что ученые взялись всерьез за изучение нестареющих организмов — как людей-долгожителей, так и животных с растениями, и с каждым новым открытием ученые приближаются к тому, чтобы понять процессы биологии старения, обнаружить их причины и продлить жизнь человека. Однако чем больше они узнавали о возможности блокирования процесса старения, тем более запутанной и неоднозначной становилась сама проблема. Напомним, что все известные этапы увеличения продолжительности жизни человека и уменьшения его смертности связаны с определенными научными открытиями человечества (открытие антибиотиков, изобретение вакцин, создание инсулина, разработка и создание противоопухолевых таргетных и онкоиммунных лекарственных препаратов, открытие стволовой клетки и т.д.), проведением системных противоэпидемических и карантинных мероприятий, созданием специализированной инфраструктуры высокотехнологичной медицины. Каждый из этих этапов истории человечества увеличивал продолжительность жизни человека на 10–15 лет.
К сожалению, существующие современные научные подходы к увеличению продолжительности жизни и активному долголетию человека путем изменения системы его физической активности, занятий спортом, создания оптимальных диет и режимов питания и еще целого ряда социально-экономических факторовеще очень несовершенны и не имеют достаточно убедительных доказательств своей эффективности, хотя и способны значительно улучшить качество жизни человека в пожилом и старческом возрасте. Очевидно, что увеличение продолжительности жизни и долголетие каждого на сегодня во многом зависят от генетики, условий и места проживания, профессиональных вредностей и еще целого ряда не зависящих от человека экологических и социально-экономических факторов окружающей среды. Существует еще определенное количество факторов, о которых мы еще не знаем и не можем оценить их роль в этом процессе. Наиболее вероятно, что реальный прогресс в этом направлении будет достигнут только тогда, когда мы научимся управлять биологией процесса старения, научимся диагностировать и лечить болезни цивилизации, приводящие к смерти, на самом зачаточном этапе их возникновения и поймем основные механизмы процесса регенерации и саногенеза организма человека при повреждении органов и тканей. В любом случае прогресс в этой области возможен только через решение проблем биоуправления и биорегуляции процессов клеточной и молекулярной биологии старения и патобиологии возникновения болезней цивилизации.
Мы полагаем, что решение основных демографических проблем России возможно не столько за счет финансового и социально-экономического стимулирования граждан страны к деторождению и снижению смертности рожденных и недоношенных российских граждан, сколько исключительно через системные медико-биологические и организационно-методологические мероприятия, проводимые обществом и Минздравом России, путем создания специализированной медико-биологической инфраструктуры для практического решения этих важных проблем! До настоящего времени все реальные достижения увеличения продолжительности жизни человечества связаны с определенными научными открытиями и системными мероприятиями, проводимыми биологами (микробиологами, эпидемиологами и молекулярными биологами) и врачами в целях лечения и профилактики определенных заболеваний человечества.
Так, глобальная смертность населения от эпидемий особо опасных инфекций была остановлена после открытия возбудителей бактериальных болезней, выяснения механизмов возникновения инфекционных болезней и создания единой системы карантинов и санитарно-гигиенических мероприятий. Преодоление смертности от детских инфекций и ряда вирусных болезней было осуществлено путем создания международной и национальной системы детских прививок и глобальной вакцинации взрослого населения. Очередное увеличение продолжительности жизни людей на 15–20 лет произошло в эру открытия антибиотиков. Внедрение в онкологию инновационных молекулярно нацеленных (таргетных) лекарственных препаратов и иммуноонкологических средств на основе моноклональных антител увеличило продолжительность жизни населения в экономически развитых странах также на 15–20 лет (по данным ВОЗ). Мы считаем, что проблема увеличения долголетия человека должна быть также решена через создание специализированной инфраструктуры и системы программных мероприятий с оборотом (сбором, хранением и применением) собственных стволовых клеток костного мозга как фундаментальной биологической основы долголетия. В этой книге мы попытаемся обосновать свой научный взгляд на данную проблему и свою биологическую концепцию увеличения продолжительности жизни и активного долголетия.
В этой монографии мы практически не будем говорить о диетах, физических упражнениях, биологически активных пищевых добавках, психологических тренингах и других аспектах социально-экономической помощи для улучшения внешнего вида и долголетия человека. Цели книги: подойти к пониманию фундаментальных биологических основ долголетия человека и создать биологические предпосылки реального увеличения продолжительности жизни за счет известных и хорошо отработанных медико-биологических манипуляций с костным мозгом человека или путем реставрации и восстановления поврежденных стволовых клеток КМ и на основании этих данных попытаться предложить и создать систему мероприятий и специализированную высокотехнологичную медицинскую инфраструктуру для медико-биологически основанного антиэйджинга и увеличения продолжительности жизни населения на 10–15 лет.
Сегодня возможность медико-биологического антиэйджинга экспериментально доказана на линейных животных. Введение КМ молодых животных старым линейным животным, находящимся в состоянии 50% гибели их возрастной группы, увеличила продолжительность их жизни на 28–30%, что было убедительно показано нашими партнерами из НИИ биофизики клетки (г. Пущино Московской области) под руководством ведущего научного сотрудника, к.ф-м. н. Алексея Карнаухова и к. б. н. Марии Ковиной (2018, 2019) из Сеченовского университета (г. Москва) и далее представлено в этой книге.
А что делать тем, кто заранее не позаботился и не сохранил свои ГСК и ГПК или не смог сохранить собственные МССК? В этом случае нами предложено новаторское решение реставрации ГСК и ГПК пожилых людей с использованием двухцепочечных (дц) ДНК и дцРНК, полученных от здоровых доноров или синтетическим путем. Целый ряд новосибирских отечественных исследователей получили уникальные достоверные научные данные о возможности потенциального увеличения продолжительности жизни на 57% и значимого изменения качества жизни, а также улучшения внешнего вида экспериментальных животных от 15 до 75% за счет восстановления молекулярно-биологического потенциала различных компартментов старых ГСК и ГПК млекопитающих (увеличение длины теломер, реставрация митохондрий, репарации ДНК и т.д.) путем реконструкции ГСК и ГПК с использованием дцДНК и дцРНК (Богачев и др., 2001–2019). То есть существует гарантированный сценарий увеличения продолжительности и улучшения качества жизни млекопитающих и человека путем реинфузии собранного ранее молодого криоконсервированного костного мозга старым животным и пожилым людям, и он экспериментально подтвержден М. В. Ковиной с соавт. (2018). Этот подход может биологическим путем обеспечить активное долголетие, не прибегая к молекулярно-биологическим манипуляциям с геномом и эпигеномом. Существует реальная возможность проверить эффективность данного подхода на человеке и масштабировать эти исследования на все человечество. Эти исследования в клинике позволят обеспечить всего лишь целенаправленные незначительные стандартные манипуляции с собственными мобилизованными в ПК гемопоэтическими стволовыми клетками человека, полученными в молодом возрасте и введенными ему же в пожилом или старческом возрасте. Наш подход к реставрации старых ГСК и ГПК человека с использованием дцДНК и дцРНК также позволяет увеличить продолжительность жизни животных на 57%.
Сама постановка инновационных медико-биологических антиэйджинговых исследований с ГСК ПК или костного мозга (КМ) была идеологически задумана, с одной стороны, как потенциальная возможность научного прорыва в геронтологии для создания и широкого внедрения инновационных биотехнологий и медицинского оборудования будущего, а с другой стороны — как абсолютно конкретная, научно-практическая реализация уникальной межгосударственной постановки и решения глобальной мировой демографической задачи здравоохранения. Цели этих исследований: увеличение средней продолжительности жизни человека, проживающего в России, на 15–20 лет за счет восстановления его молекулярно-биологического ресурса выживания; биологическое обоснование увеличения трудоспособного возраста населения России на этот период и продление активного долголетия и творческой жизни долгоживущего населения страны. Экономические преференции и финансовые бонусы для государства, участвующего в этом антиэйджинговом проекте, при возможном практическом решении этой демографической проблемы настолько очевидны и понятны, что даже не стоят дополнительного обсуждения.
Столь высокая планка практической реализации научных достижений в фундаментальной медицине и в клинике была запланирована нами к осуществлению в рамках предлагаемых исследований, применения уникальных прорывных идей и критических биотехнологий передовой исследовательской мысли отечественных ученых. Уровень использования будущих научных результатов и данная научно-практическая постановка проблемы демографии, столь значимой для государства общественно-демографической и социально-экономической задачи, была сделана не нами, а президентом Российской Федерации В. В. Путиным. По своей амбициозности поставленная перед учеными-исследователями и врачами задача была сравнима лишь с полетом человека в космос! Было необходимо сделать шаг в будущее биотехнологий и биоинженерных инноваций, определить новые горизонты, и поставить новые вехи медицины будущего, VI, технологического уклада, и понять наше место в ней.
Но именно подобные амбициозные цели и «пристальный» дальновидный взгляд руководителей страны в наше обозримое будущее двигали человечество к звездам и в глубины мирового океана, позволили преодолеть глобальные эпидемии инфекционных заболеваний и научиться управлять атомной энергией, стать мировыми лидерами в атомной энергетике и гидроэнергетике, осуществлять полеты в космос, осваивать новые месторождения природных ископаемых и углеводородов и т. д. Для этого президент Российской Федерации рекомендовал ученым, согласившимся на разработку, создание и реализацию подобного проекта, найти нестандартное и ассиметричное решение данной задачи (Послание к Федеральному собранию, 2017). Мы считаем, что мы выполнили указание нашего президента и нами был найден новаторский ассиметричный подход к проблеме увеличения продолжительности жизни россиян и увеличения их активного долголетия.
В указе президента Российской Федерации от 7 мая 2018 г. №204 «О национальных целях и стратегических задачах развития Российской Федерации на период до 2024 года» (далее — указ №204) поставлена общенациональная цель — увеличить ожидаемую продолжительность жизни (далее — ОПЖ) с нынешних 72,7 года до 78 лет к 2024 г., и для ее реализации были сформированы национальные проекты. В Послании к Федеральному Собранию Российской Федерации 20 февраля 2019 г. еще раз подчеркнуто, что национальные проекты направлены на достижение нового качества жизни для всех поколений, сбережение народа и недопустимость отступления от намеченных рубежей.
Следует отметить, что Правительству РФ за 5 лет (2012–2017) удалось добиться роста ОПЖ на 2,5 года (с 70,2 до 72,7) благодаря выполнению государственной программы «Развитие здравоохранения» и реализации мер по антитабачной и антиалкогольной политике (официальная статистика). Этот результат был достигнут в условиях, когда (за этот же период) государственные расходы на здравоохранение сократились на 18% в постоянных ценах (с 2,3 до 1,9 трлн руб.). Но, несмотря на все усилия государства по увеличению продолжительности жизни, общий коэффициент смертности в последние 5 лет стагнирует на уровне 13,0–13,1 случая на 1 тыс. населения. Последствия пандемии коронавируса COVID-19 в 2020–2021 гг. увеличили этот показатель в 2 раза.
В соответствии с указом №204 государственными структурами были разработаны национальные проекты, направленные на увеличение ОПЖ и на снижение смертности населения, основные из которых — «Здравоохранение» и «Демография». Общее финансовое обеспечение проекта «Здравоохранение» за 6 лет составит 1,73 трлн руб., из них 79% — за счет средств федерального бюджета. В среднем увеличение расходов на национальный проект «Здравоохранение» ежегодно составит ок. 290 млрд руб. в текущих ценах. Это ок. 9% к объемам государственного финансирования здравоохранения в 2018 г. (3315 млрд руб.). Причем эти 290 млрд руб. ежегодно будут подвергаться инфляции в среднем на 4% (согласно прогнозам Минэкономразвития России). Это означает, что предусмотренное увеличение расходов на здравоохранение ниже, чем получено в сценарных расчетах, где показано, что для достижения ОПЖ 78 лет к 2024 г. потребуется увеличение государственных расходов в 51,73 трлн руб. на 6 лет, что равно 290 млрд руб./год на здравоохранение, не менее чем на 15% ежегодно в постоянных ценах (Улумбекова и др., 2021).
Общее финансирование национального проекта «Демография» на 2019–2024 гг. из всех бюджетных источников составляет 3,1 трлн руб. за 6 лет. Из них средства федерального бюджета составляют 96%. Непосредственное влияние на увеличение ожидаемой продолжительности жизни будут оказывать следующие проекты: «Старшее поколение», «Укрепление общественного здоровья» и «Спорт — норма жизни».
Национальные проекты «Долголетие человека» и «Здравоохранение» планируют потратить в ближайшие годы 4,4 трлн руб. на возможность увеличения продолжительности жизни человека и его активное долголетие, не привнеся ничего кардинально нового в само понимание процесса старения и долголетия. Основной упор в этих исследованиях будет сделан на постройку устаревшей инфраструктуры первичного звена медицины и наращивание мощности специализированных высокотехнологичных национальных медицинских научных центров и инфраструктуры домов престарелых, а также на оздоровительные мероприятия физкультуры и спорта. Но, к сожалению, это никак не увеличит продолжительность жизни населения страны. Никаких кардинально новых и научно обоснованных мероприятий в проекте не предусмотрено. Это связано с тем, что ВОЗ и ведущие национальные и мировые эксперты в области долголетия связывают возможность увеличения продолжительности жизни исключительно с решением проблем улучшения мировой экологии, создания бесстрессовой среды и низкокалорийных диет, повышения физической активности и социально-экономического благополучия человека и еще целого ряда финансовых и психологических аспектов проблемы старения. Но за этот короткий период мы физически не сможем изменить экологию, которую люди разрушали все предыдущие столетия, уменьшить выбросы в атмосферу целого ряда промышленных предприятий из экономически развитых стран и устранить количество тех стихийных свалок мусора, которые есть в нашей стране, и т. д.
Нашим научным коллективом ученых, биологов, генетиков и врачей было принято решение подойти к практической реализации столь сложной биотехнологической задачи путем разработки и создания авторской инновационной научной теории старения человека и на ее основании создать инновационные решения по увеличению ОПЖ населения России. Было очевидно, что только новое теоретическое и методологическое понимание старой как мир проблемы может обеспечить научный прорыв в проблеме старения и активного долголетия и позволит создать сегодня альтернативные биотехнологии будущего для ранней диагностики, лечения и профилактики болезней цивилизации и разработать биотехнологии активного долголетия. Без новой научной теории нет и не может быть новых технологий и прорывных стратегических решений в современной медицине.
Следует отметить, что по тернистой дороге к столь грандиозной стратегической цели для всего человечества — «активному биологическому долголетию каждого» — нами была «попутно» разработана и создана уникальная теория информационно-коммутационного устройства головного мозга человека, опубликованная в России и США (2014–2015), что в последующем позволило совершить открытие и зарегистрировать новый вид микроволнового излучения головного мозга человека при когнитивной и интеллектуально-мыслительной деятельностив СВЧ-диапазоне от 1 до 5 Ггц. Открытый нами и запатентованный феномен микроволновой активности головного мозга отличается от известной биоэлектрической активности головного мозга, записываемой с помощью ЭЭГ, почти в миллиард раз, или на порядок 109 (Брюховецкий, Брусиловский, 2017, 2018, 2019, 2020; Брусиловский и др., 2019, 2020; Bryukhovetskiy A.S. et al., 2019, 2020).
Следует отметить, что на этом труднодоступном пути к активному долголетию, увеличению продолжительности и улучшению качества жизни человека была создана интеллектуальная собственность в виде целой серии запатентованных инноваций и разработок, не имеющих мировых аналогов: дистанционная мультиволновая радионейроинженерия головного мозга, разработка микроволновой энцефалографии, нейросистема фокусированного ультразвука для биоинженерии, разработка гиперзвуковой нейроинженерии под контролем МРТ, технологии получения двухцепочечных ДНК человека для реставрации поврежденных ГСК, применение лекарственной субстанции «Панаген» для реставрации ГСК.
Однако основным достоинством этой работы стало понимание проблемы долголетия как проблемы возрастзависимой постгеномной болезни собственных СК КМ, и это позволило предложить создание простой и понятной медико-биологической инфраструктуры и системы программных мероприятий по сбору, хранению, сертификации и применению костного мозга человека, не столько в известных трансплантационных целях, сколько в нетрансплантационных, профилактических целях (для реинфузии клеточных систем мононуклеаров КМ с ГСК) без высокодозной химиотерапии для лечения целого ряда БЦ и возрастных изменений органов, тканей пожилого человека. Всю эту систему программных мероприятий и нашего видения медико-биологической сетевой инфраструктуры, предлагаемой для реализации, мы описали в этой книге и представили для вашего обсуждения.
Сама структура монографии достаточно типична. В первой главе книги обсуждаются проблема старения, вопросы средней продолжительности жизни и проблема долголетия человека в разных странах мира. Также в ней иллюстрируются разные аспекты проблемы старения и существующие методологические и теоретические аспекты ее в обществе. Во второй главе анализируются фатальные онкологические, нейродегенеративные и аутоиммунные болезни цивилизации как основная причина смертности населения мира. Дается анализ роли этих заболеваний в структуре общей смертности населения в России и мире. В третьей главе обсуждаются социально-экономические аспекты проблемы старения и фатальных болезней цивилизации. В ней предпринята попытка анализа различных путей увеличения активного долголетия стариков. Четвертая глава монографии посвящена освещению современных научных теорий старения и концепций долголетия человека. Пятая глава монографии посвящена поиску единого системообразующего начала процесса старения. Это самая захватывающая глава книги, т.к. в ней предпринята попытка провести системный анализ существующего теоретического наследия и понять его роль и значение в понимании проблемы в целом. Выводом этой главы стали наши суждения о том, что сегодня мы почти все знаем и понимаем о процессах старения в организме человека и надо попытаться их систематизировать и увидеть системообразующие элементы этого инволюционного процесса, что, на наш взгляд, и было сделано с формированием концепции постгеномных изменений ГСК и других тканеспецифических СК человека и клональности гемопоэза при БЦ и старении.
А в шестой главе монографии мы впервые сформулировали и представили свою авторскую клонально-кроветворную теорию старения и развития фатальных болезней цивилизации. Мы не пытаемся доказать в ней нашим читателям и коллегам, что предложенная нами научная концепция самая правильная и объективная, но мы утверждаем, что ее использование в научно-практических целях позволяет предложить практическую систему программных мероприятий по обороту (сбору, хранению и применению) биоматериала костного мозга населения страны и в дальнейшем реально увеличить продолжительность жизни населения России на 10–15 лет. В седьмой главе книги даны экспериментальное подтверждение, научные факты и механизмы формирования молекулярно-биологических клональных изменений ГСК при старении на модели различных злокачественных опухолей у человека. А в восьмой главе, написанной в соавторстве с д. б. н. Л.Ю. Гривцовой и к. б. н. М.В. Ковиной, представлены научные факты экспериментального подтверждения возможности значительного увеличения продолжительности жизни млекопитающих путем трансфузии ГСК в костно-мозговом кластере мононуклеаров от молодых животных к старым животным, а также продления жизни у старых млекопитающих после реставрации ГСК старого КМ лекарственной субстанцией «Панаген», содержащей двухцепочечные ДНК человека, полученные от здорового донора. Омоложение старых животных костным мозгом молодых животных стало реальностью, и было показано, как приживаются клетки молодого костного мозга в старом костном мозге. Более того, экспериментально было показано, как реставрированные старые ГСК способны восстанавливать иммунопоэз и гемопоэз у старых животных. Впервые было высказано новое понимание реинфузии костно-мозгового кластера СК КМ — не как трансплантации костного мозга или трансплантации ГСК, а как заместительной реставрационной клеточной терапии с целью подавления моно- и олигоклональности гемопоэза и восстановления поликлональности кроветворения как фундаментальной биологической основы долголетия. Технологии ультраранней диагностики биологической старости и фатальных болезней цивилизации были описаны в девятой главе. Соавтором этой главы также стала д. б. н. Л.Ю. Гривцова. Ранее мы уже описывали эту технологию протеомного картирования и профилирования белковых маркеров мембранных белков ГСК при различных БЦ, но посчитали важным еще раз изложить свою точку зрения на ультрараннюю диагностику целого ряда БЦ. Мы впервые определили эти исследования не как протеомику ГСК, а как способ протеомного подтверждения нозоспецифической (нейроспецифической, онкоспецифической, кардиоспецифической и др.) клональности гемопоэза.
Десятая глава книги посвящена изложению перспективных биотехнологических манипуляций по реконструкции и восстановлению молекулярно-биологической структуры гемопоэтической стволовой клетки как фундаментальной научной основе увеличения долголетия человека. В одиннадцатой главе монографии анализируются возможности постгеномной науки как молекулярно-биологической основы управления антистарением и активным долголетием человека, а в двенадцатой главе обсуждаются возможности регенеративной медицины как реальной возможности реставрации поврежденных органов и тканей для антистарения и борьбы с болезнями цивилизации. Роль регенеративной медицины в проблемах долголетия станет центральной, и именно биомедицинские клеточные продукты станут основой увеличения продолжительности жизни. В той же двенадцатой главе представлена наша общая концепция по увеличению продолжительности жизни населения в стране и мире, а в тринадцатой главе презентуются предлагаемые нами государственная политика и стратегия развития бизнеса в области профилактики старения и комплекс глобальных системных и программных мероприятий мирового масштаба по увеличению продолжительности жизни населения в разных странах. В заключении книги мы подводим итоги своей многолетней работы в области антистарения и обобщаем наши собственные исследования.
Хотелось бы поблагодарить соавторов глав и сотрудников АО Клинический госпиталь «НейроВита» за помощь в написании этой книги и в проведении совместных исследований.
По всем возникшим относительно содержания этой книги вопросам просим обращаться непосредственно к авторам по электронной почте: neurovita@mail.ru
Авторы
Глава 1. Проблема старения, долголетия и средней продолжительности жизни человека
Старение человека, как и старение других живых организмов, — это возрастзависимый патобиологический процесс постепенной инволюции, дегенерации, атрофии и деградации морфофункциональных систем жизнеобеспечения, органов, тканей и клеток организма человека, приводящий к неизбежному фатальному (смертельному) исходу, а также имеющий биологические, социально-экономические, психологические и психопатологические последствия. Общая физиология процесса старения человеческого организма аналогична физиологии старения других млекопитающих, но некоторые аспекты этого процесса, например потеря интеллектуально-мнестических и познавательно-умственных (когнитивных) способностей, имеют большее значение для человека, чем для животных. Кроме того, большую ценность приобретают психологические, социальные и экономические эффекты инволюционного процесса старения человеческого организма, а также появление ослабоумливающего компонента в мышлении и сознании человека. В дикой природе животные редко доживают до старости, а вот у различных одомашненных млекопитающих очень наглядно можно проследить схожий процесс старения и сравнить его с аналогичным процессом у человека. Во многом причины смерти домашних животных дублируют причины смерти человека, т.е. животные болеют большинством тех же болезней современной цивилизации, которые являются главными причинами смерти человека.
Для человека разумного (Homo sapience) осознание происходящего с ним процесса старения и непонимание его сущности и сути всегда имели особое значение. Веками философы обсуждали причины старения, писатели и ученые описывали особенности этих процессов у различных людей, алхимики искали эликсир молодости, а многие религии придавали старению священное значение и готовили человека к достойному уходу из жизни. Однако многовековые поиски причин старения до конца ХХ в. не увенчались успехом, и только в последние 2 десятилетия XXI в. были получены первые реальные достижения в этой области знаний на животных. Результаты экспериментов по увеличению средней и максимальной продолжительности жизни модельных животных (у мышей увеличение жизни в 2,5 раза) и простейших организмов (дрожжи — увеличение жизни в 15 раз, нематоды — в 10 раз), а также обнаружение феномена пренебрежимого старения у многих животных (включая людей на стадии «дожития») впечатляют и позволяют надеяться, что успехи современной науки вскоре позволят существенно замедлить или вообще отменить старение (достичь эффекта пренебрежимого старения и для более молодых людей). Тем не менее, несмотря на упомянутые успехи, главной стратегической целью для большинства исследователей проблемы старения была и остается принципиальная возможность как минимум серьезно замедлить старение и как максимум отодвинуть неизбежный фатальный конец. Также важно то, что старение признано основной причиной смертности в развитых странах, а человеческая жизнь провозглашена основной ценностью во многих странах мира. До настоящего времени отдельные гражданские общества и целые государства еще не осознали необходимости фокусировки своих усилий на борьбе со старением, поэтому исследования в этой области недостаточно финансируются государствами и институтами мирового сообщества.
Сегодня успехи медицины и повышение уровня жизни человека позволили значительно увеличить его среднюю продолжительность жизни, хотя изменения максимальной продолжительности жизни пока незначительны. В преимущественном большинстве стран этот процесс привел к постарению населения, где в связи с увеличением доли пожилых людей, которые имеют иные потребности, чем остальное население, в последние годы возникло много социальных и экономических вопросов, связанных со старением. Ведущие мировые ученые в области геронтологии и гериатрии считают, что старение должно быть официально включено в список болезней и болезненных синдромов Всемирной организации здравоохранения, о чем в адрес ВОЗ было направлено коллективное письмо по результатам III Международной конференции «Генетика старения и долголетия», которая проходила в Сочи в апреле 2014 года.
Процесс старения изучает наука геронтология, которая не только исследует физиологические изменения, но и место лиц пожилого возраста в обществе. Цель исследований геронтологии — преодоление возможных недостатков, связанных со старением. Очевидно, что физиологические изменения, которые происходят в теле человека с возрастом, в первую очередь выражаются в снижении биологических функций и способности приспосабливаться к метаболическому стрессу. Эти физиологические изменения обычно сопровождаются психологическими и поведенческими изменениями. Собственно биологические аспекты старения включают не только изменения, вызванные старением, но и ухудшение общего состояния здоровья. Человек в позднем возрасте характеризуется большей уязвимостью для болезней, многие из которых связаны со снижением эффективности иммунной системы. Следовательно, так называемые болезни пожилого возраста являются комбинацией симптомов старения и болезней, против которых организм более не в силах самостоятельно бороться. Например, молодой человек может быстро оправиться от пневмонии, тогда как для человека пожилого она легко может стать смертельной. При старении снижается эффективность работы многих органов (сердце, почки, мозг, легкие и др.) и желез внутренней секреции, формируется возрастзависимая полиорганная и полигландулярная (полисекреторная) недостаточность. Частично это снижение является результатом потери значительной части клеток этих органов и желез внутренней секреции, а также снижения возможностей их восстановления в чрезвычайных случаях и болезнях. Кроме того, клетки пожилого человека не всегда в состоянии выполнять свои функции так же эффективно, как в молодом возрасте. Определенные клеточные ферменты также снижают свою эффективность, т.е. процесс старения протекает на всех уровнях (Москалев, Захаров, 2019).
Как определить хронологический возраст человека, абсолютно понятно: откройте свой паспорт, и вопрос исчерпан. А как определить биологический возраст? Под биологическим возрастом геронтологи понимают реальное состояние изношенности организма. Есть еще понятие психологический возраст, которое отражает свойство личности, его психику, включает познавательные, мотивационные и эмоциональные возможности.
Период геронтогенеза — это поздний период человеческой жизни. В нем принято выделять три фазы: пожилой возраст (для мужчин — 60–74 года, для женщин — 55–74 года); старческий возраст — 75–90 лет; долгожители — 90 лет и старше. В целом данный период характеризуется угасанием основных физических и психических функций.
При упоминании о «пожилых людях», «стариках», «престарелых», «ветеранах» зачастую возникают негативные ассоциации. Дело в том, что наше отношение к старости опосредовано возрастными стереотипами, усвоенными нами с детства. Эти стереотипы поддерживаются культурной традицией, усиливаются средствами массовой информации и социальным окружением. В геронтологической литературе доказано их влияние на то, как пожилые люди воспринимают и ощущают себя и как регулируют свое взаимодействие с окружающими. Распространенное, к сожалению, мнение, что пожилые люди — бесполезные, интеллектуально деградирующие люди, которые не живут полноценной жизнью, а лишь доживают, воздействует на их поведение. Бесспорно, разного рода утраты, нередко сопутствующие пожилому возрасту, такие как потеря работы, смерть близкого человека, ухудшение здоровья, снижение социального статуса, престижа, могут вызвать депрессию: это естественная реакция человека на сильный стресс. Но ведь депрессия бывает и адаптивной: понимание, обретенное в период депрессивной бездеятельности, может в будущем обернуться более эффективными стратегиями взаимодействия с миром. Сегодня все активнее звучат такие термины, как «активное, продуктивное старение». Более того, предлагаются даже средства для снижения биологического возраста (патент РФ RU №2738 644 С2 за 2019).
Демография старения
Главными демографическими эффектами успехов медицины и общего улучшения условий жизни на протяжении последнего столетия являются падение смертности и значительное увеличение продолжительности жизни населения. В дополнение рождаемость в большинстве стран мира снижается, что приводит к так называемому постарению населения, особенно в развитых странах мира.
Возрастной состав населения обычно изображается в виде возрастно-половых пирамид, на которых доля населения в каждом возрасте изображается в зависимости от возраста. На таких пирамидах старение населения выглядит как рост доли пожилых людей вверху пирамиды за счет молодых внизу. Процесс старения, таким образом, может быть двух типов: «старение снизу», или уменьшение рождаемости, и «старение сверху», или увеличение средней продолжительности жизни. В большинстве стран мира «старение снизу» является наибольшим из двух факторов, а в постсоветских странах, включая Украину, — единственным. Например, на Украине старение населения частично компенсируется падением продолжительности жизни (с 71 года в 1989 до 68 лет в 2005), как в связи с ухудшением медицинского обслуживания и увеличением социального неравенства, так и в связи с распространением эпидемии СПИДа. В целом в мире, согласно данным ООН, доля населения старше 60 лет составляла 8% в 1950 г., 10% в 2000 г. и ожидается на уровне 21% в 2050 году.
Старение населения оказывает значительное влияние на общество. Пожилые люди чаще предпочитают сберегать деньги вместо того, чтобы тратить их на товары широкого потребления. Это приводит к значительному дефляционному давлению на экономику. Некоторые экономисты, особенно японские, видят в этом процессе преимущества — в частности, возможность внедрения автоматизации производства без угрозы увеличения безработицы и решения проблемы перенаселения. Тем не менее негативный эффект проявляется в системе социального обеспечения и пенсий, которая во многих странах, преимущественно в Европе, финансируется за счет налогов с постоянно уменьшающейся работающей части населения. Кроме того, значительное влияние оказывается и на образование, что проявляется как в снижении государственных расходов, так и в ухудшении общего уровня грамотности в связи с пониженной способностью стареющего населения приспосабливаться к возрастающим стандартам. Таким образом, контроль старения населения и адаптация общества к новым условиям являются важнейшими задачами демографической политики.
Проблема долголетия — одна из самых фундаментальных проблем мировой науки и всемирного здравоохранения, которая негласно поднимает проблемы мировой демографии, экологии, мировой экономики и климата, социальные и медицинские аспекты здоровья населения в мире и проблемы здоровья и выживания различных наций и народностей в различных регионах земного шара. Глобальные аспекты выживания человечества в условиях неблагоприятной экологии Земли, разрушения основ самой жизни человека загрязнением акватории мирового океана, замусоривания земельных угодий отходами повсеместной «экономики дымных труб», загрязнения массивных территорий Земли радиоактивными отходами и глобального потепления привели к катастрофическим последствиям всемирного масштаба, и сегодня эти факторы резко сокращают продолжительность жизни населения планеты и угрожают основам самой человеческой цивилизации. Основными причинами смертности населения в мире до ХХI в. были эпидемии инфекционных заболеваний, мировые войны и младенческая смертность, а основными причинами смертности населения в мире в конце ХХ и нач. ХХI в. являются локальные военные конфликты, старость и фатальные заболевания цивилизации. Однако роль эпидемий в смертности населения и сегодня достаточно актуальна. Иллюстрацией этого феномена может быть глобальная пандемия коронавирусной инфекции COVID-19, которая уже унесла миллионы жизней людей по всему миру и даже к концу 2023 г. так и не прекращена.
Важным показателем в оценке демографической ситуации является средняя продолжительность жизни населения в различных странах мира. Для вычисления СПЖ используются формулы из теории вероятности и данные о смертности различных возрастных групп за год. Качество жизни и долголетие человека напрямую зависят от условий проживания, изменений климата и экологической обстановки в зоне проживания, от состояния здоровья, а также от уровня заботы и лечения в случае заболеваний. Современная медицина за последние 50 лет совершила качественный скачок. Так, продолжительность жизни в странах мира в 2019 г. стала существенно выше, чем в нач. и сер. ХХ в. Если родившиеся в 1900 г. в среднем доживали до 48–50 лет, то сейчас этот показатель по миру приближается к 70 годам.
Считается, что увеличение СПЖ связано с иммунизацией населения от инфекционных заболеваний и профилактики эпидемий особо опасных инфекций, а также с уменьшением младенческой смертности и тем, что иммунизацией в развитых странах занимаются на государственном уровне. В мировом рейтинге Япония занимает по СПЖ ведущее положение, т.к. он составляет 82,75 года (мужчины — 82,4, а женщины — 85,1 года). Однако в 2020–2021 гг. из-за пандемии коронавирусной инфекции число людей старше 65 лет, умерших от COVID-19, в мире превысило смертность во все предыдущие годы в 2 раза. Особенно наглядно это видно по статистическим показателям ежегодной избыточной смертности в США, Бельгии и Италии.
Средняя продолжительность жизни в России по регионам
Средняя продолжительность жизни в России на 2017 г. составляет 72 года и сильно различается от региона к региону, а разница составляет 16 лет. Есть регионы, перешагнувшие порог в 80 лет (в т. ч. Ингушетия; вплотную к этому порогу подошел г. Москва); 10 регионов смогли преодолеть порог в 75 лет. Более 20 субъектов РФ оказываются ниже значения в 70 лет. Ученые установили, что средний возраст старения, к которому у человека появляется сразу несколько старческих болезней, — это 65 лет. Однако этот средний возраст наступает в разных странах мира в различном возрасте. Например, жители Японии, Швейцарии, Франции и Сингапура начинают ощущать себя на 65 лет примерно в 76 лет, а жители Афганистана — в 51 год. Раньше всего старческие болезни проявляются у жителей Папуа — Новой Гвинеи — в 45 лет. Россия оказалась на 160-м месте в этом рейтинге. Россияне стареют быстрее, учитывая средний мировой показатель. Старческие болезни настигают жителей России уже в 59 лет (Берк, 2019).
В списке стран, занимающих лидирующее положение по СПЖ, стоят Франция, Италия, Испания, а в арьергарде — африканские государства, раздираемые военными конфликтами, где население проживает за чертой бедности (Ангола, Замбия и др.), где средняя продолжительность жизни 40 лет. СПЖ в России в 2019 г. составляла 72,4 года (65 лет для мужчин и 80 лет для женщин).
Может ли теоретически среднестатистический человек мира жить больше 100 лет? Мы уже пытались рассуждать на об этом во введении. А сейчас мы более детально поговорим на эту тему. Обратимся к родословной первого человека на Земле, Адама. В Ветхом Завете черным по белому записано: «Всех же дней жизни Адамовой было девятьсот тридцать лет; и он умер». Сын Адама Сиф прожил 912 лет. Внук Енос — 905. Правнук Каинан — 910. Праправнук Малелеил — 895. Прапраправнук Иаред — 962. Следующий потомок, Енох, — 365. Мафусаил и вовсе 969! Рекордсмен-долгожитель планеты, не зря есть выражение «мафусаилов век». Ламех — 777. Ной — 950. Путем несложного сложения, деления выясняем: средняя продолжительность жизни патриархов девяти допотопных поколений составляла 912 лет (десятый, Енох, не в счет: он в 365 лет был взят живым на небо. Зато успел породить самого Мафусаила!). Математическое моделирование процессов регенерации показало, что время жизни нейрона как одной из самых необновляемых клеток организма млекопитающих генетически запрограммировано более чем на тысячу лет (Галушкин, 2012). Все другие клеточные системы имеют ограниченный срок жизни и должны регулярно обновляться (лейкоцит живет 100—120 дней, эритроцит — 80—90 дней и т.д.), и поэтому в хороших условиях экологии, при хорошем питании и заботе о здоровье, при сохранности систем регуляции и надзора (иммунной системы) человек может даже сегодня прожить 120 лет.
Проект «Геном человека» ответил на главный вопрос проблемы долголетия: продолжительность жизни человека не ограничена временем жизни генома (геном нервной клетки способен жить не менее 200 лет), а обусловлена преимущественно не геномными, но постгеномными (эпигенетическими, транскриптомными, протеомными, метаболомными и секретомными) нарушениями в соматических клетках или в клетках микроокружения этих клеток. Окружающая среда, климат и неблагоприятные факторы социального микроокружения нарушают эпигенетические характеристики клетки и приводят к постгеномным накоплениям патоспецифических белков, РНК и других белковых тел, не имеющих реальных механизмов регуляции в организме человека.
По-видимому, постгеномные нарушения в специализированных высокодифференцированных клетках основных регуляторных и самообновляющихся управляющих систем и систем саморегенерации являются фундаментальной причиной старения и формирования фатальных болезней цивилизации и системной дегенерации и атрофии органов и тканей. Поэтому, возможно, именно постгеномная медицина может решить большинство проблем увеличения продолжительности жизни человека и борьбы с основными фатальными болезнями цивилизации!!! Таким образом, с позиций современной науки и реальных научных фактов среднестатистический человек мира может жить больше 150 лет! Давайте в этой книге попытаемся вместе подумать и понять, что нужно сделать для того, чтобы наши желания стали реальностью.
Глава 2. Фатальные болезни цивилизации как основная причина смертности населения мира
На сегодняшний день в мировом здравоохранении выделяют три основные группы заболеваний, нехарактерных для человека как биологического вида: болезни цивилизации; социально значимые заболевания; социально обусловленные заболевания. Этими болезнями на протяжении 6 млрд лет наши предки не страдали, а появились они в основном всего лишь 100–150 лет назад. Болезни цивилизации — это заболевания, распространенные в экономически развитых странах, происхождение их связано с неблагоприятным воздействием на человека негативных последствий ряда достижений научно-технического прогресса и загрязнения окружающей среды, приведших к глобальным изменениям климата. Под болезнями цивилизации ряд исследователей также в настоящее время понимает заболевания человека, связанные с духовным неблагополучием, нарушением морально-нравственных норм и механизмов адаптации к неблагоприятным факторам антропогенно измененной среды в условиях стремительного роста научно-технического прогресса (Агаджанян и др., 2003). К ним относятся болезни сердечно-сосудистой системы (ССС) (ишемическая болезнь сердца, атеросклероз, гипертония, инфаркты, инсульты), являющиеся главными причинами смерти населения в мире, рак и другие злокачественные новообразования, аутоиммунные заболевания (рассеянный склероз, ревматоидный артрит, аутоиммунный тиреоидит, сахарный диабет I типа и др.), все виды аллергии, дегенеративные заболевания органов и тканей (нейродегенеративные болезни, остеохондроз позвоночника, дегенерации костей и суставов), болезни нарушения обмена (ожирение, анорексия невроза, сахарный диабет I и II типов и т.д.) и др., речь о которых пойдет позже. Социально значимые заболевания являются основными причинами заболеваемости, инвалидности и смертности, особенно среди трудоспособной части населения развитых стран. Эти болезни наносят серьезный экономический ущерб либо в силу выбывания производителей материальных благ из производственной цепочки, если они погибают из-за болезни, либо в силу бремени выплат им социальных пособий, если они становятся инвалидами. К социально значимым заболеваниям также относятся болезни системы кровообращения, злокачественные новообразования, травмы, отравления и некоторые другие последствия воздействия внешних причин, сахарный диабет, туберкулез. То есть они очень перекликаются с БЦ по нозологическим формам, но различаются по своей негативной роли на социум и гражданское общество. Социально обусловленные заболевания формируются под воздействием ближайшего окружения человека и связаны с социально-экономическим состоянием страны проживания. К этой группе относятся болезни наркологического профиля, венерические болезни, туберкулез, вирусный гепатит В и др. Поскольку социально обусловленные заболевания распространены в одних и тех же группах населения, они часто ассоциируют (сочетаются) друг с другом, что усугубляет течение и затрудняет лечение каждой из них. Так, по данным ВОЗ, более 3 млн чел. являются одновременно инфицированными возбудителями туберкулеза и ВИЧ. Более 90% ВИЧ-инфицированных — наркоманы. Среди заболевших инфекциями, передающиеся половым путем (ИППП), ок. 70% злоупотребляют алкоголем, 14% страдают хроническим алкоголизмом либо наркоманией. Если в 1991 г. из 531 тыс. больных венерическими заболеваниями было выявлено 12 ВИЧ-инфицированных (2,3 на 100 тыс.), то в 1999 г. из 1739,9 тыс. больных с ИППП 822 чел. были с ВИЧ-инфекцией (47,2 на 100 тыс.). Смертность от болезней цивилизации неестественна для человека как для биологического вида, ее можно избежать, ведя здоровый образ жизни (ЗОЖ), поэтому она называется предотвратимой. Смертность от болезней ССС и рака можно и нужно успешно снижать путем раннего их выявления и адекватной диагностики при профилактических осмотрах. Как раз на решение этой проблемы направлена диспансеризация трудоспособного населения России, проводимая в рамках Национального проекта «Здоровье». Предотвращение смертности от алкоголизма и наркомании должно происходить через профилактику поведенческих факторов риска, путем формирования ЗОЖ у населения, а особенно у детей и подростков, разработки мер антиалкогольной политики. Таким образом, при ведении ЗОЖ современный человек имеет все возможности избежать вышеперечисленных заболеваний и оставаться здоровым и активным на долгие годы.
К группе болезней цивилизации относят патологии сердечно-сосудистой, нервной, иммунной, пищеварительной, эндокринной систем. Из них сердечно-сосудистые, онкологические, нейродегенеративные болезни и сахарный диабет прочно заняли ведущие места среди причин смертности, инвалидности и временной нетрудоспособности населения в мире.
Существует множество теорий обусловленности здоровья человека. Одной из самых распространенных среди них является именно теория болезней цивилизации и социальной дезадаптации. Еще в 50-х гг. XX в. её представили французские медики Э. Гюан и А. Дюссер в книге «Болезни нашего общества». Теория представляет собой ответ на вопрос о причинах резких изменений общественного здоровья, особенно сокращения его потенциала и возникновения массовой патологии. Патология (от греч. раthos + logia — «переживание, страдание, болезнь» + «учение, наука») — болезненное проявление, не норма для организма. Б. Н. Чумаков иллюстрирует понятие «болезни цивилизации» следующими фактами. Интересен результат вскрытия во время корейских событий в 1950-е гг. более 300 погибших солдат американской армии, возраст которых равнялся 22 годам, не имевших признаков атеросклероза. При жизни они считались абсолютно здоровыми. При патологоанатомическом вскрытии у 75% из них коронарные сосуды были поражены атеросклеротическими бляшками. У каждого четвертого просвет артерий оказался суженным на 20%, а у каждого десятого — на 50%. Такую картину можно наблюдать у жителей стран с высоким жизненно-экономическим потенциалом. А вот как выглядит ситуация в менее цивилизованных странах. Итальянский врач Липичирелла при обследовании 203 погонщиков верблюдов в 1962 г. в Сомали не обнаружил ни у одного из них признаков атеросклероза. При вскрытии 6,5 тыс. умерших местных жителей в Уганде не было выявлено ни одного случая коронарного атеросклероза или инфаркта миокарда. При обследовании 776 негров в Западной Африке с помощью ЭКГ лишь в 0,7% случаев наблюдались незначительные отклонения со стороны сердечно-сосудистой системы. Г. Л. Апанасенко считает, что развитие многих соматических заболеваний связано с негативным воздействием некоторых социально-гигиенических факторов. Так, у людей в возрасте 35—64 лет риск развития ишемической болезни сердца (ИБС) увеличивается при ожирении в 3,4 раза, при гиподинамии — в 4,4 раза, при высоком уровне холестерина крови — в 5,5 раза, при повышенном уровне артериального давления — в 6 раз, а при курении — в 6,5 раза. При объединении нескольких неблагоприятных социально-гигиенических факторов вероятность развития заболевания увеличивается в разы. Лица, у которых отсутствуют признаки заболеваний, но выявлены перечисленные факторы риска, формально относятся к группе здоровых, но у них возможность развития ИБС в ближайшие 5–10 лет весьма вероятна. Факторы риска — общее название факторов внешней и внутренней среды организма, поведенческих привычек, не являющихся непосредственной причиной определенной болезни, но способствующих увеличению вероятности ее возникновения и развития, ее прогрессированию и неблагоприятному исходу.
Заболевания цивилизации связывают с результатом развития индустриального общества — «экономикой дымных труб», информатизацией, социальными изменениями, радиационной ситуацией на планете, лечением лекарственными препаратами, а также с порочными наклонностями. Это основная причина ухудшения здоровья населения всей планеты. Первопричина всех болезней цивилизации лежит в дисбалансе отношений человека с природой. Болезни цивилизации угрожают основам жизни людей во всем мире и ведут к самоуничтожению человечества!
Что же заставляет выделять эти заболевания в отдельную группу? С нач. XX столетия уровень заболеваемости болезнями цивилизации стал расти в геометрической прогрессии. Сегодня мы очень много знаем об этих болезнях цивилизации, но абсолютно не можем своевременно диагностировать, а также эффективно лечить данные заболевания!
Среди бесспорных факторов риска БЦ наиболее существенными и распространенными являются следующие: гипокинезия и гиподинамия; переедание и связанная с ним избыточная масса тела; постоянное психоэмоциональное напряжение, неумение отключаться и правильно отдыхать; злоупотребление алкоголем и табакокурение. Гипокинезия (от греч. hypokinesia — «недостаточность движения») — ограничение количества и объема движений, обусловленное образом жизни, особенностями профессиональной деятельности, постельным режимом в период заболевания и сопровождающееся в ряде случаев гиподинамией. Гиподинамия (от греч. hypodynamia — «недостаточность силы») — уменьшение мышечных усилий, затрачиваемых на удержание позы, перемещение тела в пространстве, физическую работу. Она возникает при иммобилизации, пребывании в замкнутых помещениях малого объема, малоподвижном образе жизни. Эти две категории характеризуют малоподвижный образ жизни современного человека, связанный с вхождением в нее водопровода и централизованного отопления, широкого использования автомобилей, стиральных и посудомоечных машин, электрических плит, лифтов и т. д. Все эти механизмы облегчают наш быт, делают жизнь приятной и беззаботной с одной стороны, а с другой — приводят наши мышцы и сосуды в дряхлое состояние. В переедании современного человека виноват его непомерно большой, доставшийся от диких предков желудок. Вспомните, как добывал себе пищу первобытный человек. Сначала он без экскаватора и даже без лопаты должен был выкопать целый котлован, чтобы загнать туда мамонта, потом с диким криком бегать, устрашать и загонять туда мамонта. А какого размера должен был быть камень, чтобы этого мамонта им убить? А как вытащить такое большое животное из котлована без подъемного крана? А как потом снять с него шкуру без ножа и разделать без топора и пилы? И только тут начинался момент поедания пищи. А вокруг — гиены и грифы, которые уже ждали остатков от пиршества человека. Сложить пищу про запас было некуда — холодильников и морозильных камер в каменном веке не существовало. Так длилось миллионы лет, и выживал только тот, у кого желудок был больше, кто мог одномоментно набить туда большое количество пищи, ведь новый случай отобедать мясом мамонта мог представиться только через 1–2 недели. Сейчас человек добывает пищу легким движением руки, открывая дверь бытового холодильника несколько раз в день или 2—3 раза в день посещая учреждения общепита. Его желудок при приеме больших количеств еды не растягивается, как воздушный шар, а просто набивается до предела. Постоянное переедание приводит к увеличению массы тела — ожирению, а ожирение — к болезням ССС. Кроме того, современный человек ушел от гармонии с природой, он уже не ложится спать с заходом солнца и не просыпается, когда его первые лучи проникают в пещеру, и т. д. Пробуждение от звонка будильника уже нефизиологично и вызывает стресс, и так каждый день на протяжении многих лет. А неуверенность в завтрашнем дне, бесконечные революции, войны, пандемии инфекционных и вирусных заболеваний, перестройки и экономические кризисы? Все это привело к тому, что человек в наше время, по мнению ученых, находится в состоянии хронического стресса, и горе тому, кто не умеет с этим стрессом бороться. Из всего вышеперечисленного можно сделать вывод, что болезни цивилизации, к которым относятся в первую очередь болезни сердца и сосудов, онкологические и аллергические, аутоиммунные болезни, формируются из-за невозможности человеческого организма адаптироваться к стремительным изменениям окружающей среды, нарушениям ритма и образа жизни, которые происходят под воздействием техногенной модернизации условий жизни, достижений научно-технического прогресса, развития цивилизации.
Прогнозы увеличения некоторых фатальных заболеваний цивилизации на ближайшие 20–30 лет выглядят очень пессимистичными.
Рак и другие злокачественные новообразования. В настоящее время в мире раковых больных 15,12 млн чел. Согласно последнему отчету ВОЗ, к 2030 г. количество новых случаев заболевания раком возрастет примерно на 70%, достигнув цифры 21,6 млн больных в год (http//worldofoncology.com/materialy/o-rake/statistika/). Считается, что в 2050 г. их количество достигнет почти 40 млн чел. (Каприн, 2020). Рост числа онкологических заболеваний в мире становится главным драйвером увеличения смертности населения на земном шаре и отчетливым маркером усугубляющегося год от года неблагополучия окружающей среды и изменения климата во всем мире.
Нейродегенеративные болезни (НДБ). Резкое постарение населения в США и Европе привело к увеличению количества больных со слабоумием и болезнью Альцгеймера, число которых может вскоре утроиться — от 4,7 млн в 2012 г. до 13,8 млн к 2050 г. К 2050 г. каждый из 85 чел. во всем мире будет страдать болезнью Альцгеймера (Институт здорового старения, США, 2012). Каждый третий житель земли страдает нервно-психическими заболеваниями. В геометрической прогрессии нарастает количество людей с тяжелыми органическими заболеваниями мозга, а в арифметической прогрессии растет количество самоубийств и социопатов с расстройствами личности. Успехи современной нейрореанимации и нейрохирургии привели к увеличению в мире количества глубоких инвалидов, находящихся в вегетативном состоянии, с массивными поражениями мозговой ткани и интеллектуальным дефектом.
Аутоиммунные заболевания (АИЗ). Аналогичная ситуация сложилась с целым рядом АИЗ. Количество больных системной красной волчанкой (СКВ), ревматоидным артритом, рассеянным склерозом (РС) и другими аутоиммунными заболеваниями вырастет за ближайшие 20 лет на 37%, а количество больных с аутоиммунным сахарным диабетом превысит 0,5 млрд чел. в 2040 г. (Отчет ВОЗ, 2019). Смертность от этих тяжелых заболеваний цивилизации продолжает неуклонно возрастать, и противопоставить этим фактам просто нечего. Поэтому поиск любого способа лечения и терапевтического средства, способного хотя бы незначительно повысить эффективность терапии этих фатальных заболеваний цивилизации и снизить смертность от них, приобретает крайнюю актуальность и значимость для всей мировой медицины.
Существует ряд объективных обстоятельств, в связи с которыми БЦ стали одними из главных причин смертности населения в мире. Их можно определить следующим образом:
1. Причины и патогенез возникновения большинства фатальных БЦ окончательно не ясны.
2. Существует проблема поздней диагностики фатальных заболеваний цивилизации: не обнаружено объективных клинических, морфологических, биофизических, иммунохимических, генетических и постгеномных молекулярно-биологических маркеров этих смертельных болезней, и при большинстве заболеваний в принципе отсутствует ранняя диагностика.
3. Заболевания текут асимптомно, и их диагностируют только тогда, когда большая часть специализированных дифференцированных клеток организма человека уже погибла и не может быть восстановлена. Например, при боковом амиотрофическом склерозе или болезни моторного нейрона заболевание диагностируют клинически и нейрофизиологически только тогда, когда погибло более 70—80% мотонейронов головного и спинного мозга человека, а при большинстве онкологических заболеваний клинические проявления болезни появляются преимущественно на III–IV стадиях неопластического процесса и, как правило, при генерализованном процессе и наличии большого количества метастазов в органах и тканях.
4. Существующее лечение неэффективно и практически не изменяет медианы выживаемости больных: например, при мультиформной глиобластоме, несмотря на все виды современного лечения, медиана выживаемости составляет 12–15 мес. последние 100 лет. При БАС медиана выживаемости 24–36 мес., а диагноз данного нейродегенеративного заболевания, как мы уже знаем, устанавливается только тогда, когда погибло более 70–80% двигательных нейронов. Аналогичная ситуация и с болезнью Альцгеймера, заболеваемость которой за последние десятилетия стремительно увеличилась среди населения экономически развитых стран.
К сожалению, до настоящего времени так и не разработано эффективных технологий лечения большинства онкологических, аутоиммунных, нейродегенеративных, эндокринологических, сердечно-сосудистых болезней цивилизации. Причиной этого является непонимание фундаментальных молекулярно-биологических механизмов болезней цивилизации, хотя этиология и патогенез этих заболеваний представляются достаточно ясными и понятными. Но если бы мы достаточно хорошо понимали глубинную сущность этой проблемы, то решение уже давно было бы найдено. Но его пока не существует. Мы стали заложниками собственных научных догм и консервативных представлений и не можем вырваться из плена собственных заблуждений относительно БЦ.
Более 20 лет мы занимаемся лечением крайне сложных неврологических и онкологических БЦ, а также последствий тяжелых нейротравм головного и спинного мозга у больных, где традиционная конвенциональная медицина уже расписалась в своем бессилии и эти пациенты признаны паллиативными и некурабельными. В большинстве случаев эти пациенты уже давно выписаны из стационаров и никакой существенной помощи, кроме различных вариантов ухода и реабилитационных пособий, приходящими к ним на дом врачами им не оказывается. Во всем мире существующий подход классической медицины к лечению диагностически сложных и терапевтически резистентных неврологических и онкологических пациентов регламентируют единые стандарты диагностики и лечения этих болезней. Очевидно, что действующие стандарты лечения и клинические рекомендации как за рубежом, так и в нашей стране написаны ведущими и главными специалистами своих областей медицины (онкологии, неврологии, иммунологии, эндокринологии и др.) и базируются на абсолютно проверенных годами методах и способах фармакологической коррекции болезни, отработанных способах хирургического пособия, проверенных противоопухолевых способах химиотерапии, лучевой терапии и реабилитационного лечения. Все другое в программы стандартов лечения не входит по определению. Нам объясняют, что стандарты лечения и клинические рекомендации защищают интересы больного и позволяют в большинстве случаев обеспечить адекватную терапию каждому пациенту с БЦ. Но на самом деле стандарты унифицируют и нивелируют индивидуальность болезни каждого пациента и стоят не столько на стороне больного, сколько на стороне оптимизации и экономии расходов государства, финансирующего их через фонды ОМС. Стандарты лечения «пытаются» найти золотую середину и баланс между эффективностью, затратностью лечения для бюджета и прогнозируемым результатом терапии. Наверное, с государственных позиций это достаточно верно, когда руководящие медицинские документы стандартизируют и оптимизируют расходы государства на содержание и терапию этих малокурабельных пациентов. Но это не значит, что таким больным не могут быть предложены за собственные деньги новые биотехнологические терапевтические решения персонализированной медицины (геномики, транскриптомики, метаболомики, протеомики, генной инженерии, биоинженерии, тканевой инженерии и др.), которые не вписаны в существующие стандарты высокотехнологичного лечения, т.к. еще не завершился весь цикл их государственной легализации для оплаты через фонд ОМС.
То есть, с одной стороны, при целом ряде болезней цивилизации уже разработаны, созданы и существуют реальные технологии лечения неизлечимых заболеваний, которые позиционируются классической конвенциональной медициной с ее стандартами и клиническими рекомендациями как паллиативные и бесперспективные, а персонализированной медициной эти заболевания рассматриваются как основные кандидаты на оказание эффективной помощи с применением персонализированных ОМИК-технологий. И в этом нет парадокса и несоответствия. Просто биотехнологические платформы реализации этих научно-методологических подходов принципиально различны и обусловлены разными целями и мишенями терапии этих патологий.
Для примера: многие годы (более 20 лет) мы для нейрорегенерации поврежденного головного и спинного мозга используем собственные ГСК с достаточно высокой эффективностью (эффективность реабилитации повышается до 60%). Однако в последние годы мы выявили, что ГСК пациента имеют более значимую диагностическую ценность, чем даже мы могли себе представить. Оказалось, что по протеомным профилям картирования и профилирования экспрессии белковых маркеров мембранной поверхности ГСК можно выявить возникновение злокачественного новообразования в организме или системного нейродегенеративного или аутоиммунного заболевания, когда еще нет манифестации и клинических признаков болезни. Мы запатентовали эту технологию в России и стали номинантами Премии департамента здравоохранения г. Москвы, представив эту технологию на столь престижный конкурс. Но она тоже не оплачивается ОМС, хотя в десятки раз эффективнее в ранней диагностике рака по сравнению, например, с диагностическими возможностями онкомаркеров. Известно, что онкомаркеры появляются тогда, когда опухоль уже получила «прописку» в тканях конкретного органа, начала распадаться, и ее молекулы стали циркулировать в биологических жидкостях. Но при выраженном злокачественном процессе это уже может быть очень поздно, и весь организм пациента будет «осеменен» метастазами этого рака.
Последняя инновация в нашей работе заключается в том, что оказалось, что большинство иммунноассоциированных онкологических, аутоиммунных, нейродегенеративных, сердечно-сосудистых и наследственных болезней цивилизации осложнены клональным кроветворением (гемопоэзом) и, как правило, именно клональный гемопоэз является в 40–50% случаев причиной внезапной смерти этих пациентов, причиной повторных инсультов и инфарктов у сосудистых больных и главной причиной прогрессирования нейродегенеративных заболеваний. Нам удалось, используя генетические технологии секвенирования полного экзома 22 тыс. генов и протеомные технологии исследования ГСК этих пациентов, найти генетические признаки мутаций генов клональности и протеомные профили патологических клонов ГСК, что впервые в мире позволило диагностировать клональный гемопоэз у больных с болезнью Альцгеймера, болезнью Паркинсона, болезнью Пика, боковым амиотрофическим склерозом, системной корковой атрофией, системной нейродегенерацией мозга, хронической воспалительной полинейропатией. Это открытие впервые было подтверждено на уровне геномных и постгеномных исследований собственной ГСК и сегодня не вызывает сомнений.
Мы разработали технологию реституции, или восстановления статус кво (состояния до болезни), костного мозга, что позволяет манипулировать и управлять клонами ГСК в костном мозге человека, блокировать доминирующие патологические клоны ГСК и активировать ингибированные ранее здоровые клоны ГСК. Биоуправление клональностью гемопоэза не является чем-то ультраординарным, но до того эти манипуляции можно было реализовать только путем трансплантации костного мозга (ТКМ) или геномного редактирования (ГР). Наши технологии позволяют осуществлять перезапуск иммунной системы без риска смертельного отторжения пересаженного трансплантата костного мозга или возникновения смертельных осложнений от ТКМ или ГР.
Мы впервые стали брать на лечение больных с прогрессирующими наследственными заболеваниями и понимаем, что́ мы можем сделать, чтобы остановить прогрессирование наследственной болезни. Подчеркнем: не вылечить болезнь, а остановить ее прогрессирование и смертельный исход. Оказалось, что технология реституции костного мозга и управления врожденным иммунитетом может стать инструментом для предотвращения прогрессирования и рецидивов злокачественных опухолей. Для этого нужно только стандартными методами противоопухолевого циторедуктивного (хирургического), цитостатического (химиотерапия) и цитотоксического (лучевая терапия) лечения добиться минимальной остаточной опухолевой болезни, и это позволяет путем реституции костного мозга добиться восстановления молекулярно-клеточного состава костного мозга, способного остановить злокачественный опухолевый рост и прогрессирование смертельной болезни.
Таким образом, фатальные БЦ — это хорошо известный и уже состоявшийся научный факт и социальный бич нашей цивилизации, особенно наших городов и крупных мегаполисов. Именно они стали основной причиной смертности населения планеты в конце XX и нач. XXI в. Понимание фундаментальных причин возникновения этих смертельных неинфекционных заболеваний должно стать базовой основой выживания всего человечества. Эти болезни забрали пальму первенства причин смерти у инфекционных заболеваний, эпидемии которых «косили» население планеты в прошлых веках. По-видимому, когда мы научимся рано их диагностировать и эффективно лечить, придут другие заболевания второго столетия жизни человека, и уже в середине этого века они станут вызовом для медицинского сообщества нашей Земли. Ну а пока это произойдет, мы попытаемся разобраться с болезнями цивилизации и системообразующими факторами их возникновения и развития.
Глава 3. Социально-экономические аспекты старения и фатальных болезней цивилизации
Если посмотреть списки мировых рекордсменов долголетия, предложенные Википедией, то в них перечислены 100 самых долгоживущих жителей планеты, чей доказанный возраст на момент ухода из жизни перевалил за 114 лет. Перечни более «юных», в 100 лет и старше, гораздо длиннее. И тут мы встречаемся с определенными загадками и противоречиями. Если где-то наслаждаться годами помогают достойные условия жизни, т.е. социальный аспект старения помогает прожить дольше, то как объяснить феномен Мэгги Паулин Барнс, прожившей 115 лет 319 дней (с 1882 по 1998)? Это действительно уникум: она единственный представитель долгожителей мира, родившихся в рабстве; т.е. социальные условия никак не позволяли ей прожить очень долго. В упомянутых списках и примерах из Книги рекордов Гиннеса упоминаются и имена американок Бесси Купер, Элизабет Болден, японки Танэ Икаи, представительницы Эквадора Марии Каповилья и десятков других чемпионов, перешагнувших рубеж 116-летней продолжительности жизни. А Саре Кнаусс на момент ухода из жизни было более 119 лет (она из США). Танэ Икаи рассказывала, что ее успех связан с любовью к дарам моря, именно их она всегда предпочитала в питании. А вот канадка Мария Луиза Мейлер благополучно достигла возраста 117 лет и 230 дней, но всю жизнь трудилась не покладая рук, причем в тяжелых условиях. Два мужа, 10 детей. К тому же Мария не отказывалась от бокальчика-другого вина, а курить бросила лишь к 90-летию. Мужчин в этой славной когорте немного. В категории «долгожители мира» Книги рекордов Гиннеса зафиксировано имя японца, прожившего чуть более 116 лет, это Дзироэмон Кимура. Сто пятнадцать лет и 252 дня радовался жизни Кристиан Мортенсен — датчанин, эмигрировавший в США. Пуэрториканец Эмилиано Меркадо дель Торо тоже в числе рекордсменов с итогом 115 лет и 163 дня. Есть несколько более младших чемпионов долгожительства.
Долгие годы список долгожителей в мире возглавляла Жанна-Луиза Кальман с феноменальным результатом 122 года и 164 дня (1875–1997). Только представьте: она могла видеть первый полет братьев Райт, пережила две мировые войны и кучу других знаковых событий мировой истории! Всю свою жизнь она прожила в крайне неблагоприятных условиях. Ее рецептом успеха является постоянная физическая активность. Велосипед, причем не прогулочный; она была почти профессионалом в гонках! А в 85-летнем возрасте научилась прилично фехтовать. До последних дней была в памяти и ясном уме, отличалась отменным чувством юмора. И вкусом к хорошей одежде! Луиза Кальман объясняла свой рекорд умением следовать простому правилу: «Когда невозможно решить проблемы, нет нужды беспокоиться». Кстати, неистовая француженка питалась совсем не нектаром и амброзией. Она отказала себе в удовольствии выпивать каждый день по стаканчику портвейна только в 117 лет! Один невезучий нотариус решил «облагодетельствовать» 92-летнюю Жанну-Луизу, взявшись платить ей пожизненную ренту. Она прожила еще 30 лет, надолго пережив нотариуса, что так и не дождался ее скромной квартирки. Другой парадокс долголетия — это Антиса Хвичава, являющаяся образцом трудолюбия. Антиса Хвичава, обычная грузинская женщина, немного не дожившая до рубежа в 133 года, в течение 85 лет трудилась на чайных плантациях. Существуют документы, подтверждающие подлинность факта ее рождения в 1880 г.; это признали специалисты Книги рекордов Гиннеса, выдавшие грузинке соответствующий сертификат. Антиса Хвичава была неграмотной, так что об истоках своей уникальности ничего не бралась рассказывать многочисленным гостям, зато интересовалась новинками науки, хотела научиться пользованию компьютером. Живость ума и природная любознательность оставались при ней до последнего вздоха.
Профессор анатомии Калифорнийского университета Леонард Хейфлик обнаружил интересную закономерность: продолжительность жизни человека и отношение веса мозга к весу тела связаны пропорционально. Чем больше это частное, тем длиннее жизнь. По его мнению, старение начинается тогда, когда мы прекращаем расти. По сути, лет с тридцати, а то и раньше. А вот акулы, галапагосские черепахи и ряд других существ стареют весьма медленно, поскольку практически всю жизнь чуть-чуть, но прирастают в размерах. Так, например, было доказано, что гренландская акула живет 400 лет и все эти годы она прирастает в длине и объеме.
Идею американского профессора Л. Хейфлика о взаимосвязи продолжительности жизни человека и размеров его мозга поддерживает и развивает соавтор этой монографии к. б. н. М.А. Шурдов. Он сформулировал свою собственную концепцию долголетия, которая отражает прямую зависимость продолжительности жизни от степени изношенности и объема молекулярно-биологических повреждений нервной ткани собственного мозга человека. То есть он видит взаимосвязь не столько массы и объема головного мозга (ГМ) и продолжительности жизни, как Л. Хейфлик, а преимущественно между продолжительностью жизни и объёмом морфологических органических микро- и макроповреждений нервной ткани в ГМ, которые в ряде случаев существенно не меняют объема и массы мозга, но существенно сокращают регуляторный и управленческий потенциал ГМ. Другими словами, объем и масса поврежденного ГМ может практически не изменяться и (или) соответствовать возрастной норме, но при этом существенно влиять на сокращение продолжительности жизни хозяина этого ГМ. Для иллюстративности данного биологического феномена М. А. Шурдов вводит собственный новый термин: «одноразовый мозг», который в процессе жизни по-разному у разных людей изнашивается и реставрации и реконструкции практически не подлежит. Низкий регенеративный потенциал для саногенеза поврежденного ГМ, обусловленный малым количеством собственных НСК, неспособен обеспечить самореставрацию повреждений нервной ткани ГМ и спинного мозга (СМ). Масса мозга человека и его морфологическая структура, по мнению М. А. Шурдова, количественно может быть не изменена, но качественно молекулярно-биологическая (геномная, транскриптомная, протеомная, метаболомная и т.д.) структура этих клеток и всей нервной ткани может быть существенно трансформирована патологическими белками, нарушениями ДНК или РНК. Именно эти геномные, постгеномные или эпигенетические изменения в клетках нервной ткани ГМ и СМ являются фундаментальной причиной нарушения системообразующих и регуляторных функций ГМ и приводят к формированию системной дисрегуляции органов и систем организма, приводящей к сокращению продолжительности его жизни. По мнению М. А. Шурдова, термин «одноразовый мозг» подчеркивает очень важный научный факт того, что нервные клетки мозга это единственный, но резко ограниченный для самовозобновления (практически одноразовый) и дающийся при рождении невосполнимый ресурс, тогда как все другие клетки систем, органов и тканей человека способны к полному самообновлению, регенерации и замещению.
Человек рождается с анатомически сформированным головным и спинным мозгом, в котором количество нервных клеток составляет ~ 100 млрд. Мозг при рождении весит не более 100 г, а в зрелом возрасте ГМ составляет 1,5—2 кг, но количество клеток в нем не увеличивается, а к старости только уменьшается. Нервные клетки (нейроны) лишь увеличиваются в размере и удлиняют аксоны, которые достигают длины до 1—1,5 м. Сущность предложенной концепции заключается в биологическом феномене ограничения продолжительности жизни человека в зависимости от возрастного или болезнетворного накопления объема морфофункциональных повреждений, полученных его мозгом в период онтогенеза (жизни после рождения). Причиной этих молекулярно-биологических повреждений могут быть как эндогенные, так и экзогенные факторы окружающей среды, климата и профессиональных вредностей, приводящие к патогенетическим процессам в клетках нервной ткани. Невозможность или, точнее, резко ограниченная возможность самообновления клеток и низкий потенциал регенерации для реставрации поврежденной нервной ткани ГМ и СМ человека в процессе постнатального онтогенеза приводят к возрастзависимой дегенерации и атрофии нейронов, которые и формируют нарушения гомеостаза и блокирование биологических механизмов саногенеза органов и тканей организма и, несомненно, являются фундаментальными причинами сокращения продолжительности жизни. Степень выраженности молекулярно-биологического повреждения нервной ткани ГМ и СМ прямо пропорциональна продолжительности жизни человека. Нервные и психические болезни, в исходе которых лежит формирование органического морфологического дефекта нервной ткани, являются фундаментальной биологической и биофизической основой сокращения продолжительности жизни почти для всех болезней цивилизации. Именно морфологические дефекты нервной ткани ГМ и СМ сегодня легко объективизировать при помощи стандартной компьютерной томографии (КТ), так что легко выявить объем повреждения путем проведения денситометрии (программы компьютерного анализа изучения плотности ткани) КТ нервной ткани и рассчитать объем ишемизированной ткани ГМ, который соответствует диапазону плотности нервной ткани от 10 до 15 хаунсфилдов.
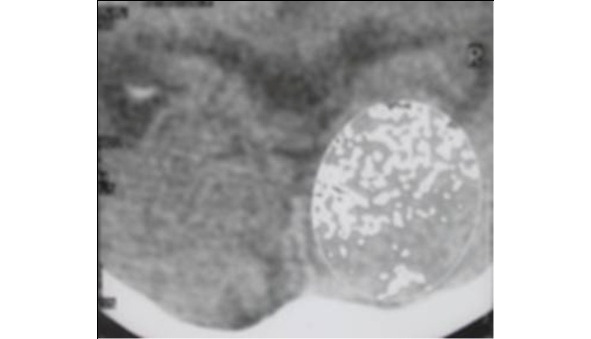
головного мозга на выявление очагов ишемии (от 5 до 14 H) для оценки объема повреждений мозга
Итак, доказанная продолжительность жизни человека сегодня лимитирована 120 годами, и преодолеть это ограничение пока никому не удалось. Возможно, это действительно связано с размерами головного мозга человека и молекулярно-биологической структурой, а может быть, с целым рядом неизвестных причин, обусловленных загрязнением окружающей среды, глобальным потеплением, изменением активности солнца, новыми климатическими условиями. Парацельс между тем был уверен, что человеку по силам жить 600 лет. Его русские коллеги Илья Мечников и Александр Богомолец давали нам срок жизни в 160 лет. Можно говорить о том, что на продолжительность жизни влияет наследственность, и отчасти это верно. Экология, питание, здоровый образ жизни — все это факторы влияния. Но даже из вышеприведенных примеров ясно, что многие долгожители не были ангелоподобными существами. Кто-то выпивал — кстати, некоторые даже весьма прилично; другие покуривали или даже дымили напропалую; третьи злоупотребляли кофе.
Социальный статус каждой возрастной группы и ее влияние в обществе тесно связаны с экономической продуктивностью этой группы. В аграрных обществах пожилые люди имеют высокий статус и являются объектом внимания. Их жизненный опыт и знания высоко ценятся, особенно в дописьменных обществах, где знания передаются устно. Потребность в их знаниях позволяет пожилым людям продолжать быть продуктивными членами общества.
В обществах с высоким уровнем индустриализации и урбанизации статус пожилых людей заметно изменился, уменьшив значение пожилых людей, а в некоторых случаях даже достигнув негативного отношения к старым людям — эйджизма. Оказывается, физическая неспособность пожилых людей трудиться играет относительно небольшую роль, а за потерю значения отвечает несколько иных факторов. Среди них наибольшую роль играет постоянное введение новых технологий, требующих непрерывного образования и тренировки, которые не так доступны старым людям. Меньшую роль играют большое число все еще достаточно крепких старых работников, которые ограничивают возможности трудоустройства новому поколению, и уменьшение количества людей, которые работают на себя, что могло бы дать старым людям возможность постепенного снижения количества работы. В связи с общим повышением уровня образования опыт старых людей, наоборот, играет все меньшую роль.
Хотя в некоторых областях, например в политике, пожилые люди все еще сохраняют высокую активность, в общем случае они все чаще уходят на пенсию с окончанием наиболее продуктивного периода жизни, что приводит к проблемам психологической адаптации к новым условиям. В первую очередь проблемы появляются в связи с уменьшением влияния старых людей, чувства собственной невостребованности и наличия значительного количества свободного времени. Кроме того, для большого количества людей в старости становятся острее финансовые проблемы, хотя во многих случаях эти проблемы ложатся на общество.
В связи с наличием свободного времени семейные взаимоотношения в большей мере стремятся быть центром внимания пожилых людей. Тем не менее в связи с изменениями в семейной структуре в развитых странах большие семьи разделились и пожилые люди все чаще не живут рядом со своими детьми и другими родственниками. Из-за этого перед обществами становится проблема большей приспособляемости пожилых людей к независимому существованию.
Важным фактором в социологии старения является сексуальная и репродуктивная активность. В развитых странах мужчины продолжают становиться отцами даже в возрасте 65 лет и старше. Для пожилых людей характерно сопротивление изменениям, хотя в большей мере это поясняется не неспособностью к приспосабливаемости, а увеличением толерантности. В помощь приспосабливаемости пожилых людей к новым условиям разрабатываются специальные учебные программы, рассчитанные на эту категорию людей.
В связи со снижением способности выполнять большинство типов работ в индустриальных и постиндустриальных обществах пожилые люди постепенно теряют источники дохода. Таким образом, они должны полагаться на собственные накопления, помощь детей и общества. Из-за меньшей уверенности в будущем пожилые люди отличаются тенденцией к сбережению и инвестированию средств вместо траты их на потребительские товары. На уровне государства старое население выбывает из рабочей силы, увеличивая нагрузку на активных работников и открывая дорогу к автоматизации производства.
Государственные социальные программы, помогающие людям преклонного возраста существовать в обществе, функционировали на определенном уровне, начиная со времен Римской империи. В средневековой Европе первый закон об ответственности государства перед пожилыми людьми был принят в Англии в 1601 г. Собственно пенсии были впервые введены в 1880 г. Отто фон Бисмарком в Германии. Сегодня большинство государств имеют какую-либо форму программ социального обеспечения для граждан преклонного возраста. Хотя эти государственные программы и облегчают тяжесть старости, они не приводят пожилых людей к уровню дохода, характерному для молодых.
Хотя физиологический эффект старения отличается среди индивидуумов, организм в целом с наступлением старости становится уязвим для многочисленных болезней, особенно хронических, требуя больше времени и средств на лечение. Со времен Средневековья и Античности средняя продолжительность жизни в Европе оценивалась между 20 и 30 годами. Сегодня продолжительность жизни значительно возросла, в результате чего все больший процент составляют пожилые люди. Потому типичные для пожилого возраста рак и болезни сердца стали намного более распространены.
Возрастающая стоимость медицинской помощи вызывает определенные проблемы как среди самих пожилых людей, так и для обществ, которые создают специальные институты и целевые программы, направленные на помощь пожилым людям. Многие развитые страны ожидают значительное старение населения в ближайшее время и потому беспокоятся об увеличении расходов для сохранения качества охраны здоровья на соответствующем уровне. Направления деятельности с целью преодоления этой проблемы заключаются в улучшении эффективности работы системы охраны здоровья, более целенаправленном оказании помощи, поддержке альтернативных организаций оказания медицинской помощи и влиянии на демографическую ситуацию.
Существует много вариаций между странами как в определении старения, так и в отношении к нему. Например, пенсионный возраст варьируется между разными странами в диапазоне от 55 до 70 лет. В первую очередь эта разница объясняется различиями в средней продолжительности жизни и трудоспособности пожилых людей. В дополнение, как указывалось выше, наблюдаются значительные различия между индустриальными и традиционными аграрными обществами. Тогда как в первых значение пожилых людей незначительно, в последних старость является признаком мудрости, а старые люди имеют большое влияние на общество.
Хотя в большей части государств некоторые права и обязанности (право голоса, право покупать алкоголь, уголовная ответственность и т.д.) предоставляются человеку начиная с определенного возраста, часто пожилые люди лишаются некоторых прав. Типичный пример: право занятия некоторых должностей (в основном руководящих).
В странах Запада в наши дни набирает популярность концепция «успешного старения», которая определяет, как наилучшим образом должно протекать старение, используя современные достижения медицины и геронтологии. Эта концепция может быть прослежена до 1950-х гг., но была популяризована в работе Роуи и Кана 1987 г. (Rowe, Kahn, 1987). Авторы критикуют исследования в геронтологии за преувеличение однородности исследованных людей и, согласно им, предыдущие исследования старости преувеличили степень, с которой такие болезни, как, например, диабет или остеопороз, могут быть приписаны возрасту.
В следующей публикации (Rowe, Kahn, 1997) авторы определили понятие успешного старения как комбинацию следующих факторов, которые должны сопровождать старение:
1) низкая вероятность болезней или инвалидности;
2) высокие возможности к обучению и физической деятельности;
3) активное участие в жизни общества.
Эти цели могут быть достигнуты как с помощью общества, так и благодаря известным усилиям пожилых людей по изучению и поддержке социальных связей, особенно с более молодыми людьми.
Социальные и экономические аспекты старения в настоящее время еще до конца не изучены и туманны, а в литературе существует достаточное количество необъяснимых фактов о данном биологическом феномене. Например, в 1993 г. в США родилась и прожила 20 лет девушка, которая практически не была подвержена возрастным изменениям. В 2009 г. 16-летняя Брук Гринберг в физическом и умственном отношении находилась на уровне годовалого ребенка: ее рост 76 см, вес — 7,3 кг, у нее молочные зубы, костная ткань соответствует 10-летнему возрасту, а мозг претерпел лишь незначительные изменения с раннего детства. Гринберг умерла в возрасте 20 лет от бронхомаляции. Американские ученые ведут поиски гена, который мог стать причиной состояния Гринберг. Не исключено, что он окажется ключом к пониманию всех процессов старения человеческого организма.
Ирландский землевладелец Браун, доживший, как считается, до 120 лет, завещал сделать себе надгробную надпись; вот ее текст: «Он был всегда пьян и так страшен в этом состоянии, что сама смерть боялась его». Вот и мысли долгожителя для всех нас… Но есть, есть-таки одно общее, что объединяет всех долгожителей мира, — это неистощимое жизнелюбие, оптимизм. Они жили долго, потому что искренне любили жизнь, и она отплатила им взаимностью. Однако только жажды жизни для этого явно недостаточно, т.к. мы пока не понимаем фундаментальных причин старения человека и млекопитающих. В следующей главе мы поговорим о различных теоретических взглядах и научных теориях ученых и исследователей всего мира на процесс старения.
Глава 4. Современные теории старения и концепции долголетия человека
История возникновения научных теорий старения человека является достаточно короткой и совсем небольшой по сравнению с 2 тыс. лет известной цивилизации, описанной в Библии. Мы не будем останавливаться на общеизвестных подходах к продлению жизни в древних цивилизациях и в Средние века, т.к. назвать их научными, наверное, было бы неправильно, хотя вся история человечества — это поиск Грааля бессмертия и чудодейственных средств продления собственной жизни. Сегодня существует несколько альтернативных теорий, которые отчасти противоречат друг другу, а отчасти друга друга дополняют. Современная биология уделяет проблеме старения очень много внимания, и с каждым годом появляются новые факты, позволяющие глубже понять механизмы этого процесса.
Первые попытки научного объяснения старения начались в конце XIX в. В 1882 г. в одной из первых работ известный зоолог и теоретик эволюционного учения Август Вейсман (Weissmann, 1882) предложил теорию происхождения старения как свойства, которое возникло в результате эволюции. Согласно А. Вейсману, «не стареющие организмы не только не являются полезными, они вредны, потому что занимают место молодых», что должно было привести эволюцию к возникновению старения. Его, правда чисто теоретическое, представление о старении и «бессмертии» клеток не было подтверждено им экспериментально, но он еще в 1881 г. предположил, что старение организма определяется тем обстоятельством, что у соматических клеток «…способность к росту путем деления не вечна, а ограниченна». По его же мнению, могут бесконечно входить в процесс деления только половые клетки, которые с этой точки зрения являются «бессмертными», т.е. иммортальными. Однако первые же опыты по выращиванию изолированных из организма клеток в культуре ткани, произведенные французским хирургом и патофизиологом Алексисом Каррелем (Carrel, 1912), казалось бы, полностью опровергли предположение А. Вейсмана о «смертности» соматических клеток. А. Каррель впервые в цитологической практике разработал технику выращивания культуры тканей с использованием плазмы крови и эмбриональной жидкости, позволившую длительное время поддерживать рост клеток, в т.ч. соматических, выделенных из организма. В своем самом известном эксперименте он удалил небольшое количество ткани из сердца эмбриона цыпленка, погрузил его в питательную среду и смог сохранить эту ткань живой в своей лаборатории. Спустя десятилетия после смерти самого Каррела в 1944 г. ткани цыпленка намеренно позволили умереть. За эти исследования, а также за разработку методик по сшиванию кровеносных сосудов А. Каррель в 1912 г. был удостоен Нобелевской премии. Вплоть до 1961 г. считалось, что постулат А. Вейсмана опровергнут, но американские цитологи Л. Хейфлик и П. Мурхед провели эксперименты по культивации фибробластов человеческих эмбрионов. Эти исследователи помещали в питательную среду отдельные клетки, а не цельный кусочек ткани, как это делал А. Каррель. Леонард Хейфлик обнаружил, что легочная ткань, по-видимому, отмирает после того, как ее клетки поделились определенное количество раз, обычно 50. Это число называли пределом Хейфлика. Более того: когда клетки приближались к своему пределу деления, они начинали напоминать старую ткань с возрастными пигментами, которые обнаруживаются в постаревших клетках сердца и головного мозга.
Оригинальную гипотезу старения выдвинул выдающийся русский биолог И. И. Мечников (1845–1916), который считал старение результатом интоксикации организма продуктами обмена бактерий, обитающих в кишечном тракте, и продуктами азотистого обмена веществ самого организма (мочевая кислота). Образуются ядовитые вещества, в т.ч. скатол, индол, фенол (карболовая кислота), крезол, кадаверин (трупный яд), тирамин и другие токсины. Данную теорию И. И. Мечников назвал теорией бактериальной интоксикации организма.
Важным шагом в исследовании старения был доклад английского биолога проф. Peter Brian Medawar перед Лондонским королевским обществом в 1951 г. под названием An Unresolved Problem in Biology («Нерешенная проблема биологии»; Medawar, 1952). В этой лекции он подчеркнул, что животные в природе редко доживают до возраста, когда старение становится заметным; таким образом, эволюция не могла оказывать влияние на процесс развития старения. Эта работа положила начало целой серии новых исследований. На протяжении следующих 25 лет исследования имели преимущественно описательный характер. Тем не менее начиная с конца 70-х гг. возникает большое количество теорий, которые пытались объяснить феномен старения (Древина, 2009). Например, в известном обзоре литературы по этому вопросу, опубликованном Калебом Финчем в 1990 г., насчитывалось ок. 4 тыс. ссылок (Finch, 1990) на различные научные исследования. Только в конце 1990-х гг. ситуация начала проясняться и большинство авторов стали приходить к общим выводам.
В настоящее время мир располагает более чем 300 общебиологическими теориями старения и психологическими подходами к определению сущности старости и старения. Остановимся очень кратко на основных биологических теориях старения человека. По мнению исследователей в области биологии, старение и смерть являются базовыми, сущностными биологическими свойствами, отражающими функционирование и эволюцию всех живых организмов, включая человека. Биологи исследуют организм, пытаясь измерить природу и предел возрастных изменений, понять, чем вызваны эти изменения, как их можно контролировать, корректировать, как можно смягчить последствия процесса старения. В этой связи биологическая наука располагает рядом теорий, непосредственно затрагивающих тематику процесса старения человека. Наиболее распространены в научном мире за рубежом два направления научных теоретических воззрений на него: это теории программированного старения и теории непрограммированного старения (Козлов, 1999).
Обобщая все вышеизложенные теории старения человека, попытаемся систематизировать наиболее значимые из них для современной геронтологии. Системный признак теории старения как запрограммированного или незапрограммированного старения может быть важным системообразующим звеном для целого ряда известных теорий старения.
Теории программированного старения
Генетические теории. Старение вызывается запрограммированными изменениями экспрессии генов, или экспрессией специфических белков. Гипотеза, согласно которой причиной старения являются изменения генетического аппарата клетки, является одной из наиболее признанных в современной геронтологии. Молекулярно-генетические теории подразделяются на две большие группы. Одни ученые рассматривают возрастные изменения генома как наследственно запрограммированные. Другие считают, что старение — результат накопления случайных мутаций. Отсюда следует, что процесс старения может являться или закономерным результатом роста и развития организма, или следствием накопления случайных ошибок в системе хранения и передачи генетической информации.
• Накопление «загрязнений»: накопление отходов метаболизма снижает жизнеспособность клеток;
• иммунологическая теория: определенные аллели могут увеличивать или сокращать продолжительность жизни;
• часы старения: старение и смерть являются результатом предопределенного биологического плана;
• эволюционные теории: естественный отбор устраняет индивидуумов после того, как они произведут потомство.
Теории «непрограммированного» старения
• Свободнорадикальная теория старения: старение является результатом случайного вредоносного повреждения тканей свободными радикалами;
• теория изнашивания: органы и ткани организма в процессе жизни изнашиваются, как изнашиваются и запчасти, «заложенные» в организме для их реставрации, и практически у организма не остается ресурса для их замещения при повреждении;
• теория старения по ошибке: основной причиной старения является накопление с возрастом генетических повреждений в результате мутаций, которые могут быть как случайными (спонтанными), так и вызванными различными повреждающими факторами (ионизирующая радиация, стрессы, ультрафиолетовые лучи, вирусы, накопление в организме побочных продуктов химических реакций и др.). Гипотеза старения по ошибке была выдвинута в 1954 г. американским физиком М. Сциллардом. Исследуя эффекты воздействия радиации на живые организмы, он показал, что действие ионизирующего излучения существенно сокращает срок жизни людей и животных. Под воздействием радиации происходят многочисленные мутации в молекуле ДНК и инициируются некоторые симптомы старения, такие как седина или раковые опухоли. Из своих наблюдений Сцилард сделал вывод, что мутации являются непосредственной причиной старения живых организмов, однако он не объяснил факта старения людей и животных, не подвергавшихся облучению. Его последователь Л. Оргель считал, что мутации в генетическом аппарате клетки могут быть либо спонтанными, либо возникать в ответ на воздействие агрессивных факторов: ионизирующей радиации, ультрафиолета, вирусов и токсических (мутагенных) веществ и т. д. С течением времени система репарации ДНК изнашивается, в результате чего происходит старение организма.
Теория запрограммированного старения — одна из самых распространенных научных теорий. Представители теории запрограммированного старения исходят из того, что функционирование живого организма запрограммировано природой лишь на период его активной жизнедеятельности, включающей развитие, т.е. рост организма, и способность к репродукции. Сторонники этой теории аргументируют свой вывод тем, что в природе всегда действовал и продолжает действовать закон естественного отбора и поэтому старые особи в естественных условиях встречаются крайне редко: прежде чем стать старыми, они либо погибают сами, либо их уничтожают свои же сородичи. В живой организм генетически заложена биологическая активность, распространяющаяся только на период его так называемой биологической полезности.
Некоторые теории старения, как, например, так называемые теории часов, исходят из того, что изменения, связанные со старением, подконтрольны своего рода биологическому датчику, основная функция которого состоит в том, чтобы следить за «расписанием» развития биологического организма до тех пор, пока он не достигнет половой зрелости и способности размножения. После выполнения программы или в отсутствие таковой расстраивается деятельность гипоталамуса и эндокринной системы, что приводит организм к снижению его физиологических функций (Козлов, 1999).
Представители теории программированного старения исходят из положения, согласно которому к процессу старения подключены генетические механизмы и только благодаря их действию происходит эволюция живой природы. Однако в процессе изменений, связанных со старением, могут действовать и другие механизмы, не включенные в генетическую программу, которые оказывают «непрограммированное» воздействие на организм. Такое воздействие может происходить в результате случайного повреждения клетки, необычного воздействия на молекулы, которые, в свою очередь, изменяют структуру клетки, ее функцию и сам процесс метаболизма. Эти необычные изменения могут затронуть и молекулу ДНК, несущую в себе генетическую информацию.
В результате нормальных метаболических процессов в пределах клеток могут образовываться ядовитые побочные продукты типа свободных радикалов. Их вредному воздействию противостоят несколько механизмов защиты клеток. Однако свободные радикалы могут повредить мембрану клетки и вызвать сбой в передаче генетической информации ДНК.
Таким образом, подход, в основе которого лежит представление о старении как процессе, запрограммированном эволюцией и включенном в генетический код (программируемое старение), и подход, согласно которому повреждения клеток не детерминируются генетически, а происходят вследствие сбоев (непрограммированного старения), имеют общий биологический характер в объяснении причин инволюции в старости. Стоит отметить, что в зависимости от предложенного механизма старения (в рамках биологического подхода) авторы выстраивают систему прогнозирования будущего состояния организма, мер профилактики негативных последствий, однако роль психологического фактора для увеличения продолжительности человеческой жизни при этом не учитывается.
Обе эти биологические теории старения являются очень общими, слишком широко трактующими причины процессов инволюции, происходящих в старости. В рамках этих подходов находят место теория основоположника отечественной геронтологии А. А. Богомольца, который связывал старение с дисгармонией физиологических процессов организма, и теория И. И. Мечникова, рассматривавшего старение как процесс интоксикации (Яцемирская, Беленькая, 1999).
Биологические теории старения являются наиболее обоснованными и верифицированными (в плане психологических исследований старости мы будем говорить не о теориях, а лишь о подходах к проблеме). Однако биологические теории не учитывают дифференциации двух аспектов старости — физиологического и психологического — и роли психологического фактора в удлинении человеческой жизни.
Все биологические теории старения можно условно разделить еще на две большие группы: эволюционные теории и теории, основанные на случайных повреждениях клеток. Первые считают, что старение является не необходимым свойством живых организмов, а запрограммированным процессом. Согласно им, старение развилось в результате эволюции из-за некоторых преимуществ, которые оно дает целой популяции. В отличие от них теории повреждения предполагают, что старение является результатом природного процесса накопления повреждений со временем, с которыми организм старается бороться, а различия старения у разных организмов являются результатом разной эффективности этой борьбы. Сейчас последний подход считается установленным в биологии старения (Kirkwood, 2005; Holliday, 2006; Hayflick, 2007). Тем не менее некоторые исследователи все еще защищают эволюционный подход (http://www.azinet.com/articles/Aging_Evolution.html), а некоторые другие совсем игнорируют деление на эволюционные теории и теории повреждений. Последнее утверждение является частично результатом смены терминологии: в некоторых работах последнего времени термин «эволюционные теории» ссылается не на теории запрограммированного старения, которые предлагают эволюционное возникновение старения как полезного явления, а на подход, который описывает, почему организмы должны стареть, в противоположность вопросу о биохимических и физиологических основах старения.
Гормонально-генетическая теория. Эта теория состоит в том, что в процессе жизни человека начиная с рождения идет повышение порога чувствительности гипоталамуса, что в конечном итоге после 40 лет приводит к гормональному дисбалансу и прогрессирующему нарушению всех видов обмена, в т.ч. гиперхолестеринемии. Поэтому одно из мнений, что лечение болезней старости необходимо начинать с улучшения чувствительности гипоталамуса, является краеугольным в этой теории.
Эволюционно-генетическая теория. Гипотеза, которая легла в основу эволюционно-генетического подхода, была предложена Питером Медаваром в 1952 г. (Medawar, 1952) и известна сейчас как теория накопления мутаций (англ. Mutations accumulation theory). Питер Медавар заметил, что животные в природе очень редко доживают до возраста, когда старение становится заметным. Согласно его идее, аллели, которые проявляются на протяжении поздних периодов жизни и которые возникают в результате мутаций зародышевых клеток, подвергаются довольно слабому эволюционному давлению, даже если в результате их действия страдают такие свойства, как выживание и размножение. Таким образом, эти мутации могут накапливаться в геноме на протяжении многих поколений. Тем не менее любая особь, которая сумела избежать смерти на протяжении долгого времени, испытывает на себе их действие, что проявляется как старение. То же самое верно и для животных в защищенных условиях.
В дальнейшем, в 1957 г. Д. Вильямс (Williams, 1957) предположил существование плейотропных генов, которые имеют разный эффект для выживания организмов на протяжении разных периодов жизни, т.е. они полезны в молодом возрасте, когда эффект естественного отбора сильный, но вредны позднее, когда эффект естественного отбора слабый. Эта идея сейчас известна как антагонистическая плейотропия (англ. Antagonistic pleiotropy).
Вместе две эти теории составляют основу современных представлений о генетике старения (Kirkwood, 2005). Тем не менее идентификация ответственных генов имела лишь ограниченный успех. Свидетельства о накоплении мутаций остаются спорными (Shaw et al., 1999), тогда как свидетельства наличия плейотропных генов сильнее, но и они недостаточно обоснованы. Примерами плейотропных генов можно назвать ген теломеразы у эукариотов и сигма-фактор σ70 у бактерий. Хотя известно много генов, которые влияют на продолжительность жизни разных организмов, других четких примеров плейотропных генов все еще не обнаружено (Leroi et al., 2005).
Эволюционно-физиологическая теория. Теория антагонистической плейотропии предсказывает, что должны существовать гены с плейотропным эффектом, естественный отбор которых и приводит к возникновению старения. Несколько генов с плейотропным эффектом на разных стадиях жизни действительно найдены — сигма-70 E. coli, теломераза у эукариотов, — но непосредственной связи со старением показано не было, тем более не было показано, что это типичное явление для всех организмов, ответственное за все эффекты старения. То есть эти гены могут рассматриваться лишь как кандидаты на роль генов, предсказанных теорией. С другой стороны, ряд физиологических эффектов показан без определения генов, ответственных за них. Часто мы можем говорить о компромиссах, аналогичных предсказанным теорией антагонистической плейотропии, без четкого определения генов, от которых они зависят. Физиологическая основа таких компромиссов заложена в так называемой теории одноразовой сомы (англ. Disposable soma theory; Kirkwood, 1977). Эта теория задается вопросом, как организм должен распорядиться своими ресурсами (в первом варианте теории речь шла только о энергии) между поддержкой и ремонтом сомы и другими функциями, необходимыми для выживания. Необходимость компромисса возникает из-за ограниченности ресурсов или необходимости выбора лучшего пути их использования.
Поддержание тела должно осуществляться лишь настолько, насколько это необходимо на протяжении обычного времени выживания в природе. Например, поскольку 90% диких мышей умирает на протяжении первого года жизни, преимущественно от холода, инвестиции ресурсов в выживание на протяжении большего времени будут касаться только 10% популяции. Таким образом, трехлетняя продолжительность жизни мышей полностью достаточна для всех потребностей в природе, а с точки зрения эволюции ресурсы следует тратить, например, на улучшение сохранения тепла или размножения вместо борьбы со старостью. Таким образом, продолжительность жизни мыши наилучшим образом отвечает экологическим условиям ее жизни.
Теория «одноразового тела». Эта теория делает несколько допущений, которые касаются физиологии процесса старения. Согласно этой теории, старение возникает в результате неидеальных функций ремонта и поддержки соматических клеток, которые адаптированы для удовлетворения экологических потребностей. Повреждения, в свою очередь, являются результатом стохастических процессов, связанных с жизнедеятельностью клеток. Долголетие контролируется за счет контроля генов, которые отвечают за эти функции, а бессмертие генеративных клеток, в отличие от соматических, является результатом больших затрат ресурсов и, возможно, отсутствия некоторых источников повреждений.
На особом месте в этой теоретической конструкции стоит разработанная М. А. Шурдовым концепция старения, обусловленная «одноразовым мозгом». Согласно этой концепции, головной мозг человека стареет в первую очередь из-за того, что состоит из клеток нервной ткани, которые не имеют возможности для деления. Мозг млекопитающих как бы одноразового использования, хотя почти все органы и ткани его организма имеют способность к самообновлению и регенерации. Отсутствие способности у мозга к саногенезу и самореставрации и есть основное «слабое звено» в организме, и оно запускает системообразующие процессы. Человек рождается с маленьким головным мозгом, в котором уже есть ок. 100 млрд нервных клеток. С возрастом мозг вырастает в объеме и аксоны его нейронов достигают длины до 1 м, но количество клеток нервной ткани в мозге лишь уменьшается, однако при этом в процессе жизни, воспитания и обучения между этими клетками формируются новые синаптические связи. Именно количество связей между клетками в мозге определяет наличие определенных функциональных систем в организме и формирует жизнеобеспечивающие функции мозга. М. А. Шурдов пришел к выводу, что именно старение клеток нервной ткани головного мозга является «генератором» общего процесса увядания и старения всех систем организма человека. Нарушение центральных систем управления и надзора за органами и тканями организма со стороны увядающего и стареющего мозга при его локальной дегенерации синхронизирует общий системный возрастной дегенеративно-атрофический процесс в органах и тканях. Сосуды головного и спинного мозга человека одними из первых компонентов нервной ткани страдают в процессе этого старения за счет формирования повреждений сосудов мозга и запускают системные процессы дегенерации, атрофии и увядания в органах и тканях организма. М. А. Шурдов считает, что нейрореставрация стареющего мозга позволит значительно приостановить общеорганизменные системные процессы старения.
Свободнорадикальная теория старения
Выдвинутая практически одновременно Д. Харманом (1956) и Н. М. Эмануэлем (1958), свободнорадикальная теория объясняет не только механизм старения, но и широкий круг связанных с ним патологических процессов (сердечно-сосудистых заболеваний, ослабления иммунитета, нарушений функции мозга, катаракты, рака и некоторых других). Согласно этой теории, причиной нарушения функционирования клеток являются необходимые для многих биохимических процессов свободные радикалы — активные формы кислорода, синтезируемые главным образом в митохондриях — энергетических «фабриках» клеток. Если очень агрессивный, химически активный свободный радикал случайно покидает то место, где он нужен, он может повредить и ДНК, и РНК, и белки, и липиды. Природа предусмотрела механизм защиты от избытка свободных радикалов: кроме супероксиддисмутазы и некоторых других синтезируемых в митохондриях и клетках ферментов, антиоксидантным действием обладают многие вещества, поступающие в организм с пищей, в т.ч. витамины А, С и Е. Регулярное потребление овощей и фруктов и даже несколько чашек чая или кофе в день обеспечат вам достаточную дозу полифенолов, также являющихся хорошими антиоксидантами. К сожалению, избыток антиоксидантов — например, при передозировке биологически активных добавок — не только не полезен, но может даже усилить окислительные процессы в клетках.
Существуют свидетельства нескольких важнейших механизмов повреждения макромолекул, которые обычно действуют параллельно один другому или зависят один от другого (Kirkwood, 2005). Вероятно, любой из этих механизмов может при определенных обстоятельствах играть доминирующую роль. Во многих из этих процессов важную роль играют активные формы кислорода (в частности, свободные радикалы); набор свидетельств об их влиянии был получен достаточно давно и сейчас известен под названием «свободнорадикальная теория старения». Сегодня, тем не менее, механизмы старения намного более детализированы.
Теория соматических мутаций. Многие работы показали увеличение с возрастом числа соматических мутаций и других форм повреждения ДНК, предлагая репарацию (ремонт) ДНК в качестве важного фактора поддержки долголетия клеток. Повреждения ДНК типичны для клеток и вызываются такими факторами, как жесткая радиация и активные формы кислорода, и потому целостность ДНК может поддерживаться только за счет механизмов репарации. Действительно, существует зависимость между долголетием и репарацией ДНК, как это было продемонстрировано на примере фермента поли (АДФ-рибоза) полимеразы-1 (PARP-1), важного игрока в клеточном ответе на вызванное стрессом повреждение ДНК (Burke, 2001). Более высокие уровни PARP-1 ассоциируются с большей продолжительностью жизни.
Теория апоптоза. Академик РАН проф. В. П. Скулачев называет свою теорию теорией клеточного апоптоза. Апоптоз — процесс запрограммированной гибели клетки. Как деревья избавляются от частей, чтобы сохранить целое, так и каждая отдельная клетка, пройдя свой жизненный цикл, должна отмереть и ее место должна занять новая. Если клетка заразится вирусом, или в ней произойдет мутация, ведущая к озлокачествлению, или просто истечет срок ее существования, то, чтобы не подвергать опасности весь организм, она должна умереть. В отличие от некроза — насильственной гибели клеток из-за травмы, ожога, отравления, недостатка кислорода в результате закупоривания кровеносных сосудов и т.д., при апоптозе клетка аккуратно саморазбирается на части и соседние клетки используют ее фрагменты в качестве строительного материала. Самоликвидации подвергаются и митохондрии; изучив этот процесс, В. П. Скулачев назвал его митоптозом. Митоптоз происходит, если в митохондриях образуется слишком много свободных радикалов. Когда количество погибших митохондрий слишком велико, продукты их распада отравляют клетку и приводят к ее апоптозу. Старение, с точки зрения В. П. Скулачева, — результат того, что в организме гибнет больше клеток, чем рождается, а отмирающие функциональные клетки заменяются соединительной тканью. Суть его работы — поиск методов противодействия разрушению клеточных структур свободными радикалами. По мнению ученого, старость — это болезнь, которую можно и нужно лечить, программу старения организма можно вывести из строя и тем самым выключить механизм, сокращающий нашу жизнь. По мнению В. П. Скулачева, главная из активных форм кислорода, приводящих к гибели митохондрий и клеток, — перекись водорода. В настоящее время под его руководством проходит испытания препарат SKQ, предназначенный для предотвращения признаков старения.
Теория накопления измененных белков. Так же важен для выживания клеток кругооборот белков, для которого критично появление поврежденных и лишних белков. Окисленные белки являются типичным результатом влияния активных форм кислорода, которые образуются в результате многих метаболических процессов клетки и часто мешают корректной работе белка. Тем не менее механизмы репарации не всегда могут распознать поврежденные белки и становятся менее эффективными с возрастом (Kirkwood, 2005) за счет снижения активности протеосомы (Carrard et al., 2002). В некоторых случаях белки являются частью статических структур, таких как клеточная стенка, которые не могут быть легко разрушены. Кругооборот белков зависит также и от белков-шаперонов, которые помогают белкам получать необходимую конформацию. С возрастом наблюдается снижение репарирующей активности (Soti, Csermey, 2003), хотя это снижение может быть результатом перегрузки шаперонов (и протеасомы) поврежденными белками.
Существуют свидетельства, что накопление поврежденных белков действительно происходит с возрастом и может отвечать за такие ассоциированные с возрастом болезни, как болезнь Альцгеймера, болезнь Паркинсона и катаракта.
Митохондриальная теория старения. Митохондриальная теория старения впервые была предложена в 1978 г. (митохондриальная теория развития, старения и злокачественного роста; Лобачёв, 1985). Суть ее заключается в том, что замедление размножения митохондрий в высокодифференцированных клетках вследствие дефицита кодируемых в ядре митохондриальных белков создает условия для возникновения и селективного отбора дефектных делеционных мтДНК, увеличение доли которых постепенно снижает энергетическое обеспечение клеток. В 1980 г. была предложена радикальная митохондриальная теория старения (Miquel et al., 1980). В настоящее время накопилось много данных, свидетельствующих о том, что свободные радикалы не являются причиной естественного старения. Эти данные не опровергают митохондриальную теорию старения (Lobachev, 1985), которая опирается на свободные радикалы, но доказывают ложность радикального варианта митохондриальной теории старения (Miquel et al., 1980).
Важность связи между молекулярным стрессом и старением была предположена на основании наблюдений за эффектом накопления мутаций в митохондриальной ДНК (мтДНК) (Wallace, 1999). Эти данные были подкреплены наблюдением увеличения с возрастом числа клеток, которым не хватает цитохром-с-оксидазы (COX), что ассоциировано с мутациями мтДНК. Такие клетки часто имеют нарушения в производстве АТФ и клеточном энергетическом балансе.
Теломерная теория старения. Это одна из самых общепризнанных теорий старения, и поэтому мы остановимся на ней более подробно. В 1971 г. советский биолог Алексей Матвеевич Оловников предположил, что ограниченное количество делений клетки связано с механизмом удвоения ДНК. Он устроен так, что концы линейных хромосом — теломеры — с каждым делением укорачиваются, поэтому после некоторого количества делений клетка больше делиться не может. А. М. Оловников сформулировал проблему концевой недорепликации линейных молекул ДНК, поскольку ДНК-полимераза не может реплицировать несколько нуклеотидов на 3» -конце матрицы ДНК. Он же высказал мысль о том, что должен существовать особый биологический механизм, предотвращающий этот эффект. Предполагалось также, что названный механизм действует в половых, а также раковых клетках и в клетках организмов, размножающихся вегетативным путем, и не действует в большинстве других случаев, в частности во многих наших соматических клетках. Впоследствии предсказанный А. М. Оловниковым фермент, компенсирующий укорочение ДНК, был действительно обнаружен во всех типах клеток, перечисленных выше, и назван теломеразой. Фермент теломераза занимается тем, что наращивает на концах ядерной ДНК многократно повторяемый гексануклеотид (TTAGGG у человека), образующий теломеру. В итоге укорочение линейной ДНК затрагивает лишь этот нетранскрибируемый текст теломерного участка хромосомы, но не приводит к утрате наследственной информации и не нарушает механизма ее считывания. На определенной стадии развития, приходящейся на ранний эмбриогенез, в подавляющем большинстве соматических клеток человека происходит «выключение» гена, кодирующего теломеразу. Тем самым гено́м оказывается беззащитным перед опасностью укорочения. Медленно, но верно теломера укорачивается, что приводит к ухудшению функционирования хромосом. Это ухудшение наступает задолго до того, как исчезнет вся теломера и начнется деградация смысловых участков ДНК. Дело в том, что теломера, помимо защиты от потери генетического материала при репликации, играет также какую-то неясную пока структурную роль в расположении хромосом внутри ядра и в правильном их функционировании (Хлюпина, 2014). Сама же теломера была открыта в 1932 г. американским ученым Германом Джозефом Мёллером. Теломера — это концевая часть плеча хромосомы, представляющая собой повторяющиеся последовательности ДНК. Длина теломер у разных видов различна и меняется от приблизительно 300–600 пар оснований у дрожжей до многих тысяч пар оснований у человека. Состоят теломерные повторы из TG-богатых единиц длиной 6–8 п. о. Эти последовательности играют важную роль в защите концов хромосом от деградации. Хромосома имеет две теломеры. Теломера содержит 242 специальные последовательности ДНК, обеспечивающие точную репликацию хромосом. Считается, что функциями теломерного повтора также являются защита хромосом от деградации и предотвращение их слияния друг с другом. Анализ длины теломерных повторов выявил, что соматические клетки теряют от 50 до 200 нуклеотидов при каждом клеточном делении. Причина этого — неполная репликация концов хромосом из-за особенностей молекулярного механизма репликативного синтеза ДНК. Отстающая цепь репликативной вилки в синтезе ДНК не может синтезироваться до 5» -конца в отсутствие рибопраймера, который, в свою очередь, не образуется непосредственно на концевом фрагменте. Потери концевой ДНК делают невозможной бесконечную пролиферацию. Предполагают, что укорачивание хромосом до определенного размера индуцирует процессы клеточного старения, а длина теломер, по этим представлениям, может служить мерой пролиферативного потенциала клеток. Предложено несколько гипотетических моделей, объясняющих, каким образом клетка «устанавливает» длину своих теломер и в определенный момент запускает механизм блока пролиферации. Возможно, общее количество ТТАGGG-повторов определяется благодаря учету специфически связывающегося с ними белка. Другая модель исходит из того, что длинные теломеры молодых клеток представляют собой гетерохроматиновые блоки. Предполагается, что ген, супрессирующий программу клеточного старения, локализован в субтеломерном районе. По мере укорачивания теломер все больше субтеломерной ДНК подвергается гетерохроматизации. Гетерохроматизация гена-супрессора приводит к его инактивации и запуску механизма клеточного старения. Обнаружено, что в соматических клетках, делящихся в организме, длина теломер со временем уменьшается. Укорочение теломер наблюдается также по мере старения фибробластов в культуре. Более того, оказалось, что длина теломер лучше предсказывает способность клетки к делению, чем возраст донора клеток. Предположительно теломеры укорачиваются в результате того, что механизм, ответственный за удвоение ДНК в процессе клеточного деления, делает характерную ошибку: в каждой новой копии ДНК элиминируется маленький участок каждой теломеры. Из этого следует, что теломеры могут быть теми «часами», которые определяют в клетках потерю способности к пролиферации. Интересно, что длина теломер сохраняется или даже немного увеличивается в сперматозоидах и в трансформированных («бессмертных») клетках. Такое постоянство помогает объяснить, каким образом половые и злокачественные клетки не утрачивают способности к делению. После обнаружения теломер возник вопрос об их природе. Необходимо было установить механизм их образования на концах 23 хромосомы. Американские ученые К. Грейдер и Э. Блэкберн проводили исследование с целью выяснить, не участвует ли в формировании ДНК теломер какой-то неизвестный до этого времени фермент. В 1984 г. К. Грейдер обнаружила признаки ферментативной активности в клеточном экстракте. Обнаруженный энзим Э. Блэкберн и К. Грейдер назвали теломеразой. После его выделения и очистки ученые установили, что он состоит не только из протеина, но и из РНК, которая содержит ту же последовательность, что и теломера. Таким образом, РНК служит шаблоном для построения теломеры, в то время как белковый компонент фермента необходим непосредственно для ферментативной деятельности. Теломераза удлиняет ДНК теломеры, обеспечивая платформу, которая, в свою очередь, позволяет ДНК-полимеразам скопировать хромосому по всей длине без потери генетической информации. Таким образом, хромосома при копировании не укорачивается. Во многих клетках человека утрата их способности к делению связана с утратой теломер на концах хромосом после определенного количества делений. Это происходит из-за отсутствия фермента теломеразы, который обычно экспрессируется только у зародышевых и стволовых клеток. Теломераза позволяет им непрерывно делиться, формируя ткани и органы. У взрослых организмов теломераза экспрессируется в клетках, которые должны часто делиться, однако большинство соматических клеток ее не производят.
Полина Ребенина (2017) в своей статье сделала ряд обобщений о том, что фермент теломераза, который восстанавливает концы ДНК, способен достраивать укороченные концы хромосомы в клетках опухолей, что делает их бессмертными. Поэтому предел в 50 делений справедлив не для всех клеток: раковые, а также стволовые клетки могут делиться бесчисленное количество раз. Этот фермент всякий раз «заводит внутренние часы» заново при слиянии женской и мужской половых клеток. Благодаря ему дети проживают свой срок сполна, а не получают в наследство кусок жизни, как это, например, произошло с клоном овечки Долли. Хотя на самом деле неизвестно, насколько разрушение теломер влияет на процесс старения: основные исследования направлены на процессы сохранения целостности ДНК и в особенности ее теломерных участков, особенно при раке. Майкл Фоссел в одном из интервью (Fossel, 2016) предположил, что лечение теломеразой может использоваться не только для борьбы с раком, но и для борьбы со старением человеческого организма, увеличивая продолжительность жизни. Недавно было обнаружено, что окислительный стресс также может иметь влияние на утрату теломер, значительно ускоряя этот процесс в определенных тканях (von Zglinicki, 2002).
Позднее А. М. Оловников пришел к выводу, что данная теория не объясняет причины старения полностью, и внес в нее уточнения. Он предложил новую редусомную теорию старения. Редусома — это маленькая ядерная частица, располагающаяся в субтеломерных частях хромосомы. Оловников считал, что линейная молекула ДНК редусомы постепенно укорачивается из-за уменьшения ее линейной молекулы ДНК, покрытой белками, что приводит к уменьшению содержащихся в ней генов. Именно это укорочение молекул ДНК редусомы является отсчетом биологического времени и причиной старения. Однако эта последняя теория не получила того же одобрения со стороны ученых-геронтологов, как теломерная теория.
Эпигенетическая теория старения. Клетки со временем медленно теряют маркеры репрессированного хроматина, что может быть связано с дифференцировкой клеток в организме. Утрата маркеров репрессии рано или поздно должна приводить к дерепрессии дремлющих транспозонов, соответственно, к росту количества вызванных ими повреждений ДНК с последующей активацией клеточных систем репарации ДНК. Последние, помимо участия в восстановлении ДНК, вызывают и несанкционированные рекомбинации в теломерах. Также не исключено, что рекомбиназы транспозонов могут непосредственно инициировать подобные рекомбинации. В результате протяженные участки теломерной ДНК преобразуются в кольца и теряются, а теломеры укорачиваются на длину утраченной кольцевой ДНК. Данный процесс ускоряет утрату теломерной ДНК в десятки раз, а последующий апоптоз большинства клеток и предопределяет старение как биологическое явление. Предложенная теория является альтернативой гипотезе о генетически запрограммированном старении и гипотезе о старении как следствии накопления ошибок и повреждений, объясняет механизм ускорения утраты теломер в случае окислительного стресса и повреждений ДНК, а также взаимосвязь старения и возникновения опухолей (Галицкий, 2009).
В последнее время в качестве важного фактора старения рассматривается метилирование ДНК. Так, определение эпигенетического старения по метилированию ДНК генов ITGA2B, ASPA и PDE4C позволяет определить биологический возраст человека со средним абсолютным отклонением от хронологического возраста, не превышающим 5 лет. Эта точность выше, чем возрастные прогнозы на основе длины теломер (Weidner et al., 2014).
На первых этапах исследования старения многочисленные теории рассматривались как конкурирующие в пояснении эффекта старения. Тем не менее сегодня считается, что многие механизмы повреждения клеток действуют параллельно и клетки также должны тратить ресурсы на борьбу со многими механизмами. Для исследования взаимодействия между всеми механизмами борьбы с повреждениями был предложен системный подход к старению, который пытается одновременно принять во внимание большое количество таких механизмов. Более того, этот подход может четко разделить механизмы, которые действуют на разных стадиях жизни организма. Например, постепенное накопление мутаций в митохондриальной ДНК часто приводит к накоплению активных форм кислорода и снижению производства энергии, что, в свою очередь, приводит к увеличению скорости повреждения ДНК и белков клеток.
Другой аспект, который делает системный подход привлекательным, — это понимание разницы между разными типами клеток и тканей организма. Например, клетки, которые активно делятся, с большей вероятностью пострадают от накопления мутаций и утраты теломер, чем дифференцированные клетки. В то же время необходимо уточнить, что данный тезис не относится к быстро и многократно делящимся трансформированным и опухолевым клеткам, которые не утрачивают теломер и не накапливают мутаций. Дифференцированные клетки с большей вероятностью пострадают от повреждения белков, чем клетки, которые быстро делятся и «разбавляют» поврежденные белки вновь синтезированными. Даже если клетка теряет способность к пролиферации за счет процессов старения, баланс механизмов повреждения в ней сдвигается.
Другим подходом к изучению старения являются исследования популяционной динамики старения. Все математические модели старения можно примерно разбить на два главных типа: модели данных и системные модели (Новосельцев и др., 2003). Модели данных — это модели, которые не используют и не пытаются пояснить какие-либо гипотезы о физических процессах в системах, для которых эти данные получены. К моделям данных относятся, в частности, все модели математической статистики. В отличие от них, системные модели строятся преимущественно на базе физических законов и гипотез о структуре системы, главной в них является проверка предложенного механизма.
Первым законом старения является закон Гомпертца, который предлагает простую количественную модель старения. Этот закон дает возможность разделить два типа параметров процесса старения. Исследования отклонения закона старения от кривой Гомпертца могут дать дополнительную информацию относительно конкретных механизмов старения данного организма. Самый известный эффект такого отклонения — выход смертности на плато в позднем возрасте вместо экспоненциального роста, наблюдавшийся во многих организмах (Mueller, Rose, 1996). Для пояснения этого эффекта было предложено несколько моделей, среди которых вариации модели Стрелера — Милдвана (Там же) и теории надежности (Gavrilov, Gavrilova, 2006).
Системные модели рассматривают много отдельных факторов, событий и явлений, которые оказывают непосредственное влияние на выживание организмов и рождение потомства. Эти модели рассматривают старение как баланс и перераспределение ресурсов как в физиологическом (в течение жизни одного организма), так и в эволюционном аспектах. Как правило, особенно в последнем случае, речь идет о распределении ресурсов между непосредственными затратами на рождение потомства и затратами на выживание родителей (Новосельцев и др., 2003).
Старость как базовое биологическое свойство всех живых организмов рассматривается в теориях клеточных отходов, старения иммунной системы и цитологической теории. В каждой из этих теорий обосновывается своя модель механизма старения организма. В рамках биологического подхода рассматривается теория основоположника отечественной геронтологии В. А. Богомольца, который утверждал, что основным фактором старения является нарушение гармонии физиологических процессов.
Геронтолог В. В. Фролькис определяет старость как период сокращения адаптивных возможностей организма. Анализируя фундаментальные механизмы старения, автор не только констатирует факт снижения адаптивных возможностей организма, но и показывает тенденции саморегуляции, которые противодействуют процессам разрушения и направлены на стабилизацию жизнедеятельности и увеличения продолжительности жизни. Понятие антистарения, или витаукт (лат. vita — жизнь, auctum — увеличивать), является важным аспектом предложенной им адаптационно-регуляторной теории старения.
Подход, в основе которого лежит представление о старении как процессе, запрограммированном эволюцией и включенном в генетический код (программируемое старение), и подход, согласно которому повреждения клеток не детерминируются генетически, а происходят вследствие сбоев (непрограммированное старение), имеют общий биологический характер в объяснении причин инволюции в старости. Стоит отметить, что в зависимости от предложенного механизма старения (в рамках биологического подхода) авторы выстраивают систему прогнозирования будущего состояния организма, мер профилактики негативных последствий, однако роль психологического фактора для увеличения продолжительности человеческой жизни при этом не учитывается.
Целый спектр научных теорий старения рассматривает старость как социальную проблему. В теории освобождения, «выхода из игры» старение описывается как непременный процесс последовательного разрушения социальных связей. Данный процесс включает изменения мотивации, концентрации собственного внутреннего мира и снижение уровня коммуникаций. Объективными его проявлениями являются потеря социальных ролей, ухудшение состояния здоровья, снижение доходов, а также потеря близких людей. Разрушение социальных связей каждый индивид субъективно переживает как сужение спектра интересов, сосредоточенность на себе, осознание собственной ненужности.
Суть теории заключается в том, что определенный процесс разрушения биологически и психологически обусловлен и неизбежен. Разрыв между личностью и обществом происходит после выхода на пенсию. Сначала пожилой человек поддерживает старые связи, интересуется тем, что происходит на работе; со временем эти связи становятся «неорганическими» и постепенно прерываются. Количество информации, которую получает человек, уменьшается, снижается активность, в связи с чем ускоряется процесс старения.
Главный аспект теории активности — прямая связь между уровнем активности личности и удовлетворенностью жизнью. Согласно данной теории, пожилые люди должны привлекаться к общественной жизни, что существенно повысит положительные проявления эмоциональной сферы. Концепция непрерывного жизненного пути трактует старость как процесс борьбы за сохранение привычного стиля жизни.
Другая группа теорий старения рассматривает старость как исключительно когнитивную проблему. В основе этого подхода лежит так называемая модель дефицита — процесс потери или снижения эмоциональных и интеллектуальных способностей. Теория ингибиции (сдерживания) утверждает, что старые люди становятся менее умелыми в связи с осложнениями восприятия внешней информации и поэтому они концентрируются на выполнении более простых задач. Согласно теории отказа, интеллектуальные способности в пожилом возрасте ухудшаются вследствие недостаточного их использования в процессе деятельности. Другой вариант когнитивной теории, связанный с персональными аспектами старения: речь идет об основных способах интерпретации людьми преклонного возраста собственных возрастных изменений. При этом главное значение имеют три сферы: личные переживания (ухудшение самочувствия, уменьшение физической привлекательности), особенности социального статуса (активное привлечение, интеграция или изоляция), а также осознание конечности собственного бытия.
Самое современное направление в решении теоретических аспектов проблемы — это комплексные теории старения. Процесс старения является чрезвычайно многогранным и включает биологические, социальные и психологические составляющие, которые тесно связаны между собой. Дж. Тернер и Д. Хелмс выделяют три взаимосвязанные и взаимозависимые процесса старости:
1) психологическое старение — особенности осознания и отношения индивида к процессу своего старения при сравнении его со старением других людей;
2) биологическое старение — биологические изменения организма (инволюция);
3) социальное старение — особенности исполнения социальных ролей, связь старения с обществом.
В теоретической модели П. Балтеса подчеркивается, что процесс развития детерминирован сложным взаимодействием ряда факторов: внешнего (социальной среды), внутреннего (биологического) и синтеза биологического и социального. Эти факторы задают три направления развития: нормативное возрастное, нормативное историческое и ненормативное развитие жизни. Нормативное возрастное развитие связано с последовательным переходом от одного возрастного этапа к другому в биологическом (начало пубертатного периода или менопаузы) и социальном (влияние выхода на пенсию на поведение) аспектах старения. Нормативное историческое развитие происходит в контексте тех глобальных социально-исторических событий, которые переживают представители целого поколения. Ненормативное развитие жизни обусловливается влиянием событий, которые являются уникальными в жизни конкретного индивида (сыграть главную роль в фильме, получить Нобелевскую премию и т.п.). По мнению автора, степень влияния данных факторов отличается в разные возрастные периоды. В преклонном возрасте наибольшее влияние имеют нормативные возрастные факторы; кроме того, важно учитывать особенности ненормативных личных событий. Модель П. Балтеса дает возможность выделить типичные моменты развития разных людей, общие для конкретных поколений и специфические в жизни отдельного индивида.
Развитие психики не завершается в период юности. Определенная динамика психического развития отмечается и в более позднее время, поэтому в современной психологии принято выделять еще два периода: акмеологический период развития, или период взрослости, и период геронтогенеза. Специфику возрастного характера определяют следующие условия: физиологические; психологические (индивидуальные личностные особенности, уровень знаний, мышления); социальные (особенности условий жизни и требований общества, особенности взаимоотношений с окружающими). Возраст можно определять по хронологическим, биологическим или психологическим признакам, причем не всегда обнаруживается жесткая связь между психологическим возрастом и данным метрического свидетельства.
Попытки увеличения продолжительности жизни
На основе существующих теорий старения основным направлением исследований по геронтологии (так называемая биомедицинская геронтология) являются попытки увеличения продолжительности жизни, особенно человека. Заметное увеличение продолжительности жизни уже происходит в глобальном масштабе с помощью таких факторов, как общее улучшение медицинского обслуживания и повышение уровня жизни. На уровне индивидуума увеличение продолжительности жизни возможно за счет определенной диеты, физических нагрузок и избегания потенциально токсичных факторов, таких как курение. Тем не менее преимущественно все эти факторы направлены на преодоление не старения, а только «случайной» смертности (член Мейкхама в законе Гомпертца — Мейкхама), которая уже сегодня составляет небольшую долю смертности в развитых странах, и таким образом этот подход имеет ограниченный потенциал увеличения продолжительности жизни. Вопрос, следует ли увеличивать продолжительность жизни, сегодня является вопросом многочисленных дебатов на политическом уровне, а основная оппозиция преимущественно состоит из представителей некоторых религиозных конфессий. Ряд общественных (РТД, WTA) и религиозных (раэлиты) организаций активно выступает в поддержку работ по значительному увеличению продолжительности жизни человека. Под руководством Михаила Батина и Владимира Анисимова разрабатывается комплексная программа исследований «Наука против старения». В 2017 г. ученые из Университета штата Аризона Пол Нельсон и Джоанна Мазель, чья статья была опубликована в журнале Proceedings of the National Academy of Sciences, показали, что с математической точки зрения старение неизбежно, т.к. даже если создать для организма идеальные условия, в нем все равно будут накапливаться или злокачественные, или нефункциональные клетки, приводящие к смерти.
Существует несколько возможных стратегий, за счет которых исследователи надеются уменьшить скорость старения и увеличить продолжительность жизни. Например, продолжительность жизни увеличивается до 50% в результате ограничения калорий в диете, которая в общем остается здоровой, у многих животных, включая некоторых млекопитающих (грызунов). Влияние этого фактора на продолжительность жизни человека и других приматов пока еще не обнаружено, известных данных все еще недостаточно, и исследования продолжаются. Тем не менее на данный момент значительный успех все еще не достигнут и, как считает большинство геронтологов, неизвестно когда — через годы или десятилетия — произойдет значительный прогресс в этой отрасли.
Глава 5. В поисках системообразующего начала процесса старения человека
Данные о большом количестве современных научных теорий и научно-методологических подходов к изучению проблем старения, долголетия и возникновения фатальных болезней цивилизации, представленные в главе 4, показывают, что в настоящее время реального решения этих очень сложных и практически тупиковых научных проблем пока так и не найдено. Наличие существования более 300 научных теорий старения говорит лишь о том, что ни одна из них не отвечает на фундаментальные вопросы современной науки, не позволяет предотвратить старость, создать практические технологии борьбы со старением и реально увеличить активное долголетие человека. По-видимому, это скорее связано с существующим фундаментальным недопониманием учеными биологической сущности процесса старения, чем действительно с неразрешимым тупиком в науке о старении. До настоящего времени нет полной ясности в понимании базовых системообразующих механизмов возникновения старения. Нет объяснения различий скорости и динамики процесса старения у каждого конкретного человека. Нет четкого понимания существующих в обществе определенных лимитов и ограничений наших собственных научных представлений на проблему старения. Возможно, как только мы поймем системные и информационные основы возникновения и молекулярно-биологической машинерии процесса старения, мы совершим серьезный научный прорыв в этом направлении. И для этого у нас уже практически все есть!
В настоящее время мы владеем уникальными знаниями об устройстве генома человека. Нам известны все пути сигнальной трансдукции в соматической клетке. Мы знаем фундаментальные основы молекулярной биологии и понимаем механизмы межклеточного взаимодействия клеточных систем. Для нас не являются секретом очень глубокие фундаментальные знания о роли и месте стволовых клеток в организме человека. Но при этом, говоря о старении, мы снова готовы повторить слова английского биолога проф., сэра Peter Brian Medawar, сказанные перед Лондонским королевским обществом в 1951 г.: старость — An unresolved Problem in Biology («Нерешенная проблема биологии») (Medawar, 1952). Но сегодня мы бы добавили к этому высказыванию сэра P.B. Medawar свое важное дополнение. Старение — это не только нерешенная проблема биологии, но и величайшая дилемма современной медицины. По существующим научным представлениям, старение — это не столько запрограммированный биологический инволюционный процесс деградации живого организма, приводящий к смерти, сколько системное возрастзависимое молекулярно-биологическое (геномное, эпигеномное и постгеномное) заболевание клеток органов и тканей организма всех живых существ (Брюховецкий А. С., Брюховецкий И. С., 2020). Поэтому поиск решения этой не только биологической, но и важной медицинской проблемы — вот главный вызов, поставленный всему человечеству и всей современной биомедицинской науке, и он настоятельно требует своего незамедлительно решения уже в нач. XXI века.
Как мы видим из предыдущей главы, существует большое разнообразие методологических подходов и теоретических воззрений на возникновение процесса старения и бесконечное количество теорий, объясняющих механизмы его формирования и причины его завершения смертью. Нам было очень важно разобраться и понять суть фундаментальных базовых представлений, которые лежат в основе того или иного научного подхода или той или иной научной теории старения, поскольку специфика осмысления данного феномена определяет спектр теоретических вопросов и основные пути решения многочисленных практических проблем, связанных с процессом старения.
Известно, что правильно поставленный вопрос уже содержит в себе правильный ответ или его часть! Но как четко и точно нужно сформулировать вопрос, чтобы сразу же получить на него правильный ответ? Очевидно, что при наличии такого большого разнообразия и разнонаправленности существующих научных фактов, экспериментальных данных и теоретических взглядов и различных методологических подходов ученых во всем мире к проблеме старения, а также уже полученных фантастических результатов увеличения продолжительности жизни у модельных животных (у мыши — в 2,5 раза, у дрожжей — в 15 раз, у нематоды — в 10 раз) и при явном отсутствии реальных практических результатов от клинического применения данных достижений в современной геронтологии на человеке есть только один научно-методологический путь решения проблемы. Этот путь заключается в том, что необходимо попытаться найти между всеми уже известными научными фактами, практическими явлениями и экспериментальными наблюдениями за процессом старения, а также всеми существующими научными теориями старения что-то общее, системообразующее, связывающее и интегрирующее их между собой. Это «что-то» должно позволить объединить все известные экспериментальные и научные факты и теоретические воззрения на проблему старения и возникновение возрастзависимых болезней в единый интегральный трехмерный взаимосвязанный медико-биологический, формирующийся во времени и пространстве и формируемый феномен, определяемый термином «системная биология старения». Возможно, что правильный ответ на этот вопрос будет содержать в себе объяснение большинства уже известных научных фактов и экспериментальных данных о старении и долголетии и просто расставит их на свои места в этом временном континууме событий жизни человека и животных. Вероятно, что ответ на этот вопрос лежит где-то рядом, на виду, но мы просто его не видим или не замечаем из-за его очевидности. Каждая из существующих современных теорий старения человека несет в себе его структурную частичку и системообразующую часть той научной правды, которую в разное время и в разных частях света обнаружили различные ученые и исследователи во время своих экспериментов и наблюдений процесса старения за многие годы накопления предшествующих знаний. Напрашивается достаточно банальный вывод о том, что мы явно не замечаем чего-то очень очевидного и простого, что давно лежит на поверхности перед нашими глазами, и именно из-за этого мы еще не открыли фундаментальных механизмов этого важного научного явления! Более того, мы убеждены, что фундаментальные законы старения уже открыты и глубоко изучены для объяснения определенных сторон старения, просто никто не решается масштабировать их на всю системную биологию и информациологию процесса старения. Именно поэтому ни одна из известных теорий старения не позволяет нам дать исчерпывающие ответы на основные фундаментальные научные вопросы проблемы старения и долгожительства. Именно раскрытие этих системообразующих и взаимозависимых молекулярно-биологических механизмов старения помогло бы понять глобальную фундаментальную и биологическую сущность процесса старения и обеспечить базовые медико-биологические основы реального долголетия человека.
Мы не будем в этой монографии пытаться критиковать, осуждать или выделять из существующего большого количества научных теорий, известных научных фактов о старении и теоретических концепций об активном долголетии наиболее яркие, наиболее документально доказанные и запротоколированные научные исследования, а, наоборот, подчеркнем достоверность, нужность, необходимость, правильность, технологичность и экспериментальную очевидность и ценность каждого из них для нашего осмысленного и целостного понимания всей этой проблемы. Научные факты и экспериментальные доказательства, представленные как отечественными, так и преимущественно зарубежными учеными, в большинстве этих научных теорий очень убедительные, научно и экспериментально обоснованные и не вызывают сомнений. Почти каждый научный факт этих теорий настолько интересен и наукоемок, что сам претендует на самостоятельную научную теорию, что́ мы и видим на практике. Именно поэтому каждый из ученых, изучавших процесс старения, увидев что-то на его взгляд очень важное и необычное в процессе биологии старения, ставит его на первое место и формирует вокруг него свою теорию возникновения старения. Но, на наш взгляд, все-таки это не причины, а очевидные и закономерные следствия и взаимозависимые биологические этапы системного процесса, называемого биологией старения. Это составляющие молекулярные компоненты и биологический инструментарий одной очень большой, многогранной, растянутой во времени, мультисистемной молекулярно-биологической возрастзависимой болезни организма человека и животных, приводящей к морфологическому увяданию, функциональной дезинтеграции и формированию различных органических поломок и дефектов органов и тканей организма, приводящих к угасанию жизни и последующей смерти.
По-видимому, нам сегодня практически не нужны новые научные факты о старении! Вряд ли мы сделаем какие-то новые фантастические открытия и найдем что-то чудесное и принципиально новое, чего мы сегодня еще не знаем. Мы знаем о старении и обо всех молекулярных процессах, сопровождающих и формирующих этот медико-биологический феномен у человека и животных, так много, что вряд ли найдем что-то такое, что нам еще вообще неизвестно. О биологии и медицинских аспектах старения написаны горы книг, содержащих фантастические объемы информации, которые мы даже неспособны целиком прочитать, понять и переосмыслить. Нам нужно очень внимательно и методично систематизировать уже имеющиеся у нас экспериментальные, научные и теоретические данные о старении и свести их в определенную иерархию информационных взаимоотношений, взаимодействий и взаимосвязей. Для поиска истины нам нужна принципиально новая, объединяющая и интегрирующая уже все имеющиеся научные факты теория старения, которая позволит понять, что является «системообразующим началом» в запуске системной биологии процесса старения, его роль и участие в поддержании и неуклонном прогрессировании этого процесса, приводящего к инволюции и завершающегося смертью человека и млекопитающих. Только тогда, с этим новым методологическим и теоретическим пониманием проблемы старения, можно будет найти адекватное решение проблемы увеличения продолжительности жизни человека и других млекопитающих и решить проблему активного долголетия на уровне молекулярной биологии.
Все, что нам нужно сегодня, так это новое понимание того, как начинается старение! Нужно осознать молекулярно-биологический механизм возникновения и поддержания процессов системной и молекулярной биологии старения и понять механизмы управления процессами программного самообновления. Мы убеждены, что все фундаментальные аспекты проблемы старения уже изучены вдоль и поперек и все основные молекулярно-биологические «пазлы» этой биологической конструкции и необходимый инструментарий уже давно найдены. Мы достаточно много знаем о старении, но очень мало понимаем суть данного явления! По-видимому, само явление начала процесса старения пока находится вне поля нашего зрения или мы просто его не замечаем из-за его обыденности, очевидности или простоты! Но именно фундаментальным «системообразующим началом» старости и нужно попытаться заняться в первую очередь, чтобы ответить на главные вопросы: где, когда и почему возникает и неуклонно углубляется процесс старения в организме? Это ключ к пониманию патогенеза и всей машинерии столь сложных молекулярно-биологических и функционально-морфологических системных процессов перехода от развития, роста, пролиферации и дифференцировки в молодом возрасте к процессам апоптоза, деструкции, дегенерации, атрофии, дистрофии органов и тканей при старении человека. И именно это «системообразующее начало» позволит разработать и создать новую теорию старения, которая объединит все эти разрозненные «пазлы» научных фактов и экспериментальных данных в целостную картину многомерного и многопараметрического процесса старения.
Давайте попробуем систематизировать накопленные многолетние знания о роли основного «системообразующего начала» в процессе старения не как естественного биологического и патофизиологического процесса увядания организма, приводящего смерти, а как этиопатогенеза системной возрастзависимой болезни организма человека и животных. Ведь не мы первые из ученых назвали старение болезнью, зависимой от возраста, задались этим вопросом и попытались дать на него ответ.
Вопросы системной биологии старения, механизмы запуска и мониторинга процессов молекулярной биологии старости уже давно интересуют ведущих ученых во всем мире. Еще в позапрошлом веке, в 1896 г., французские ученые Клод Бернар и Рене Лериш (основоположник сосудистой хирургии), описывая «вегетативную жизнь тканей человека», подметили одну очень важную научную закономерность, заключающуюся в том, что дегенеративная болезнь органов и тканей и старение тканей, а также опухоли в большинстве случаев возникают в тканях не в один день, а формируются многие годы и (или) даже десятилетия жизни человека до появления клинической симптоматики проявлений самой болезни (Лериш, 1965). Они также обратили внимание на то, что при этом в некоторых других наблюдениях время от момента действия этиологического фактора до исхода болезни сокращено до предела и исчисляется неделями или месяцами. Они показали, что основными причинами большинства возрастных болезней человека являются малозначительные микротравмы тканей и микроповреждения мелких суставов, микроповреждения органов и тканей давностью более чем в 20–30 и даже 40 лет, а также незначительные заболевания, перенесенные когда-то в легкой форме, много лет назад и впоследствии приведшие к тяжелым негативным и деструктивным, дегенеративным и атрофическим изменениям в тканях, железах внутренней секреции и органах организма. Они первыми в мире заговорили о наличии системных механизмов старения и возрастных изменений органов и тканей человека как болезни. Эти французские ученые считали, что, возможно, этим «системообразующим началом» старости, дегенерации и атрофии органов и тканей является нарушение обеспечения вегетативной нервной системой локальной автономной иннервации участков ткани, т.к. именно она имеет свою централизованную и селективную биологическую представленность во всех органах и тканях организма и даже присутствует в нервной ткани мозга человека. Они полагали, что повреждение автономной вегетативной иннервации в локальных участках органов и тканей является главной причиной нарушения контроля и надзора над ними на периферии организма. Они описали удивительные феномены пикноцитоза, жирового перерождения и дегенерации вставочных клеток в узлах симпатической и парасимпатической автономной (вегетативной) нервной системы (АНС) как биологической и морфологической основы старения органа.
Другими словами, понимание повреждения системы АНС как причины старения формально является сильной и перспективной научной позицией, т.к. оно позволяет рассматривать «системообразующим началом» морфологические изменения в симпатических и парасимпатических ганглиях, непосредственно приводящие именно к формированию локальной (местной) патологической денервации органов и тканей человека как фундаментальной причине их инволюции и дегенерации при отсутствии контроля над ними центральных нейрональных компонентов ЦНС. Это системообразующее начало в АНС позволяет объяснить возникновение дисбаланса и дисрегуляции биоуправления в тканях и органах человека в результате нарушения вегетативной денервации определенных участков ткани, при его бесконтрольности со стороны ЦНС и возможности безудержного роста и пролиферации. Или, позволяет объяснить изменения как морфологическую основу тотальной дегенерации и атрофии ткани в связи с устранением централизованного мозгового контроля над периферическими тканями организма. Именно эта теория позволила в начале прошлого века описать медленное и постепенное формирование процессов ишемии, дегенерации и атрофии ткани органа при параличе иннервации кровоснабжающего его сосуда и формирования патологической извитости (кинкина) в зоне денервации сосуда. Эти наблюдения и их теоретическое переосмысление позволили Рене Леришу (1905) предложить технологию симпатэктомии (удаление симпатического вегетативного узла) как способ восстановления локального кровотока при местных денервационных поражениях сосудов головы и шеи в сосудистой хирургии.
Казалось бы, французскими учеными было найдено столь важное «системообразующее начало» в форме повреждения морфоструктурных компонентов АНС, формирующее старение, дегенерацию и атрофию органов и тканей. Эти изыскания привели к модному нынче термину, описывающему комплекс дегенеративно-атрофических процессов в мышечных тканях пожилых людей, характерных для старения, в виде болезни саркопении. Диагноз саркопения — это относительно новый термин, который начал применяться в медицине с 1989 г. С его помощью описывался процесс потери массы скелетной мускулатуры, связанный со старением. В 2010 г. был пересмотр терминологии, и на сегодняшний день определение звучит следующим образом: «Саркопения — это снижение мышечной массы и ее функциональных характеристик, которое развивается из-за нейрогуморальных сдвигов, нарушения питания или разрушения мышц в результате процессов катаболизма». С сентября 2016 г. саркопения была официально включена в МКБ-10 и ей был присвоен код М 62.84. В медицинской практике саркопения является важным прогностическим маркером при определении прогноза жизни и выздоровления, особенно у тяжелых больных. Объем потери мышечной массы имеет прямую связь с полиорганными нарушениями. Если потеряно ~ 5–10% мышечной массы, нарушается работа одного органа, 10–20% — двух-трех органов, и если потеряно более 20% мышечной массы, нарушается работа четырех и более органов.
Но при ближайшем рассмотрении становится очевидно, что роль АНС в формировании старения не первична, а тоже вторична, т. к. АНС полностью подчинена ЦНС. В идеале АНС полностью контролируется и управляется ЦНС. АНС имеет очень серьезную систему дублирования и защиты в ЦНС. Особенность феномена верховного контроля ЦНС над АНС была наглядно показана в работах великого советского нейрохирурга проф., д.м. н. Андрея Львовича Поленова в 50–60-х гг. прошлого века, где он продемонстрировал многоступенчатость, высокий уровень дублирования функций и наличие высоких степеней защиты в АНС. В то же время профессор А. Л. Поленов очень наглядно проиллюстрировал, что наличие локальных повреждений в ЦНС приводит к локальным изменениям в АНС, которую она контролирует. Существует целый ряд факторов, на которых мы не будем подробно останавливаться в этой книге, которые позволяют исключить повреждение периферической нервной системы как основной механизм запуска процессов старения, инволюции и увядания организма человека. На наш взгляд, роль денервации автономной вегетативной нервной системы в процессах старения действительно вторична относительно процессов, происходящих в ЦНС.
Хотя старение мозга является одним из важнейших феноменов, усиливающих системную дегенерацию органов и тканей, и приводит к нарушениям когнитивных функций, снижению памяти, снижению функциональности и адаптированности человека к окружающей среде и экстремальным воздействиям внешнего мира, оно полностью зависит от функционального состояния ЦНС человека. С другой стороны, функциональность ЦНС абсолютно критично зависима от сосудистой (кровеносной) системы организма и даже незначительные повреждения в ней приводят к несоразмерным повреждениям в органах и тканях (острая и хроническая ишемия) и смерти организма вообще и мозга в частности. Очевидно, с одной стороны, что нейроны нервной ткани человека могут жить до 1 тыс. лет (Галушкин, 2012), но, с другой стороны, клетки коры головного и спинного мозга человека умирают первыми даже при кратковременной гипоксии мозга, в пределах 10–15 мин, что проявляется клинической смертью и смертью коры головного мозга. Даже 10% мотонейронов, сохраненные в процессе дегенеративно-дистрофической болезни (напр., при боковом амиотрофическом склерозе), позволяют человеку ходить, т.е. не влияют на его моторную функцию. Поэтому ЦНС тоже не может претендовать на роль «системообразующего начала» в формировании старости, но при этом роль повреждения, дегенерации и атрофии клеток ЦНС в старости достаточно значима и усугубляет общий процесс старения значительно.
Претендентом на системообразующее начало в формировании старения в организме человека теоретически могла бы быть сердечно-сосудистая система, состоящая из большой сети кровеносных сосудов (артерий и вен) и, конечно же, сердца. О роли сердца и сосудов в процессе старения не следует забывать. Очевидно, что органом, обеспечивающим центральное системообразующее механическое взаимодействие всех структурных и функциональных компонентов организма человека и млекопитающих, является именно сердце. Этот орган задает постоянство (константу физических параметров гомеостаза) и регулярность сокращений всех органов (биологический ритм и циркадность), а также обеспечивает иерархию взаимодействия и протекания всех биофизических и химических процессов. Однако центральная роль сердца и сосудов в регуляции процессов старения достаточно ограничена и сомнительна. Чаще процесс старения сам повреждает сердце и коронарные сосуды в виде системного склерозирующего атеросклероза. В этой связи сердечно-сосудистая система не может претендовать на главный системообразующий фактор, интегрирующий все системы организма человека. Несмотря на то что атеросклеротическое поражение сосудов сердца, грудного и брюшного отделов аорты и атеросклероз сосудов головного мозга — это неотъемлемые атрибуты старости и есть почти у каждого пожилого человека, вряд ли это все же первичные признаки, определяющие старость. В большинстве случаев старение действительно сопровождается системным атеросклеротическим поражением всех сосудов сердца и других органов человека, но атеросклероз — это не причина старения, а скорее его проявления и исход. Именно системный атеросклероз и есть фундаментальный системообразующий механизм, запускающий уже идущий процесс старения организма человека, усугубляющий его и делающий необратимым. Кровеносная артериальная и венозная система — это всего лишь прекрасная биологическая транспортно-логистическая система, которая имеет представленность во всех органах и всех «потаенных уголках» тканей нашего организма. Центральной функцией кровеносной системы человека является обеспечение питания различных органов и частей организма путем переноса кислорода, питательных веществ и сигнальных молекул и т. д. То есть сердечно-сосудистая система — это важный инструментарий для обеспечения работы всех клеток различных органов и тканей, но нарушения в ее работе не могут быть фундаментальной причиной возникновения и прогрессирования процесса старения человека. Сосуды, так же как и сердце, большая мишень глобального процесса старения, как и нервные клетки ЦНС и АНС.
Эндокринной системе человека и животных всегда приписывалось важное системообразующее значение в возникновении и прогрессировании процесса старения в организме млекопитающих и человека. Роль эндокринных возрастных изменений гипоталамо-гипофизарной системы, дегенерации вилочковой железы и других желез внутренней секреции очевидна и достаточно понятна, но, на наш взгляд, она также вторична, а не является пусковой и определяющей в процессе старения. Эндокринные возрастные сдвиги у человека существенно меняют его уровень гормонов («гормональное зеркало»), его функциональность и адаптационные возможности, но они — следствие, а не причина. Они — ответ на экстремальные экзогенные и эндогенные воздействия.
Существуют научные представления, что важнейшим системообразующим фактором старения является время! Ведь старение — это отчетливый возрастзависимый процесс. Так, есть радикальная точка зрения целой школы отечественных геронтологов и гериатров (Шабалин, 2012), что процесс старения начинается у человека с момента его рождения, и этому исследователи дают теоретическое обоснование. Но мы с этим утверждением категорически несогласны, т.к. это противоречит основам системной биологии. Все процессы отмирания, замещения и дегенерации части клеток и тканей у новорожденного происходят по четко заданной траектории и определенной генетической программе и направлены на совершенствование и точность формирования «запроектированной» в геноме протеомной формы органов и тканей, их соответствие существующим транскриптомным «чертежам» и генетическим «эскизам» моделируемого этими процессами видоспецифического фенотипа новорожденного человека. Поэтому концепция появления признаков старости сразу при рождении, на наш взгляд, несостоятельна и абсурдна. При естественном физиологическом процессе эмбриогенеза нет достаточного периода накопления критического количества дополнительных соматических мутаций (ДСМ) в клетках организма пациента и в его ГСК. Но, например, поражение матери и плода ионизирующей радиацией или хронической интоксикацией позволяет набрать нужное количество критических ДСМ достаточно быстро, и процесс накопления ДСМ, занимающий в естественных условиях 25–30 лет, может быть завершен в краткосрочном порядке за несколько минут. Но эти процессы критического накопления ДСМ в результате радиации и интоксикации не имеют ничего общего с физиологическим процессом старения, поэтому их роль в процессе старения ничтожна и несущественна.
С другой стороны, по-видимому, созидательные системные процессы роста, окончательной специфической дифференцировки и созревания органов и тканей организма, а также завершения процессов специализации функций всех высокодифференцированных клеток и тканей организма человека во времени в обычных естественных условиях являются завершающим этапом позитивного онтогенетического вектора развития. Это краеугольное событие жизни должно быть достаточно простым и понятным физиологическим явлением в процессе его жизни. Например, это могут быть завершение гормонального пубертатного периода полового созревания организма и высокая степень готовности его для продолжения своего рода. Другими словами, человек уже может начать стареть с появлением у него потенциальной возможности воспроизведения потомства и физической возможности продолжения собственного рода. Эта известная концепция «эгоистического генома», предложенная Ричардом Докинзом (1976), популяризует идеи, разработанные в 60-х гг. У. Д. Гамильтоном, смысл которых заключается в том, что цель каждого человека — удовлетворить потребность выживания его собственного генотипа. Как только у индивидуума появляются потомки, несущие его геном, его жизнь для всего мира в рамках данной концепции теряет всякий смысл, т.к. его «эгоистический геном» удовлетворен и он продолжит свое земное существование. С позиций продолжения рода возможность у индивидуума рождения потомства и передачи своего генетического материала детям обесценивает жизнь самого этого индивида, и якобы теряется смысл его существования, т.к. главная функция его организма может быть реализована просто путем передачи своего генетического материала потомкам. То есть с этих позиций половое созревание (11–14 лет) и способность к продолжению рода является Рубиконом, при переходе которого в организме млекопитающих могут наступать процессы жизнедеятельности с обратным (отрицательным) знаком, сопровождаемые инволюцией и дегенерацией, которые становятся началом вхождения организма в онтогенетический вектор старости. Но что физически должно произойти в организме человека, чтобы так кардинально, на 180 градусов, поменять вектор его системного развития с созидательного и животворящего на разрушительный и деструктивный? Неужели именно половая жизнь запускает информационные процессы старения? Но история знает массу примеров, когда половая жизнь у людей физически отсутствовала весь период их жизни, но это не отменяло их старения, увядания и наступления смерти. И наоборот: очень рано начатая половая жизнь абсолютно не влияла на внешний облик человека и не способствовала его старению.
Что касается периодов возникновения процесса старения, то наиболее вероятно, что они определены единой генетической программой ядер основных регуляторных системообразующих клеток конкретного организма, а не всех соматических клеток органов и тканей. Вряд ли процесс старения запускается сразу после завершения периода полового созревания человека. И здесь системообразующую роль начинает играть иммунная система. Процесс полового созревания и созревания иммунной системы (ИС) ребенка характеризуется наличием критических периодов (КП). Знание КП становления иммунной системы делает понятным скачкообразный характер заболеваемости в различные периоды детства. Первый КП — период новорожденности (до 29-го дня жизни). Иммунная система находится в состоянии физиологической депрессии, носит пассивный характер (за счет материнских антител), с неразвитой системой фагоцитоза (клеточного захвата и уничтожения микробной флоры). У ребенка имеется склонность к генерализации микробно-воспалительного процесса, сепсису. Второй КП (3–6 мес.) — ослабление пассивного гуморального иммунитета в связи с уменьшением материнских антител. На антигены развивается активный первичный иммунный ответ с образованием IgM, не оставляющих иммунологической памяти. Проявляется недостаточность системы местного иммунитета, что выражается в повторных ОРВИ. Проявляются наследственные иммунодефициты, пищевая аллергия. Третий КП — 2-й год жизни; расширяются контакты с внешним миром. Иммунная система уже полноценно функционирует, активируются функции лимфоцитов, есть достаточное количество IgG, формируется собственный долговременный иммунитет. Но по-прежнему сохраняется дефицит местного иммунитета, что приводит к частым ОРВИ. Первые 3 КП характеризуются низкой сопротивляемостью по отношению к инфекциям. Острые тонзиллиты у детей 2 лет жизни на 80% связаны с вирусами, а из бактерий преобладает стафилококк. Аденоидиты и тонзиллиты носят рецидивирующий характер, что приводит к гиперплазии (разрастанию) миндалин (это к вопросу, откуда берутся часто болеющие дети). Четвертый КП — 4–6-й годы жизни. Синтез антител, кроме IgA, достигает величин взрослых, повышается уровень IgE. Система местного иммунитета еще до конца не сформирована. Начинают проявляться наследственные дефекты иммунной системы. Половые гормоны, синтезируемые в этот период, угнетают иммунитет. Развиваются аутоиммунные и лимфопролиферативные заболевания, повышается восприимчивость к микробам. Нарастает воздействие экзогенных факторов (курение). Это последний критический период развития собственной иммунной системы человека.
Период полового созревания стали связывать с началом старения в связи с процессами, происходящими в первую очередь в вилочковой железе человека. Известно, что (https://ru.wikipedia.org/wiki/%D0%A2%D0%B8%D0%BC%D1%83%D1%81) вилочковая железа (тимус) — небольшой орган розовато-серого цвета, мягкой консистенции, поверхность ее дольчатая. У новорожденных его размеры составляют в среднем 5 см в длину, 4 см в ширину и 6 мм в толщину, масса ~ 15 г. Рост органа продолжается до начала полового созревания (в это время его размеры максимальны — до 7,5–16 см в длину, а масса достигает 20–37 г). С возрастом тимус подвергается атрофии и в старческом возрасте едва отличим от окружающей его жировой ткани средостения; в 75 лет средняя масса тимуса составляет всего 6 г. По мере инволюции он утрачивает белый цвет и за счет увеличения в нем доли стромы и жировых клеток становится более желтым. Именно этот научный факт, говорящий о том, что размеры тимуса максимальны в детском возрасте, но после начала полового созревания тимус подвергается значительной атрофии и инволюции, и стали основой гипотезы, что после полового созревания наступает его инволюция и это действительно Рубикон начала старения. Дополнительное уменьшение размеров тимуса происходит при старении организма, с чем отчасти связывают понижение иммунитета у пожилых людей.
Основная роль тимуса — дифференцировка и клонирование Т-лимфоцитов. В тимусе Т-лимфоциты проходят селекцию, в результате чего в кровоток и ткани выходят клетки, которые могут вовлекаться в иммунный ответ против определенных чужеродных антигенов, но не собственного тела. Вырабатывает гормоны: тимозин, тимулин, тимопоэтин, инсулиноподобный фактор роста I, тимусный гуморальный фактор — все они являются белками (полипептидами). При гипофункции тимуса снижается иммунитет, т.к. снижается количество Т-лимфоцитов в крови. Инволюция тимуса разрушает основы первичного кроветворения и иммунитета растущего организма, заложенные при рождении, и передает все функции кроветворения гемопоэтическим стволовым клеткам костного мозга. Именно этот феномен полного перехода от смешанного (тимус-ассоциированного и костно-мозгового) гемопоэза к исключительно костно-мозговому кроветворению знаменует собой начало процесса старения человека. По-видимому, в этот период меняется вектор развития организма с позитивного на отрицательный или негативный. Но на самом деле это неверно, т.к. история орнитологии подтверждает, что инволюция бурсы у воронов в 100 лет никак не сказывается на процессе их старения и смерти в возрасте 300 лет и более.
Таким образом, формирование начала старости в подростковом возрасте маловероятно, т.к. половое созревание начинается в среднем в возрасте 11–12 лет и заканчивается в течение 5–6 лет. Половые гаметы уже в 11–13 лет способны дать нормальное потомство при оплодотворении, но процессы формирования его вторичных половых признаков, роста головного и спинного мозга и формирования психического развития еще не завершены до 18–20, а то и до 25–30 лет. В возрасте 11–13 лет идет процесс формирования нейросоматических «ножниц»: соматически тело готово к продолжению рода и оплодотворению гамет противоположного пола при несозревших вторичных половых признаках и полном психическом инфантилизме, а также невозможности самостоятельного выживания и самообслуживания в экстремальных условиях в неблагоприятной окружающей среде и социуме. Еще более 8–10 лет нужно организму человека, чтобы стать самостоятельным индивидуумом, способным выжить в экстремальных условиях окружающей среды и агрессивного социума. Его тело продолжает увеличиваться и развиваться в формах и размерах до генетически запрограммированного фенотипа своего вида до 25–30 лет, постоянно меняются его гормональный фон и иммунная система, видоизменяется его психическое осознание себя в окружающем мире и социуме. Показано, что существуют определенные скачкообразные колебания «гормонального зеркала» (гормонального фона) в возрасте от 12 до 25 лет, когда тимус функционирует достаточно активно. В этом возрасте тимус и костный мозг обеспечивают активную выработку в корковом слое тимуса и костном мозге ГСК, т.к. наличие достаточного количества ГСК крайне необходимо организму для его дальнейшего роста и развития, и вероятность возникновения ошибок и сбоев при митозах такого большого количества делящихся и пролиферирующих клеток при столь активном процессе роста и развития соматики и психонейросоматики организма подростка требует очень жесткого контроля со стороны главного регуляторного инструмента иммунитета человека — собственных ГСК.
Существует мнение, что более обоснованным генетическим Рубиконом перехода к старости является период окончательного завершения процесса роста организма человека. Именно с этого времени якобы начинается генетически запрограммированная инволюция вилочковой железы и ее дисплазия, которая манифестирует полным прекращением формирования в ней новых ГСК. С этого периода ГСК имеют ограниченный режим клеточных делений. Именно с этого времени не происходит постоянного добавления извне новых ГСК в костный мозг. Это обусловлено прекращением их созревания в тимусе и остановкой постоянной миграции из вилочковой железы. ГСК лимфоидного ряда начинают производить созревающие T-лимфоциты исключительно в костном мозге, а процесс образования и созревания гемопоэтических стволовых и прогениторных клеток макрофагального ряда из тимуса переносится постепенно в лимфатические узлы, где далее и образуются типичные макрофаги, дендритные и интердигитирующие клетки.
Известно, что животные-долгожители (гренландские акулы — 400 лет, голопогосские черепахи — 300 лет, голубые киты — 200 лет и т.д.) прирастают в размерах понемногу весь период своей жизни, и считается, что эти факты подтверждают научные воззрения о том, что старость начинается после завершения роста человека. Есть мнение, что именно гормоны роста являются основными «дирижерами» процессов биологического строительства и совершенствования мозга и тела человека, но объективного научного обоснования и доказательного подтверждения этому явлению нет. Нет и реальных экспериментальных доказательств этого феномена со стороны современных нейроэндокринологии и геронтологии. Все системы жизнеобеспечения организма, солидные и эндокринные органы человека, достигнув генетически детерминированных размеров и формы, больше не нуждаются в нейрогормональной стимуляции роста и получении дополнительного белкового биоматериала (РНК, ДНК, протеинов) для построения новой ткани органов и систем, т.к. полученный образец полностью соответствует запрограммированному эталонному образцу «эскиза», имеющемуся в его геноме, и существующему «чертежу» профилей экспрессии РНК всех клеток организма, хранящемуся в его транскриптоме. Все профили экспрессии ДНК клеток и профили протеомного картирования белков этих органов и систем при завершении роста человека уже достигли нужной экспрессии генов и нормализованной сигнальной интенсивности белков. То есть по окончании процесса роста протеом организм пришел к нужному фенотипу взрослой особи данного вида и других изменений не требуется. Чтобы остановить биохимический и биофизический процесс созидания и строительства растущего организма на уровне достигнутого фенотипического образца, совпадающего с генетическим и постгеномным кодом данного индивидуума, нужно остановить всю информационную и строительно-монтажную работу клеток и тканей организма, и это должен быть очень мощный информационный стимул, способный полностью переломить всю существующую молекулярно-биологическую машинерию организма человека в обратную сторону. Другими словами, это должно быть почти информационно-волновое цунами! По-видимому, точка приложения этого стимула заложена в программе генома наших соматических клеток и включается путем информационного воздействия на него секретома клеток крови.
Возможно, что при достижении нужных фенотипических видовых форм и размеров этот стимул включается и изменяет экспрессию генов большинства пролиферирующих и дифференцирующихся клеток на экспрессию подавления их роста и развития, на включение программной клеточной гибели (апоптоза), инволюции и подавления процессов пролиферации и деления клеток. Является ли этот процесс автоматическим или осуществляется организмом в так называемом ручном управлении внешними стимулами, пока неясно. Но, с другой стороны, здравый смысл и сама жизнь подсказывают, что после достижения нормы и запланированной геномно-постгеномной реализации формирования протеомного фенотипа организма должен существовать гарантийный период его безаварийной эксплуатации и использования. Какой же гарантийный срок заложен нашим Создателем в нашем организме для оптимального функционирования? Ответа на этот вопрос пока не существует. Понимание фундаментальных информационно-коммутационных процессов, происходящих в органах и тканях, при переключении всех систем организма с многолетнего режима роста и развития на состояние покоя и последующий режим угасания, по-видимому, должно всегда сопровождаться цитокиновой «бурей» и мощными гормональными перестройками. При этом перевод экспрессии генов большинства клеток органов и систем при остановке роста человека в режим блокирования пролиферации и дедифференцировки должен сопровождаться снижением экспрессии РНК ответственными за это генами и системным подавлением смежных с ними генов. Значимость этого системного процесса должна быть достаточно очевидна как на гормональном уровне, так и на фенотипическом, но, скорее всего, протекает у каждого индивидуально. Как правило, процесс остановки роста завершается к 25 годам, и с этого возраста молодые люди начинают хорошо социализироваться в обществе, у них сглаживаются существующие акцентуации характера и даже имеющиеся расстройства личности, мешавшие им в подростковом возрасте. В некоторых случаях процесс завершения роста затягивается до 30–32 лет. Когда же кончается «гарантийный срок» биологического изделия под названием «живой организм» и начинается старость, мы не знаем и не понимаем. Где и как в организме человека разворачиваются эти информационные события в первую очередь, нам тоже пока непонятно. Возможно, этим запускающим старость инструментарием являются запрограммированная модуляция экспрессии генов транскриптома и гормональный всплеск, которым она сопровождается. Есть мнение, что в процессе жизни человека начиная с рождения идет повышение порога чувствительности гипоталамуса, что в конечном итоге после 40 лет приводит к гормональному дисбалансу и прогрессирующему нарушению всех видов обмена, в т.ч. гиперхолестеринемии. Поэтому бытует одно из мнений, что лечение болезней старости необходимо начинать с улучшения чувствительности гипоталамуса, т.к. именно он и его гиперчувствительность запускают гормонально-генетический и цитокиновый шторм, который и становится пусковым моментом начала старости человека. При этом остается непонятной и абсолютно не доказанной роль эндокринной системы как «системообразующего начала» процесса старения. Работы отечественных хирургов-андрологов под руководством акад. РАН, проф. И. Д. Кирпатовского из Российского университета дружбы народов по пересадке гипоталамо-гипофизарного комплекса на сосудистых связях молодых особей у старых животных и человека не выявили омоложения их органов и тканей (Кирпатовский, 2003).
Другие научные теории пытаются найти «системообразующее начало» патологического процесса старения в повреждении митохондрий в отдельных клетках организма человека и млекопитающих (митохондриальная теория старения), в повреждении теломер в хромосомах соматических клеток (теломеразная теория старения Оловникова) и т. д. К сожалению, пока все эти хорошо задокументированные и экспериментально установленные биологические причины и механизмы старости слишком локальны, чтобы претендовать на единый системообразующий и этиопатогенетический негативный системный «двигатель» старения и возникновения основных фатальных болезней цивилизации. Именно поэтому они не позволяют понять, как запускается и почему поддерживается весь механизм изнашивания и саморазрушения организма человека, приводящий к его смерти. При этом глупо отрицать, что снижение длины теломер хромосом клетки в десятки раз в результате частых делений клетки блестяще коррелирует с ее способностью к выживанию. Оказалось, что чем меньше длина теломерных участков ДНК, тем менее клетка жизнеспособна и выживаема. Но что приводит к этому системному эффекту укорочения теломер хромосом в клетке и митохондриальных нарушений в этой клетке, что является их первопричиной? Пока еще недостаточно ясно! Причинно-следственных взаимоотношений и взаимодействий этих очевидных молекулярных признаков старения клетки установить так и не удалось. Да и невозможно решить проблему борьбы с этими внутриклеточными возрастзависимыми нарушениями без понимания фундаментального «системообразующего начала» для их возникновения. Все молекулярно-биологические старческие изменения в клетке — это не причина, а следствие морфобиологического поворота на 180 градусов позитивного развития и регенерации в тканях и органах и начала формирования нового вектора движения, но уже в противоположном или, точнее, в отрицательном направлении. Этот так называемый биологический полицейский поворот в жизни каждого живого существа и развитие у него всех негативных молекулярно-биологических процессов в организме приводят к глобальной смене вектора созидания и развития клеток организма на вектор их разрушения, дегенерации и атрофии.
Абсолютно очевидно, что системообразующая роль иммунной системы в процессах старения и возникновения большинства болезней цивилизации просматривается при всех этих патологических процессах, и просматривается достаточно отчетливо. Старение и БЦ — это всегда иммуноассоциированные и иммуноопосредованные заболевания. При возникновении опухолей иммунная система толерантна к незрелым опухолевым клеткам и позволяет развиться опухоли, не препятствуя ей, что и становится основной причиной смерти организма. При аутоиммунных болезнях цивилизации роль иммунной системы в генезе и развитии этих заболеваний тоже более чем очевидна и понятна. Воспаление и аутоиммунный процесс разрушают организм и часто являются причиной смерти пациента от присоединения вторичных инфекций и иммунодефицитных состояний. При нейродегенеративных болезнях различной локализации также собственные иммунные клетки атакуют специализированные клеточные системы разных органов и приводят к их атрофии и дегенерации. Таким образом, роль иммунной системы в процессе старения является центральной и важнейшей. Это проявляется в иммунной недостаточности костного мозга и в невозможности формирования адекватного иммунного ответа. Недостаточность иммунной системы становится главной причиной смерти пожилых людей от банальных простуд, бронхитов и пневмоний. Очевидно, что именно «мертвая петля», которую формирует собственный иммунитет организма человека и животных, приводит к иммунотолерантности или иммунореактивности этой системы, которая убивает специализированные высокодифференцированные клетки других систем жизнеобеспечения организма или, наоборот, дает возможность развиваться генетически дефектным клеткам. Но на самом деле формирование «мертвой петли» собственного иммунитета тоже вторично, а не первично в генезе процесса старения. Коррекция пострадавшего иммунитета организма современными фармакологическими средствами не позволяет добиться результата и увеличить продолжительность жизни. Соответственно, патология иммунной системы вторична и только углубляет внутренний молекулярно-биологический дисбаланс, обусловленный «системообразующим началом» старения.
Таким образом, оценив роль почти всех систем организма в возникновении процесса старения, мы не находим в них первопричины возникновения всего комплекса типичных повреждений, свойственных пожилым и старым организмам человека и млекопитающих. Мы не получили ответа на самый главный вопрос: что запускает и поддерживает процесс старения и почему он возникает в принципе? Все выявленные нами феномены вторичны, и, несмотря на их системную представленность в организме, не они запускают процесс старческого повреждения систем, органов и тканей организма живых существ.
Итак, чего действительно так недостает во всех существующих научных теориях старения человека и млекопитающих, так это понимания того, что же могло бы запустить, объединить, постоянно поддерживать и неуклонно усугублять все эти столь многообразные динамические молекулярно-биохимические (генетические, протеомные, транскриптомные, секретомные, метаболомные и т.д.), биофизические (резонансно-волновые, атомарные, физиологические, нейрофизиологические, программно-кибернетические и т.д.), энергетические процессы инволюции в одном отдельно взятом организме человека или млекопитающего. Возможно, что только информационный подход, основанный на взаимодействии, взаимовлиянии и взаимозависимости этих информационных компонентов различных систем организма позволит объединить их все и увязать их взаимоотношения между собой. Информация — вот главный системообразующий фактор, который позволяет описать все взаимодействия компонентов различных систем, органов и тканей организма между собой в единое целое и определить его судьбу. Именно этим первичным системообразующим началом должен запускаться и поддерживаться столь длительное время весь генез патологического процесса старения. Именно его последствия должны являться причиной закономерной преждевременной смерти млекопитающего и (или) человека при фатальных болезнях цивилизации или, наоборот, определять долгую жизнь человека на Земле. При этом мы не пытаемся свести все имеющиеся факты к информационной теории старения, а говорим об информации как о фундаментальном инструменте познания природы и человека и базовом двигателе процесса старения. Все, о чем мы говорили выше, это грани и нюансы системного подхода в биологии и медицине, но они не позволяют сформулировать правильный ответ на поставленный нами вопрос.
Следует отметить, что бурное развитие информационных технологий в современной науке и технике выявило тенденцию отказа от системного подхода в точных науках (математике, физике, химии и т.д.) в указанном выше смысле и перехода к использованию информационного подхода как новой методологии научных исследований. Это обусловлено тем, что информационный подход показал явное преимущество по сравнению с системным, вероятностным, линейно детерминированным, синтетическим, материалистическим и другими подходами. Принцип информационного подхода заключается в том, что сначала производятся анализ и синтез не свойств вещей, предметов или их элементов, а отношений внутри них и их отношений с внешним миром. После классификации внутренних отношений свойств и их внешних отношений по признакам последних, анализируются и синтезируются свойства на базе (относительной) информации. Информационный подход не исключает системных закономерностей предмета исследований, они являются как бы автоматическим фоном, на котором развертываются внутренние и внешние сугубо информационные процессы. Но что такое информация и какой научный смысл мы вкладываем в это понятие? Информация — это фундаментальные отношения (полей, спинов, их следов и т.д.), проявляющиеся колебаниями (относящихся) частиц, частотами, электронами, фотонами, резонансами, осцилляциями, мгновенными излучениями. Информация проявляется электромагнитными, гравитационными и торсионными (спиновыми) полями, которые создают отношения, соотношения, взаимосвязи, взаимозависимости и взаимодействия между безмассовыми и массовыми виртуальными и гипотетическими частицами, которые определяются по определенному порядку — информационному коду, обеспечивающему этим частицам долговременную жизнь или мгновенный распад. В результате взаимодействия информационов создается информационно-сотовое пространство — волновое, резонансное, осциллирующее, колеблющееся относительно своего положения равновесия состояния электронов.
Трансфер информации невозможен без конкретного материального носителя, и на каждом информационном уровне он свой! Более подробно механизмы передачи информации в органах и тканях организма человека мы разбирали ранее на модели информационной структуры головного и спинного мозга (Брюховецкий А. С., 2014; Bryukhovetskiy A.S., 2016). Поэтому читателям, интересующимся этим процессом, рекомендуем обратиться к нашим ранним работам.
Информация является основным «пассажиром» для всех информационных носителей как на уровне организма, так и на уровне отдельно взятой клетки. На клеточном уровне существуют первичные носители информации. Так, на клеточном уровне индуктома (резонансно-волнового уровня, уровня элементарных частиц и атомарного уровня) ее носителями являются электромагнитные поля и электромагнитные волны, на уровне генома клетки ее носителем является ДНК, на уровне клеточного транскриптома носителем информации становятся различные типы РНК. На протеомном уровне клетки носителем информации выступают различные белки. При переходе на уровень метаболома клетки информационными носителями внутри клетки становятся различные жиры и углеводы, ферменты и энзимы. А на уровне секретома клетки носителями информации являются гормоны, медиаторы, факторы роста, нейротрофины и другие биохимические соединения, секретируемые клеткой (Там же). На межклеточном уровне появляются вторичные информационные носители (мессенджеры), которые структурно становятся более сложными, компактными и более информационно емкими. В качестве мессенждеров на межклеточном уровне выступают микровезикулярные транспортные системы по типу экзосом, эндосом, микровезикулярных пузырьков и т.д., которые осуществляют межклеточные взаимодействия между клетками определенной ткани и ее межклеточным матриксом, а также между клеточными системами других тканей и органов организма. Именно эти носители информации путем горизонтального (между соседними клетками ткани) и вертикального (между отдаленными клеточными системами разных органов) переноса первичных информационных носителей осуществляют основные межклеточные регуляторные взаимодействия и взаимоотношения. Этим путем осуществляется целенаправленная доставка всех жизнеобеспечивающих биологических веществ и сигналов между клетками внутри тканей и между органами для обеспечения их текущего выживания. Так, например, эритроцит переносит кислород до каждой клетки независимо от удаленности клеток и тканей организма от сердца, головы и всего туловища. Биологической информационной шиной для этого типа межклеточного взаимодействия являются в первую очередь кровь и другие биологические жидкости организма человека (лимфа, ликвор и т.д.). Микровезикулярная транспортная система межклеточного взаимодействия интегрирует в себе различные информационные носители (белки, углеводы, микроРНК, ДНК и т.д.), формируя из них информационные мессенджеры, или систему мгновенных межклеточных сообщений. Эти мессенджеры (экзосомы, эндосомы, микровезикулярные пузырьки и т.д.) обеспечивают межклеточный трансфер всех информационных носителей первого уровня, или так называемых первичных носителей информации. Информационным носителем третьего уровня являются собственно сами клеточные системы крови. Каждая клетка крови способна перенести определенную информацию и доставить ее адресату. Каждая клетка крови является информационной «дискетой», способной перенести данные на очень большие расстояния и высокоточно доставить нужному адресату в организме. Информационно-сотовое пространство, формируемое циркулирующими клетками крови, задает информационные параметры индуктомам (резонансно-волновым уровням, уровням элементарных частиц и атомарному уровню) всех стационарных высокодифференцированных клеток различных тканей и органов, прикрепленных к межклеточному матриксу ткани или строме органа или железы внутренней секреции. Эти клетки способны выполнять системные функции коммутации информации, защиты и обороны как отдельной ткани, так и всего организма в целом. Но главное их достоинство в том, что они создают физиологическую индуктивность всех тканей и органов организма человека. Именно индуктивность клеток крови заставляет работать все информационные уровни стационарных клеток, и именно поэтому наличие блока информации в этих клетках-мишенях при микротромбозе сосудов заканчивается смертью ткани органа. Мы намеренно не останавливаемся на обсуждении всех клеточных функций крови, чтобы не потерять нити наших рассуждений.
Как было отмечено ранее, в этой связи целесообразно рассматривать каждую клетку как самостоятельную информационную «дискету», способную перенести на себе любые первичные и вторичные данные. В клеточной иерархии есть клеточные системы, способные выполнять еще и системные функции управления и регуляции индуктивности ткани. При этом в одном случае они могут передавать информацию, которая запрограммирована генетически в их геноме, а в другом случае — выполнять надзорные функции защиты органа или всего организма человека, адаптируясь к изменяющимся внешним условиям. Например, натуральные киллеры (НК-клетки) и НКТ-клетки крови генетически приспособлены уничтожать чужеродные клетки, бактерии, вирусы, опухолевые клетки и т.д., т.е. клетки и живые организмы, имеющие чужеродные антигены. В других случаях клетка может формировать нужную для выживания организма информацию для других клеток, как это, например, делают дендритные клетки, поглощая патологические антигены и презентируя их на своей поверхности для обучения собственных цитотоксических лимфоцитов (ЦТЛ). В-третьих, клетка способна на основе информации, полученной от дендритных клеток, формировать новую информацию о персонализированных антигенах, имеющихся на патологических и чужеродных клетках, угрожающих здоровью организма, и моделировать ЦТЛ, способные убивать клетки с чужеродным антигеном. Эти функции выполняют свободно циркулирующие клеточные системы крови, не привязанные к определенной клеточной нише или межклеточному матриксу ткани или органа человека. Они постоянно находятся в циркулирующем объеме центральной и периферической крови и выполняют все тканевые функции крови в организме человека.
С позиций современной геронтологии и гериатрии роль и место кроветворной системы в процессе развития старения практически никогда не рассматривались исследователями как центральное, определяющее и системообразующее начало. Этой важной системе жизнеобеспечения организма преимущественно отводится второстепенная роль в процессах гомеостаза и репродукции клеток крови. Она сводится преимущественно к роли кроветворной системы организма, «заточенной» исключительно под непосредственное воспроизводство (репродукцию) клеток крови, и не более того! Но наш многолетний (более 30 лет) опыт изучения системы кроветворения у человека и млекопитающих и применения ГСК для лечения нервных и онкологических болезней в эксперименте и клинике заставил нас обратить внимание на центральную роль кроветворных стволовых клеток в регенерации органов и тканей, регуляции и управлении процессами саногенеза в органах и тканях, в поддержании гомеостаза организма, формировании врожденного и приобретенного иммунитета, организации систем иммунопоэза и гемопоэза, модерировании системы надзора и контроля за всеми процессами в организме.
Глава 6. Гемопоэтические стволовые клетки как молекулярно-биологическая системообразующая основа процесса старения
Одними из центральных научных представлений об информационном «системообразующем начале» процесса старения организма человека и животных могут стать наши взгляды на роль и место в формировании процессов старения ГСК млекопитающих и других СК костного мозга (Брюховецкий А. С., 2016). Ранее нами (Брюховецкий А. С., Брюховецкий И. С., 2020) было высказано достаточно парадоксальное мнение о том, что главными системообразующими и запускающими процессы старения и патогенез большинства фатальных болезней цивилизации являются постгеномные (эпигенетические, транскриптомные, протеомные, метаболомные и секретомные) изменения молекулярно-биологической структуры стволовых и прогениторных клеток системы кроветворения или системы гемопоэза (от лат. haemopoiesi — «кроветворный»).
ГСК — самые долгоживущие и практически «бессмертные» клетки в организме человека и животных. Именно в них в процессе жизни накапливается самое большое количество дополнительных соматических мутаций, что к 70 годам составляет более 1 млн ДСМ. Система кроветворения определяет необходимое и достаточное количество клеток крови и, главное, их функциональные и качественные молекулярно-биологические характеристики, обеспечивающие их потенциальные возможности для санации, управления саногенезом и регуляции иммунитета. Именно геномные и постгеномные характеристики ГСК крови определяют емкость, адекватность и достаточность информационно-коммутационного обеспечения между органами и тканями всего организма на всем протяжении жизни человека. В Википедии отмечено, что СК активно делятся и они имеют бо́льшую вероятность пострадать от накопления мутаций и утраты теломер, чем, например, высокодифференцированные клетки. Важным вопросом старения на уровне клеток и ткани является клеточный ответ на повреждения. Из-за стохастической природы повреждений отдельные дифференцированные клетки стареют, например в связи с достижением предела Хейфлика, быстрее остальных клеток. Такие клетки потенциально могут угрожать здоровью всей специализированной ткани. В наибольшей мере такая угроза проявляется именно среди стволовых клеток костного мозга и эпителия кишечника в связи с большим потенциалом таких тканей в создании мутантных и, возможно, раковых клеток. Известно, что именно СК этих тканей быстро отвечают на повреждения инициацией программы апоптоза. Например, даже низкие дозы радиации (0,1 Гр) вызывают апоптоз в клетках эпителия кишечника, а даже слабый химический стресс вызывает апоптоз стволовых клеток старых мышей. Как правило, в таких тканях массовый апоптоз является признаком возрастания числа повреждений клеток. С другой стороны, в других тканях ответом на возрастание уровня повреждений может быть арест клеток на определенной стадии клеточного цикла для прекращения деления (Kirkwood, 2005). Баланс между апоптозом и арестом поврежденных клеток наиболее важен как компромисс между старением и раком (Тyner et al., 2002). То есть или организм должен убить поврежденные клетки, или дать им возможность существовать, увеличивая риск возникновения рака. Однако, по современным представлениям, клетка стареет в результате накопления белковых повреждений. Скорость этого накопления устанавливается прежде всего генетически детерминированными затратами на ремонт и поддержку клеточных структур, которые, в свою очередь, определяются организмом для удовлетворения своих экологических потребностей.
Долгоживущие организмы имеют большие затраты (иногда более длительный метаболизм), что приводит к более медленному накоплению повреждений. Для борьбы с риском, который представляют собой поврежденные клетки, организм создал систему механизмов, которые часто включают второй ряд компромиссов. Эпигенетические изменения в СК за время жизни накапливаются. Механизм накопления эпигенетических изменений клетки уже известен:
1) со временем в клетке медленно теряются маркеры репрессированного хроматина, что может быть связано с дифференцировкой клеток в организме;
2) происходит утрата маркеров репрессии, которая рано или поздно приводит к дерепрессии дремлющих транспозонов и, соответственно, к росту количества вызванных ими повреждений ДНК;
3) отмечается активация клеточных систем репарации ДНК, которые участвуют в восстановлении ДНК, вызывают и несанкционированные рекомбинации в теломерах;
4) рекомбиназы транспозонов непосредственно инициируют рекомбинации ДНК;
5) в результате протяженные участки теломерной ДНК преобразуются в кольца и теряются;
6) теломеры укорачиваются на длину утраченной кольцевой ДНК и ускоряют утрату теломерной ДНК в десятки раз;
7) последующий апоптоз большинства клеток и предопределяет старение как биологическое явление.
Данный механизм является альтернативным гипотезе о генетически запрограммированном старении и гипотезе о старении как следствии накопления ошибок и повреждений, объясняет механизм ускорения утраты теломер в случае окислительного стресса и повреждений ДНК, а также взаимосвязь старения и возникновения опухолей (Галицкий, 2009).
Именно эти постгеномные эпигенетические изменения являются первым этапом старения соматической клетки. Но клетки крови живут очень недолго. Клетки сохраняют жизнеспособность в течение ограниченного периода (напр., эритроциты живут 100–120 дней, лейкоциты — 80–120 дней), поэтому они нуждаются в постоянной замене. Этот процесс постоянной замены обеспечивают кроветворные (гемопоэтические) стволовые клетки, находящиеся в красном костном мозге, после 25 лет. Все клетки периферической крови являются потомками кроветворных стволовых клеток или ГСК; из самых крупных ГСК образуются эритроциты. Во время этого процесса происходит несколько преобразований, и одна клетка остается СК или ГСК, а другая клетка становится гемопоэтической клеткой-предшественником (ГКП); эти клетки лишаются ядра, в них накапливается пигмент крови — гемоглобин. Другие клетки становятся дифференцированными и превращаются в различные типы лейкоцитов. Мезенхимальные стромальные клетки костного мозга являются строительным и реконструктивным материалом для реставрации повреждений солидных органов и эндокринных тканей. Очень важен тот факт, что ГСК способны превращаться в любые форменные элементы крови и клеточные элементы ткани, а другие — только в строго определенный вид форменных элементов крови. Тромбоциты, обусловливающие способность крови к свертыванию, возникают при разделении цитоплазмы стволовых клеток. Основными компонентами кроветворной системы после завершения роста и полового созревания являются костный мозг, лимфатические узлы и селезенка. В костном мозге происходит образование эритроцитов, разных форм лейкоцитов и тромбоцитов. Лимфатические узлы участвуют в процессах кроветворения, вырабатывая лимфоциты, плазматические клетки. Селезенка состоит из так называемой красной и белой пульпы. Красная пульпа заполнена форменными элементами крови, в основном эритроцитами; белая пульпа образована лимфоидной тканью, в которой вырабатываются лимфоциты. Помимо кроветворной функции, селезенка осуществляет захват из тока крови поврежденных эритроцитов, микроорганизмов и других чуждых организму элементов, попавших в кровь; в ней вырабатываются антитела. В теле взрослого человека кроветворение происходит в костном мозге коротких и плоских костей. Костная система кроветворения называется миелоидной системой (название произошло от греч. myelos — «костный мозг»). Красный костный мозг — основной орган кроветворения взрослого. В костном мозге, где имеются стволовые кроветворные клетки, происходит образование из них эритроцитов, тромбоцитов и лейкоцитов (гранулоцитов, лимфоцитов, моноцитов). Некоторые виды лейкоцитов вырабатываются в печени, селезенке и лимфатических узлах. Клетки крови, или, точнее, форменные элементы крови, образуются в красном костном мозге, откуда они попадают в большой круг кровообращения.
Таким образом, именно в системе кроветворения человека с возрастом происходит драматическое накопление дополнительных соматических мутаций и формируются патологические информационные постгеномные (эпигенетические, протеомные, транскриптомные, метаболомные, секретомные и т.д.) изменения молекулярно-биологической структуры собственной гемопоэтической (кроветворной) стволовой клетки организма и постгеномные нарушения в других тканеспецифических СК органов и тканей. Подобное утверждение было сделано после анализа научной литературы по данному вопросу и более 20 лет изучения геномики, транскриптомики, протеомики, секретомики и метаболомики тканеспецифичных СК и в первую очередь ГСК, изучения их межклеточных взаимодействий и взаимоотношений с патологическими клетками в организме и роли других СК в процессах патогенеза заболевания (Брюховецкий, Хотимченко, 2018). Но за последние годы понимание накопления эпигенетических нарушений в ГСК никак не объясняло механизма накопления патологических белков. Было очевидно, что неблагоприятное воздействие факторов внешней среды и внутреннего гомеостаза как-то должно было оставлять свой след в ГСК, и только в этом году на модели инфекций этот механизм стал понятен.
Еще 10 лет назад научной догмой иммунологии и гематологии было то, что ГСК — это неспециализированные клетки, слепые к внешним сигналам, таким как инфекции, излучения, интоксикации и т. д. Ведущие российские иммунологи (Черных и др., 2012; Селедцов и др., 2018) и специалисты в области иммунологии гемопоэза (Тупицын и др., 2002–2020, Гривцова и др., 2016) полностью разделяли эту точку зрения зарубежных специалистов (Rossi, 2017). Считалось, что только специализированные дочерние клетки ГСК могли чувствовать эти сигналы и активировать иммунную реакцию. Но работа немецкой лаборатории Дюссельдорфского университета под руководством проф. Michael Sieweke (de Laval, 2020) за последние годы доказала, что эта догма ошибочна, и показала, что ГСК действительно может чувствовать внешние факторы, чтобы специфически и прецизионно производить подтипы иммунных клеток «по требованию» для борьбы с инфекцией и другими патологическими антигенами. Помимо их роли в формировании экстренной иммунной реакции, оставался вопрос о функции ГСК в ответ на повторяющиеся инфекционные эпизоды и об иммунной памяти. Известно, что иммунная система обладает памятью, которая позволяет ей лучше реагировать на возвращающиеся возбудители инфекции и патологические антигены. Научное исследование команды Michael Sieweke et al. (2020) в настоящее время устанавливает центральную роль гемопоэтических стволовых клеток крови в этой долговременной иммунной памяти.
Научный сотрудник компании Inserm Sandrine Sarrazin и соавтор публикации из команды проф. Michael Sieweke утверждает: они обнаружили, что ГСК могли бы способствовать более быстрому и эффективному иммунному ответу, если бы они ранее подвергались воздействию LPS (липополисахарида) — бактериальной молекулы, имитирующей инфекцию. Проф. Michael Sieweke, объяснил, как они обнаружили, что память хранилась в гемопоэтических стволовых клетках: «Первое воздействие LPS приводит к тому, что следы откладываются на ДНК стволовых клеток, прямо вокруг генов, которые важны для иммунного ответа. Подобно закладкам, метки на ДНК гарантируют, что эти гены будут легко найдены, доступны и активированы для быстрого ответа в случае повторного заражения подобным агентом». Далее авторы исследовали, как память об антигене была записана на ДНК, и нашли белок C/EBPb. Это известный энхансерный белок, связывающийся с CCAAT-последовательностью, с которой связываются транскрипционные факторы для активации гена старения SMP30, или регукальцина (Regucalcin, RGN), также известного как маркер старения protein-30 (senescence marker protein-30). Вместе эти выводы должны подвести нас к улучшению настройки иммунной системы или улучшению стратегий вакцинации с одной стороны и к фундаментальному пониманию механизмов накопления эпигенетических изменений вокруг активных генов ГСК, участвующих в старении, с другой стороны.
Способность иммунной системы отслеживать предыдущие инфекции и более эффективно реагировать на них при повторном появлении является основополагающим принципом работы вакцин, но этот феномен накопления эпигенетических изменений рядом с геномом клетки приводит к ее старению, быстрому изнашиванию и даже смерти. Теперь, когда стало понятно, как стволовые клетки крови маркируют цепи иммунного ответа, ученые должны быть в состоянии оптимизировать стратегии иммунизации, чтобы расширить защиту для инфекционных и противоопухолевых агентов, а также отработать возможность очистки генома ГСК от эпигенетических антигенных шлаков, накапливающихся вокруг генома, и научиться их удалять. В более общем плане это также может привести к появлению новых способов усиления иммунного ответа в случае его недостаточной эффективности или отключения в случае чрезмерной реакции (de Laval, 2020). То есть накопление белка C/EBPb в эпигеноме ГСК — это важнейший элемент иммунной памяти, а не накопление эпигенетического «мусора» в них.
Особенно иллюстративно это научное положение о накоплении эпигенетического «мусора» вокруг активных генов, приводящем к нарушению функционирования клетки, на модели рака и других злокачественных заболеваний. Сегодня общепризнанное определение рака звучит так: рак — это генетическое заболевание ядра стволовой клетки (Канцерогенез, 2014). Приблизительно так же рассматриваются и другие фатальные заболевания цивилизации, где ведущими являются несостоятельность и недостаточность функций тканеспецифических стволовых клеток. Наряду с этим убедительных данных об исключительной роли повреждения (мутации) определенных генов при раке и целом ряде злокачественных новообразований нет. Есть достаточно большой набор поврежденных генов, который в каждом случае разный. При этом наличие эпигенетических, протеомных и транскриптомных изменений в ОК описано всеми исследователями, и они имеют закономерный характер. Именно накопление патологических белков в клетках при старении и практически при всех болезнях цивилизации является общим признаком и формирует повреждение генов. То есть в клетке с возрастом происходит первичное накопление постгеномных изменений, которые в ряде случаев формируют различные геномные повреждения — дополнительные соматические мутации. Это положение кардинально меняет стратегию лечения старости как болезни и целого ряда фатальных заболеваний цивилизации, имеющих аналогичный патогенез развития.
Но накопление различных патоспецифических белков в различных типах высокодифференцированных клеток организма — это явление достаточно типичное для возрастзависимых болезней, но его недостаточно для возникновения физиологической старости. Любой стресс и другие неблагоприятные этиопатогенетические факторы внутренней и внешней среды способны запустить цепь патобиологических процессов в пострадавшей клетке и обеспечить в ней накопление эпигенетических изменений ДНК, появление патологических РНК и патологических белков. Другой аспект, который делает постгеномный подход к старению клеток привлекательным, — это понимание фундаментальной биологической разницы между разными типами клеток и тканей организма. Например, клетки, которые активно делятся, с большей вероятностью пострадают от накопления мутаций и утраты теломер, чем дифференцированные клетки. В то же время необходимо уточнить, что данный тезис не относится к быстро и многократно делящимся трансформированным и опухолевым клеткам, которые не утрачивают теломер и не накапливают мутаций. Дифференцированные клетки с большей вероятностью пострадают от повреждения белками, чем клетки, которые быстро делятся и «разбавляют» поврежденные белки вновь синтезированными. Даже если клетка теряет способность к пролиферации за счет процессов старения, баланс механизмов повреждения в ней сдвигается.
Это достаточно обычный тип реагирования клетки на любое отрицательное воздействие, и механизм формирования этих протеинов хорошо известен и описан. Эволюционным механизмом решения этой проблемы для любой соматической и половой клетки является митоз. В результате митоза при делении клетки все патологические белки изолируются в одной части клетки, и при отшнуровывании и разделении клетки на две дочерние клеточные системы они локализуются в одной из них. Клетка, получившая в процессе деления столь большое количество патологических белков, становится нежизнеспособной и по механизму апоптоза погибнет и будет утилизирована иммунокомпетентными клетками организма, а здоровая клетка, освободившаяся от патологических белков, сможет продолжить свое нормальное существование. Поэтому простой феномен накопления эпигенетических изменений в ДНК и патологических белков в цитоплазме стареющей гемопоэтической стволовой клетки и может стать постгеномным стимулом старения всего организма и быть тем системообразующим фактором, который запускает весь каскад системного старения. Идея, что именно молекулярно-биологические постгеномные структурные изменения ГСК запускают весь процесс старения организма и приводят к его смерти, становится реальной при более фундаментальном рассмотрении роли и места ГСК во всей иерархии клеток и тканей организма человека.
Другими словами, наш Создатель (Бог, Природа или Эволюция) смоделировал наш организм настолько совершенным и оптимальным, что все его системы жизнеобеспечения, ткани и органы были способны самообновляться, реставрировать повреждения ткани, управлять саногенезом, саморегенерацией и саморегуляцией. В благоприятных условиях внешней среды, называемой в Библии словом «Рай», человек спокойно мог бы жить тысячу лет, т.к. большинство его клеток способны к замене и самообновлению, а долгоживущие клеточные системы имеют срок жизни около тысячи лет. Но это возможно только в модельной ситуации, а в условиях жизни на Земле все долгоживущие клетки (нервные клетки, клетки кости, ГСК, МССК и др.) подвергаются агрессивному воздействию факторов окружающей микросреды (неблагоприятные климатические условия, бактерии, вирусы, хищники и т.д.) и становятся самой главной мишенью этой совершенной системы, созданной Создателем. В ряду всех долгоживущих клеток именно кроветворные СК подвержены накоплению большего количества мутаций, значительно больше, чем нервные, мышечные и костные клетки. Именно ГСК и есть основная мишень для воздействия всех неблагоприятных факторов внешней и внутренней среды. Расположенные в нишах костного мозга, находящихся в длинных трубчатых костях, грудине и костях таза, они на первый взгляд являются самыми защищенными элементами в организме человека. Они защищены каркасом плотной костной ткани и, казалось бы, подвергаются механическому повреждению в меньшей мере. Но это не спасает их от повреждающих механических, инфекционных, токсических и вирусных воздействий факторов окружающей среды. И, казалось бы, бессмертные клеточные системы к концу жизни человека значительно уменьшаются в количестве и погибают. К 70 годам их количество в костном мозге сокращается в 10—15 раз, а иногда и более.
Гемопоэтическая стволовая клетка, или кроветворная стволовая клетка (КСК), — это клетка — родоначальница всей многомиллиардной системы клеток кроветворения (гемопоэза), всех клеток иммунной системы (иммунопоэза) и главный регуляторный, управляющий и саногенетический инструмент среди всех 220 типов тканеспецифических соматических и стволовых клеток в организме человека. ГСК впервые были описаны русским эмигрантом в США проф. А. А. Максимовым в 1908 г. как клетки — родоначальницы кроветворения. А. А. Максимовым было показано, что именно ГСК — это клетки, формирующие гемопоэз, т.е. клетки, лежащие в основе всего процесса кроветворения человека и животных. Но как мощное терапевтическое средство они не получили своего заслуженного признания в нач. ХХ в. Более полувека они были забыты, и только в сер. 1960-х гг. ГСК были успешно применены для лечения острых и хронических лейкозов, лимфолейкозов и миелолейкозов у взрослых и детей путем проведения трансплантации костного мозга (Менткевич, Маякова, 2010). Невероятные успехи в лечении рака крови и даже полное излечение больных от этого онкологического недуга обусловили широкое, но преимущественно одностороннее, в основном онкогематологическое применение ГСК в лечении заболеваний человека. Позже, к концу ХХ в., ГСК в большинстве современных исследований широко применялись для восстановительного лечения нарушенного гемопоэза у онкологических пациентов после высокодозной химиотерапии и лучевой терапии опухолей. ГСК использовались как фундаментальная основа трансплантаций костного мозга в лечении неопластических образований, но прямого противоопухолевого эффекта ГСК на раковые клетки ранее доказано не было (Брюховецкий А. С., 2011). По крайней мере в доступной нам литературе ничего подобного мы не нашли.
ГСК с маркерами клеточной поверхности CD34+, CD45+HLA-DR–, CD38–Gp130– в организме человека являются самыми универсальными регуляторами гомеостаза, т.к. имеют самый большой период жизненного клеточного цикла (ок. 360 дней; Пальцев и др., 2003). В свете современных концепций системного подхода к управлению очевидно, что в любом биохимическом процессе в организме млекопитающих управляющей системой является самая медленная фаза (Неймарк, 1985). В этой связи ГСК CD34+, CD45+HLA-DR–, CD38–Gp130– обладают доминирующими управляющими свойствами среди всех клеточных систем организма и их регуляторные функции являются системообразующими (Брюховецкий А. С., 2010) для всех нормальных клеток. Также ГСК в зависимости от органных потребностей тканей способны под влиянием сигналов микроокружения трансформироваться как в НСК, так т в МССК, что с позиций теории клеточного замещения является крайне важным для реставрации поврежденных тканей.
Функцию обновления и восстановления тканей in vivo выполняют преимущественно тканеспецифичные СК, которые представляют собой пул запасных недифференцированных стволовых клеток и клеток — предшественников различных типов тканей (Тепляшин, 2005). Выделены различные типы тканеспецифичных СК взрослого организма: гемопоэтические CD34+CD45+ (предшественники всех клеток крови) СК (ГСК) (патент РФ № RU 228319), нейрональные (CD133+СD133–) СК (предшественники клеток нервной ткани, НСК) (патент РФ № RU 3394593), мезенхимальные (CD10+, CD13+, CD44+, CD90+ (Thy-1), CD105+, CD34–, CD45– и CD117–) стромальные СК (МССК — клетки, способные дифференцироваться в клетки тканей мезенхимального происхождения) (патент РФ № RU 2252252), а также СК других зародышевых листков.
Необходимо отличать как взрослые ГСК CD34+CD45+HLA-DR–CD38–Gp130– от гемопоэтических клеток-предшественников, имеющих несколько другие маркеры клеточной поверхности: CD34+, CD45–HLA-DR+, CD38+Gp130+, так и взрослые МССК с маркерами клеточной поверхности CD10+, CD13+, CD44+, CD90+ (Thy-1), CD105+, CD34–, CD45– и CD117– от мезенхимальных стромальных прогениторных клеток (МСПК) CD10+, CD13+, CD44–, CD90+ (Thy-1), CD105+, CD34+, CD45+ и CD117+. Помимо отличия в маркерах клеточной поверхности, ГСК и МССК отличаются от ГКП и МСПК своими фундаментальными свойствами и функциями. Только взрослые СК способны при делении давать 2 СК или СК и прогениторные клетки-предшественники (ПКП), а ПКП способна поделиться только на 2 ПК, которые неспособны в обычных условиях производить СК. Функциональная плюрипотентность свойственна только СК, а у ПК она значительно ниже, чем у СК. Для ПК характерны мультипотентность и склонность к дифференцировке.
Самым первым и самым эффективным опытом терапии с использованием СК, позволившим полностью излечить пациентов от рака крови еще в 60-х гг. прошлого века, был опыт применения при ТКМ в случаях гемобластозов препарата ГСК и ГКП, т.е. клеток, являющихся предшественниками кроветворения. Путем трансплантации ГСК, полученных из костного мозга донора, удалось заместить все клетки кроветворения (гемопоэза) реципиента и полностью вылечить больного, страдающего острым миелолейкозом. Поэтому противоопухолевые свойства ГСК в онкогематологии являются золотым стандартом терапии ГСК и постоянным предметом изучения ученых уже более 70 лет. Более того, сегодня стало очевидно, что ГСК кроме формирования кроветворения имеют в организме важнейшую регуляторную и системообразующую функцию. В связи с этим считается, что применение биомедицинских клеточных продуктов (БМКП), изготовленных на основе ГСК, является наиболее перспективным направлением в современной медицине (Тупицын и др., 2014; Отчет DARPA за 2011). Уже более 100 тыс. пациентов по всему миру получили лицензированный американский клеточный продукт «Гемакорд», содержащий ГСК пуповинной крови.
Взрослые ГСК CD34+CD45+HLA-DR–CD38–Gp130– обладают уникальной способностью направленного трансфера в зону повреждения тканей органа, мигрируя на градиент концентрации воспаления (патотропизм, или хоуминг СК) (Брюховецкий А. С., 2013). ГСК, попадая в головной и спинной мозг, являются мощным индуктором синапсогенеза в них или участвуют в формировании новых межклеточных контактов в тканях солидных органов (Брюховецкий А. С., 2010, 2013).
Известно, что при пересадке ГСК в различные органы (почки, мозг, печень и т.д.) не наблюдолась их прямой трансдифференцировки в специализированные клетки (кардиомиоциты, миоциты или клетки кожи) этих органов, а трансплантация клеток — предшественников гемопоэза в сердце не приводила к формированию нейронов или секреторных клеток кишечника. Дифференцировка in situ, как правило, контролировалась сигналами микроокружения. Хорошо известна потенциальная возможность трансдифференцировки ГСК в НСК in vitro под воздействием определенных пертурбогенов (ретиноевая кислота; Kuroda et al., 2010). Многолетние клинические наблюдения также подтвердили отсутствие аномалий дифференцировки СК в трансплантате. В то же время ГСК обладают функцией целенаправленной миграции к зонам повреждения (Брюховецкий А. С., 2003; Чехонин и др., 2005; Баклаушев и др., 2014) в головном мозге, как и НСК и МССК. В 2003 г. J. Praice в Англии запатентовал технологию (патент №2216336 от 20.11.2003) трансплантации ГСК для интрацеребрального введения при лечении поврежденного мозга, которая также рекомендована авторами для использования в терапии болезни Альцгеймера, болезни Паркинсона и болезни Крейцфельда — Якоба. Аналогичные свойства целенаправленной миграции к повреждению, хоуминга, патотропизма ГСК характерны и для других тканеспецифических СК и их предшественников, таких как МССК и НСК (Snyder et al., 1997).
В настоящее время доказано, что трансплантированные клетки лейкоконцентрата мобилизованных мононуклеаров формировали костно-мозговые кластеры ГСК и гемопоэтических прогениторных клеток (ГПК) в ткани поврежденного органа (Ono et al., 1999). В нашей работе было показано, что мультиклеточный кластер мобилизованных МНК, ГСК и ГКП человека после введения в организм (кровь, ликвор, ткань органа) крысы вел себя как системообразующий по отношению к входящим в него клеткам, и те очень организованно и скученно мигрировали преимущественно (78%) в пострадавший орган, а затем и в зону максимального повреждения этого органа и равномерно распределялись в этой зоне (Брюховецкий А. С., 2013). E. Snyder описал подобный эффект миграции НСК за 36 дней при введении их в нервную ткань мозга из правого (интактного) полушария в левое полушарие, где была смоделирована глиальная опухоль мозга мыши. В нашем исследовании повторение данного эксперимента было проведено на крысах с глиомой С6. Введение лейкоконцентрата мобилизованных мононуклеаров, содержащих ГСК и МССК человека, в правое полушарие мозга крысы с моделированной глиобластомой в левом полушарии приводило к миграции ГСК в опухоль в течение не более чем 14 дней. Этот феномен может быть ключевым не только в решении вопроса регенерации органов и тканей после повреждения, но и в разработке и создании клеточных препаратов на основе ГСК в нейроонкологии и при старении. Именно клеточный кластер трансплантированных кроветворных стволовых клеток имеет важнейшее значение для трансфера этих клеток к месту повреждения, а также целенаправленного распределения их в зоне повреждения патологического органа и адгезии СК к пострадавшим клеткам, оказания оптимального саногенетического, регуляторного и реставрационного воздействия СК и их предшественников на поврежденные клетки органа и ткани.
По-видимому, роль клеток микроокружения ГСК в восстановлении нарушенного гемопоэза является определяющей для уровня функциональной активности ГСК как в нише костного мозга, так и для ГСК, трансплантируемых в кровь или ткань, а также переливаемых в ликвор в составе кластера костно-мозговых клеток. В этой связи мы полагаем, что для того, чтобы получить требуемый функциональный (регуляторный, противоопухолевый, нейрореставрационный и т.д.) эффект ГСК в организме человека, целесообразно использовать их именно в составе лейкоконцентрата, содержащего весь спектр клеток микроокружения костно-мозговой ниши. Именно поэтому в клинике нервных болезней мы широко использовали именно этот подход введения ГСК с мононуклеарами их микроокружения в организм неврологического и нейроонкологического пациента при их интравентрикулярной или интратекальной трансфузии в ликвор. ГСК мы вводили обязательно в составе мононуклеарной фракции лейкоконцентрата мобилизованной периферической крови, т.к. эффекта от введения чистой культуры ГСК мы не отметили ни в эксперименте, ни в клинике (Брюховецкий А. С., 2010, 2011, 2013; Брюховецкий А. С. и др., 2014, 2016). Интересно, что изолированное введение клеток лейкоконцентрата мононуклеаров, освобожденных от ГСК (СD34+CD45+CD45–), не обеспечивает требуемых нейрореставрационных эффектов в эксперименте у крыс (Брюховецкий А. С. и др., 2015), как и изолированное введение очищенных ГСК не дает нужных эффектов нейрорегенерации (Брюховецкий, Хотимченко, 2018). Поэтому старая английская пословица «Короля делает свита» как нельзя правильно характеризует взаимоотношения ГСК и клеток их нишевого микроокружения.
В результате протеомного картирования и профилирования белков ГСК человека в норме и при разных болезнях цивилизации нами были обнаружены глобальные протеомные нарушения белковой структуры ГСК при различных типах патологии и проявляющиеся в протеомных изменениях структуры ГСК и ее протеомного профиля маркеры белковой поверхности ГСК (Брюховецкий А. С., 2014; Bryukhovetskiy A.S., 2019). Причина этих изменений была выявлена экспериментально при изучении межклеточных взаимодействий ГСК с клетками различных опухолей и нейродегенеративными заболеваниями. Был установлен универсальный механизм процессов регуляции ГСК на уровне как клеточного цикла, так и аффекторных функций в патологических клетках. Оказалось, что ГСК посредством микровезикулярного транспорта осуществляет горизонтальный и вертикальный обмен белками с поврежденными клетками. ГСК выделяет экзосомы с регуляторными белками и микроРНК, которые, попадая в патологическую клетку, или реставрируют ее, или запускают в ней апоптоз (программную клеточную гибель). Однако в процессе межклеточной регуляции ГСК получают и патологические белки из поврежденных клеток (Брюховецкий А. С., 2014). Например, они накапливают опухолеспецифические белки (ОСБ) при взаимодействии с опухолевыми клетками (ОК) или тау-белки при взаимодействии с нервными клетками у больных с болезнью Паркинсона или болезнью Альцгеймера. Именно механизм межклеточного горизонтального и вертикального обмена белками и РНК между ГСК и ОК или нейродегенеративными клетками и есть ключ к запуску патологического системного процесса. В общем виде этот процесс выглядит следующим образом. В результате молекулярного механизма межклеточного протеомного обмена между патологическими клетками и ГСК накапливается критический объем патологических белков, который приводит к накоплению ДСМ. Если это ОСБ, то судьба ГСК может стать следующей: При количестве белков от 30 до 60% протеомной структуры ГСК формируются раковые СК (РСК), и в зависимости от специфики протеомной структуры ОСБ в ГСК пациента разовьется определенный вид гемобластоза (лимфолейкоз, миелоидный лейкоз, лимфома и т.д.). Скорость и количество накопленных в ГСК ОСБ задаюют время формирования процесса и определяют его как острый или хронический.
При количестве ОСБ менее 30% происходит иммунизация ГСК, и их потомки в виде всех иммунокомпетентных клеток (ИКК) врожденного (НК-клеток, НКТ-клеток, гамма-дельта Т-клеток) и приобретенного (дендритных клеток, цитотоксических лимфоцитов, макрофагов и т.д.) противоопухолевого иммунитета иммунной системы человека становятся толерантны к ОК, содержащим подобные ОСБ, что приводит к постоянному уклонению ОК от иммунного надзора и контроля ИКК крови и к беспрепятственному развитию опухоли.
В случае если ГСК накапливает до 30% патоспецифических белков от других патологичных высокодифференцированных клеток (бета-клеток поджелудочной железы, нейронов различной локализации или клеток соединительной ткани), формируются стойкие аутоиммунные внутритканевые процессы, в которых задействованы эти клетки. В случае накопления в ГСК большего количества патоспецифических белков эти клетки инициируют дегенеративный и атрофический процесс в этих специализированных клетках и манифестируют нейродегенеративными, эндокринными или системными заболеваниями соединительной ткани и т. д.
Если количество патологических белков менее 10–15% от общего количества картированных белков, то это свидетельствует в пользу обычного старения ГСК и наличия в них не только протеомных, но транскриптомных и эпигеномных нарушений.
В результате наших собственных исследований был установлен уникальный научный факт, что геномное и постгеномное повреждение ГСК — это и есть то информационное первичное «системообразующее начало», «ключ к запуску» и «основной двигатель» развития патологии при всех аутоиммунных, онкологических, эндокринологических и нейродегенеративных процессах в организме человека, а также фундаментальная причина включения, непрерывного динамического поддержания и летального завершения программы старости у человека и млекопитающих. Именно возникновение в соматических клетках и тканеспецифических стволовых клетках организма человека и млекопитающих под воздействием различных этиологических факторов (травма, ишемия, гипоксия, кровоизлияние, электромагнитное облучение, интоксикация и т.д.) различных патологических и патофизиологических процессов (оксидативного стресса, митохондриальной дисфункции, ослабленного поглощения глутамата, освобождения воспалительных медиаторов, возникновения в протеоме патологических белков и белковых агрегатов, возникновения мутаций, эксайтотоксичности глутамата и т.д.) и является причиной накопления в специализированных клетках-мишенях патоспецифических белков (теория накопления), которые блокируют их клеточный цикл (КЦ) на определенной стадии или осуществляют арест КЦ соматической клетки или СК.
Сила и активность этиологических и патогенетических факторов определяют разновекторность и разновеликость постгеномных нарушений в эпигенетике и метилировании ДНК в ядрах высокодифференцированных специализированных клеток, тканеспецифических стволовых клеток типа НСК, МССК и ГСК.
Таким образом, с позиций классической теории систем основным «системообразующим началом» и инструментом постоянного прогрессирования процессов старения и формирования большинства фатальных болезней цивилизации являются геномные и постгеномные (эпигенетические, транскриптомные, протеомные) молекулярно-биологические изменения в гемопоэтических стволовых клетках, приводящие к разновекторым ДСМ в ДНК. Геномные нарушения, приводящие к определенной болезни в ГСК, вторичны; первичны всегда эпигенетические и протеомные нарушения в предшественниках гемопоэза. Но системный подход не позволяет понять, почему происходит этот резкий биологический поворот в жизни живого существа от процессов созидания, строительства организма и его совершенствования к его разрушению и гибели.
Возможно, что решить проблему остановки развития организма при достижении генетически детерминированного фенотипа определенного вида млекопитающих и человека и запуска процессов старения может не системный, а исключительно информационный подход. С информационных позиций повреждение каждого из составных компонентов молекулярно-биологической структуры органов и тканей разрушает часть системных базовых механизмов саногенеза и самореставрации организма человека или млекопитающего и включает повреждение базовых механизмов системной биологии старения. Установленные учеными научные факты и отдельные данные о молекулярно-биологических процессах старения есть фактическое доказательство этих системных поломок организма. Весь этот арсенал мировых научных открытий в области старения — это, с одной стороны, мозаичные элементы единого системообразующего молекулярно-биологического механизма саморазрушения организма, а с другой стороны, медико-биологические «пазлы» очень сложной и многогранной картины информационного процесса, сопровождающегося функционально-морфологическим развалом органических анатомо-морфологических конструкций тканей и органов и потерей основных жизнеобеспечивающих функционалов многоуровневого организма. Поэтому мы не исключаем ни одного из описанных в этих теориях экспериментального факта или механизма развития процесса старения, а, наоборот, пытаемся найти их место в этой сложной, многоуровневой и многоцелевой картине из многочисленных биологических компонентов, оформленных учеными в виде различных научных теорий и разрозненных опытно-экспериментальных данных. Именно их правильные взаимодействие и взаиморасположение в этой на первый взгляд хаотичной картине тотального развала и деградации органов и тканей организма при старении позволяют увидеть закономерности этого феномена и их реальное место в этом очень строгом и генетически запрограммированном процессе эволюции и инволюции организма. Это во многом сможет объяснить все многообразие и мультисистемность биологических процессов, происходящих в организме человека и млекопитающих в процессе старения. Также этот подход позволит понять причины, приводящие к смерти высокоорганизованного и совершенного биофизического и молекулярно-биологического механизма под названием организм человека, имеющего многоуровневые системы дублирования функций и биологической защиты.
Несмотря на их биологическую важность, роль стволовых клеток в старении человека еще предстоит выяснить. Santos G.A., Magdaleno G.D., de Magalhães J.P. (2023) в своей исследовательской работе применили методологию машинного обучения к данным транскриптома GTEx и присвоили оценки стволовости 17 382 здоровым образцам из 30 тканей людей в возрасте от 20 до 79 лет. Они обнаружили, что ~ 60% исследованных тканей демонстрируют значительную отрицательную корреляцию между возрастом субъекта и показателем стволовости. Единственным существенным исключением из этого паттерна была матка, у которой исследователи наблюдали увеличение СК с возрастом. Вместе с тем, Santos G.A., Magdaleno G.D., de Magalhães J.P. наблюдали глобальную тенденцию положительной корреляции между пролиферацией клеток и стволовостью. При индивидуальном анализе тканей было обнаружено, что ~ 50% тканей человека демонстрируют положительную корреляцию между стволовостью и пролиферацией, а 20% — отрицательную корреляцию. Более того, анализы показывают отрицательную корреляцию между стволовостью и клеточным старением со значительными результатами примерно в 80% проанализированных тканей. Наконец, была выявлена тенденция к тому, что гемопоэтические стволовые клетки, полученные от старых пациентов, могут иметь большую стволовость. Santos G.A., Magdaleno G.D., de Magalhães J.P. присвоили баллы стволовости образцам и показали доказательства потери стволовости всеми тканями во время старения человека, что придает вес идее о том, что разрушение стволовых клеток способствует старению.
Особую роль в тканевых информационных взаимодействиях и взаимоотношениях занимают тканеспецифические стволовые клетки и клетки-предшественники, которые мобилизуются в экстремальных ситуациях для организма человека и животных, могут покидать свои тканевые ниши и становиться свободными на определенный период для выполнения регуляторных и управляющих функций, а также становиться свободно циркулирующими клеточными системами. Еще раз подчеркнем уникальный феномен ГСК! Они способны передвигаться в любом направлении внутри ткани, мигрировать в зоны повышения градиента воспаления в них и выполнять базовые регуляторные функции саногенеза и реставрации. Это самые «медленные» в своей ткани клетки, т.е. клетки с самым медленным клеточным циклом в ткани или органе человека, и их клеточный цикл является управляющим инструментом и камертоном для настраивания функций для всех клеток своей ткани и других тканей организма. Все другие клетки организма находятся в управляемых ими подсистемах.
Таким образом, в информационном плане в «системообразующем начале» старения определяющее место занимают специализированные тканеспецифические СК крови, которые исполняют функции трансфера целевой информации. Как работают эти тканеспецифические СК крови? В научной литературе описаны многочисленные механизмы патотропизма и целенаправленной миграции тканеспецифических СК в зоны повреждения тканей и органов. Тканеспецифические СК (нейральные, печеночные, мезенхимальные стромальные, гемопоэтические и т.д.) мигрируют в зоны повреждения (ишемии, гипоксии, воспаления, кровоизлияния и т.д.) и самостоятельно идут на градиент концентрации воспаления в поврежденной ткани (патотропизм, или хоуминг СК), формируемый в поврежденной ткани различными этиопатогенетическими факторами окружающей среды или нарушениями гомеостаза. Затем СК прилипают к патологическим клеткам (механизм клеточной адгезии), оказывают регуляторное или управляющее воздействие на поврежденные клетки по механизму «рядом стоящего» (by stаnder effect) и запускают процессы программной клеточной гибели (апоптоза) или, наоборот, активируют процесс санации и восстановления поврежденной клетки (регенерации; Брюховецкий А. С., 2019). В исключительных случаях СК может сама занять место поврежденной клетки и дифференцироваться в нужную клетку. Пластичность СК столь высока, что при отсутствии определенного типа тканеспецифических клеток в организме человека мультипотентные тканеспецифические СК одного типа (напр., нейральные) могут трансдифференцироваться в нужный тип мультипотентных СК (напр., в ГСК). Это было показано в эксперименте несколькими группами ученых, когда НСК женской особи трансдифференцировались в костном мозге доноров мужского пола в ГСК. После трансплантации НСК женских особей крыс в кровь животных мужского пола, осуществленной после проведенных высокодозной миелоаблативной химиотерапии и тотального облучения костного мозга, в ряде случаев становились ГСК. Особенностью этих тканеспецифических СК является то, что после стабилизации и нормализации состояния они снова уходят в свои тканевые ниши и снова выполняют функции регуляции постоянства количественного состава клеток. Например, гемопоэтические СК занимаются контролем кроветворения и регуляцией количества клеток крови в организме или выполняют надзорные функции за клетками нервной ткани ГСК, так же как и нейральные СК способны следить за отсутствием опухолевых клеток и балансом количества нейронов и глиальных клеток в нервной ткани (Брюховецкий И. С., 2018). Итак, на наш взгляд, собственные ГСК — это самый первый информационный эшелон старения в организме человека и животных. ГСК покоятся в костном мозге, выходят из состояния покоя и генерируют клонально ограниченных предшественников, когда получают внешние сигналы, играя важную роль в восстановлении гемопоэза и в качестве клеток-мишеней для генной терапии при гематологических злокачественных новообразованиях (Khan et al., 2020). ГСК и клетки-предшественники поддерживают высокую продукцию новых клеток, но уязвимы к истощению, что в конечном итоге приводит к частой анемии и снижению системных иммунных реакций. В частности, накопление повреждений ДНК и выработка активных форм кислорода (АФК) приводит к снижению регенеративной способности и миелоидной дифференцировке в старых ГСК, что иногда сопровождается несбалансированным иммунным ответом (Kuribayashi et al., 2021). Примечательно, что полярность цитоскелета, эпигенетические сдвиги и клональная селекция ГСК также представляют новое понимание механизмов их старения (Akunuru, Geiger, 2016).
Аутофагия — процесс, который подавляет митохондриальный метаболизм для сохранения ГСК, — также снижается во время гемопоэтического старения. Механически активация аутофагии активирует нижестоящую экспрессию SIRT3 — ключевого митохондриального белка, способного омолаживать кровь, — и таким образом ось «аутофагия — SIRT3» замедляет процесс старения (Fang et al., 2020). Имеющиеся данные также показывают, что слабая аутофагия в ГСК вызывает накопление митохондрий и активацию метаболического состояния, приводящую к ускоренной миелоидной дифференцировке и нарушению активности самообновления и регенеративного потенциала ГСК (Ho et al., 2017).
Предыдущие исследования определили продукцию АФК и низкую функцию митохондрий как механизмы, лежащие в основе старения ГСК (de Haan, Lazare, 2018). Метаболизм митохондрий жизненно важен для экспансии HSC плода, а потенциал митохондриальной мембраны (MMP) различается в HSC старых и молодых мышей. Сообщалось, что MMP можно фармакологически манипулировать in vivo для улучшения функции HSC (Mansell et al., 2021). Примечательно, что старые ГСК обычно демонстрируют усиленное митохондриальное окислительное фосфорилирование (OXPHOS) и повышенную продукцию АФК, что ухудшает функцию ГСК (Nakamura-Ishizu et al., 2020). В ГСК с дефицитом FIP200 (семейство киназ фокальной адгезии, взаимодействующих с молекулярной массой 200 кДа) скорость пролиферации, митохондриальная масса и продукция АФК повышены (Liu et al., 2010). Инактивация Drp1 (белок 1, родственный Dynamin), который опосредует деление митохондрий, вызывает потерю регенеративного потенциала HSC при сохранении покоя HSC (Hinge et al., 2020).
В соответствии с особенностью миелоидной дифференцировки возрастные профили в старых ГСК также показали, что гены, связанные с миелоидной дифференцировкой, активировались, в то время как гены лимфопоэза подавлялись (Rossi et al., 2005). Действительно, ГСК подвергаются возрастному эпигенетическому перепрограммированию, состоящему из перераспределения метилирования ДНК и снижения H3K27ac, H3K4me1 и H3K4me3 (Adelman et al., 2019). Сообщалось, что эпигеномные изменения метилирования ДНК тесно связаны с функциональным снижением ГСК во время старения (Beerman et al., 2013). Эти эпигенетические сдвиги затрагивают главным образом пути развития, формируя предрасполагающие условия для развития заболеваний, связанных со старением.
Кроме того, клональная селекция ГСК также лежит в основе механизмов старения (Akunuru, Geiger, 2016), в сочетании с заметными изменениями в нишах ГСК (Kuribayashi et al., 2021; Pinho, Frenette, 2019). Недавнее исследование показало, что гиперактивация HSC у мышей и людей с атеросклерозом потенциально способствует клональному гемопоэзу (Heyde et al., 2021). Дефицит инсулинового фактора роста-1 (IGF1) в микроокружении костного мозга инициирует клональную селекцию HSCs — фенотип, который был спасен прямой стимуляцией IGF1 (Young et al., 2021). Старые эндотелиальные клетки нарушают репопуляционную активность молодых ГСК в нише костного мозга (Poulos et al., 2017), подтверждая идею о том, что старение HSC вызывается как внутренними компонентами клетки, так и компонентами микроокружения. Зондирование микросреды выявило активацию экспрессии генов, индуцированную передачей сигналов IL-6 и TGF-β, в постаревшей строме костного мозга, прокладывающую путь к восстановлению функциональности старого костного мозга за счет ингибирования TGF-β рецептора и IL-6 (Valletta et al., 2020). Тем не менее состарившиеся ГСК были устойчивы к системным омолаживающим вмешательствам, передающимся через кровь, таким как трансплантация, парабиоз и перенос плазмы (Ho et al., 2021). В совокупности более глубокое выяснение механизмов старения ГСК может помочь нам определить новые мишени для задержки начала заболеваний, связанных со старением.
Молекулярно-биологическая трансформация ГСК приводит к геномным, эпигеномным, транскриптомным и протеомным изменениям значительной части этих клеток, и это ведет к формированию определенных патологических клонов ГСК, которые имеют тенденцию к увеличению и расширению. Формирование доминирующего клона (клонов) ГСК на молекулярном уровне определяется накоплением в их цитоплазме патоспецифических белков из поврежденных клеток. В результате клеточный цикл этих клеток еще более замедляется и эти ГСК становятся доминирующими в системном процессе регуляции и управления в гемопоэзе; они доминируют среди других 50–200 тыс. ГСК. Также патоспецифические клоны ГСК становятся победителями в «соревновании на выживание» с другими здоровыми ГСК организма и получают преимущества в размножении и репродукции. Итогом этого процесса становится формирование моно- или олигоклонального гемопоэза, который и является центральным пусковым стимулом системного вовлечения в процесс старения органов и систем организма и главным «двигателем» поддержания этого патогенетического процесса.
Моно- и олигоклональный гемопоэз формирует второй информационный эшелон старения. Первично формируется клональный гемопоэз с неопределенным потенциалом (англ. CHIP — clonal hematopoesis with indifferential potential). CHIP является системным явлением, запускающим многоуровневые морфофункциональные процессы старения в различных органах и системах организма человека и высших млекопитающих. С одной стороны, CHIP приводит к формированию малозаметных микроизменений в органах и тканях организма. А с другой стороны, со временем количественные микроизменения накапливаются и количество переходит в качество в виде накопления патоморфологических дефектов, нарушающих функции органов и тканей. К микроизменениям CHIP относятся интраганглионарные повреждения в автономной (вегетативной) нервной системе, которые нарушают ускоренную передачу информации между органами и тканями человека путем формирования сбоев информации и нарушений передачи пакетов импульсов электрического тока в периферическом нерве, осуществляющем передачу их по периферическим нервам между органами, с последующей трансляцией в центральную нервную систему и ее дальнейшим микроструктурным повреждением. Очевидно, что накопление повреждений ЦНС в течение времени и нарастание сосудистых нарушений в ЦНС и других системах организма постепенно формируют третий и четвертый информационные эшелоны старения организма человека и высших млекопитающих. Таким образом, формирование CHIP запускает целый каскад необратимых старческих изменений во всех органах и системах. Длительное существование и расширение CHIP в циркулирующей крови объясняет почти все феномены старения, описанные в научной литературе. Однако в этой книге мы не будем останавливаться на тонкостях работы этих информационных систем, а отошлем любознательных читателей к нашей монографии: Брюховецкий А. С. Проблемы теоретической неврологии. Информационно-коммутативное устройство и принципы работы мозга человека. М.: Полиграф-Плюс, 2014. 396 с.
Но вернемся после небольшого отступления к непосредственной тематике данной главы. Таким образом, возрастзависимое геномное и постгеномное заболевание кроветворных стволовых клеток и гемопоэтических предшественников является системообразующим феноменом единого системного процесса, который запускает многоуровневые информационные процессы старения. Каким образом информация, это удивительное «системообразующее начало» всего живого, способна противопоставить себя жизненной динамике неуклонного роста, развития, самосовершенствования молодого растущего организма человека? Как информация способна остановить эти процессы в определенной точке? Почему в итоге информация способна подавить и разрушить столь сильные, генетически детерминированные регуляторные и саногенетические механизмы и инструменты молекулярной самосанации, гемопоэза, иммунопоэза и гомеостаза, существующие в организме каждого млекопитающего и человека от момента его зачатия?
На самом деле ответ на этот вопрос лежит в самом содержании понятия «информация». Информация может быть как позитивной, так и негативной. Позитивная информация позволяет создавать и восстанавливать информационно-сотовое пространство, а негативная информация позволяет разрушать и ломать созданное ранее информационно-сотовое пространство. То есть, с информационных позиций процесс старения — это всего лишь изменение знака информации с плюса на минус или наоборот, а также усиление или уменьшение потока и объема информации. Поэтому и остановка процесса старения, и запуск процесса ревитализации могут быть решены путем смены знака информации с плюса на минус, и не более того. Это может быть реализовано путем увеличения или уменьшения объема и биологического содержания поступающей к управляемому или регулируемому объекту управления информации. Вопрос о том, как это сделать на практике, и должен стать предметом фундаментальных исследований человечества.
Попытаемся на аналогии показать возможности управления и регуляции этой информации. Если представить информационный поток в виде русла реки, а дно реки и ее берега станут носителями этой информации, то изменение русла реки и перенаправление ее в новое (другое) русло могут привести к большому наводнению и затоплению ближайшей местности и нанести ей большой урон. Или, наоборот, перекрытие русла реки может привести к осушению прежнего русла, в котором река текла годами, к наступлению засухи и обезвоживанию данной территории. Даже небольшое изменение русла реки может привести к необратимым изменениям экологии и нарушению социально-экономического функционирования данной местности. Так и с информацией, переносимой различными клеточными носителями. Изменение молекулярно-биологической структуры клетки как информационного носителя меняет информационную емкость и функциональную значимость этой клетки. А образование доминирующего клона клеток в крови формирует в организме определенные информационные потоки с отрицательным знаком, которые и создают основной негативный информационный вектор развития и воздействия этих клонов на ткани и органы. Очевидно, что значимую роль в этом сложном процессе имеют системообразующие носители информации, и в первую очередь кроветворная стволовая клетка. Она является главным информационным носителем жизнеобеспечения информационного выживания организма, родоначальницей большинства циркулирующих в крови клеток иммунной системы. Поэтому различные нарушения и изменения молекулярно-биологической структуры информационного носителя подобной информации приводят к изменению знака информации, изменению динамики информационных процессов, трансформации информационно-сотового пространства, формируемого данным клоном (клонами) ГСК. Учитывая, что в костном мозге взрослого человека имеется, по разным данным, от 50 до 200 тыс. ГСК, которые полностью обеспечивают поликлональность гемопоэза (существование большого разнообразия различных клонов ГСК, участвующих в кроветворении и регуляции иммунитета), трансформация или повреждение одной или даже сотен ГСК не являются критичными для выживания организма. Но возникновение, формирование и расширение одного или нескольких патологических клонов ГСК, в которых нарушена иммунная функция контроля и надзора за количеством опухолевых клеток, инфекционных бактериальных и вирусных агентов или патологических антигенов, становятся крайне опасными для человека или млекопитающих из-за возможности запуска патогенеза различных болезней цивилизации.
Для объяснения происходящих информационных изменений в ГСК и формировании патологической клональности нужно попытаться понять основную локацию, динамику и теоретические временные пределы формирования знаковых информационных процессов старения в организме человека. Где и когда клональный гемопоэз начинает осуществлять глобальный информационный фазовый переход и перелом жизненного цикла каждого человека от позитивной динамики биохимических и биофизических процессов развивающегося и растущего организма к негативной динамике увядания, разрушения, приводящей к смерти организма? Когда впервые наступает саморазрушительный процесс дегенерации ткани, атрофии клеток и смерти организма? Почему в целом ряде случаев детской онкологии и наследственных болезней столь совершенная система саморегуляции и обновления клеток организма, заложенная нашим Создателем, дает сбой у одних пациентов в очень раннем возрасте, а другим дает время дожить до 120 лет? Если теоретически считать, что процесс старения начинается из-за накопления дополнительных соматических мутаций в ГСК, накопления патологических белков и изменения молекулярно-биологической структуры ГСК, приводящей к клональности кроветворения, то как в процесс старения пошагово вовлекаются все остальные клетки и ткани организма? С чего и как морфологически формируется информационный процесс старости, и где он локализуется территориально в организме человека в первую очередь? В настоящее время с позиций доказательной медицины на эти фундаментальные вопросы науки ответов пока нет.
Итак, в организме млекопитающих и человека существует системообразующий информационный фактор старения в виде патоспецифического клонального гемопоэза, который формирует и поддерживает последовательный системный разновекторный (разнонаправленный) информационный стимул и временные ориентиры для запуска и начала формирования процесса старения человека в тканях и органах. Системообразующими факторами старения с этих информационных позиций являются как нарушение процессов передачи (трансфера) между носителями информации внутри клетки, так и ее блокирование на любом из информационных уровней органов и тканей и информационных этапов организма. Причиной этому могут быть самые различные этиопатогенетические факторы внешней среды и внутреннего постоянства систем организма, приводящие к информационной блокаде на любом из уровней. Если это информационное повреждение наступает медленно и значительно растянуто во времени на клеточном уровне, постепенно вовлекает все новые и новые клетки и новые информационные уровни и платформы, то мы расцениваем этот процесс как физиологическое старение. Возникновение негативной информации, запускающей начало генерализованного процесса старения организма человека, обусловлено невозможностью выполнения клеткой (клетками) физиологического алгоритма передачи информации между клеточными информационными уровнями как вследствие локальных молекулярно-биологических повреждений информационных носителей (ДНК, РНК, белков, углеводов, жиров, гормонов, ферментов, факторов роста и т.д.), так и в результате повреждения системных отношений клеток, тканей и органов в связи повреждением ЦНС, АНС или магистральных или микроциркуляторных сосудов.
Если этот процесс информационного блокирования развития протекает очень быстро и приводит к нарушению информационного проведения на уровне информационных этапов, то это состояние информационного блока, как правило, манифестирует острыми сердечно-сосудистыми или острыми неврологическими заболеваниями (инфаркт миокарда, кардиомиопатии, все виды инсультов, сосудистые энцефалопатии и т.д.). Сегодня этот факт абсолютно подтвержден наличием клонального гемопоэза. Если блок проведения информации обусловлен формированием опухоли, то в зависимости от локализации в органе и степени ее злокачественности мы получаем различные онкологические заболевания и рак. Клональность гемопоэза также обнаружена при многих онкогематологических болезнях, о чем мы будем говорить ниже. Если нарушения проведения информации обусловлены аутоиммунными процессами в тканях, то блоки информации могут как быть кратковременными, так и приводить к смертельному исходу. Клональность гемопоэза также установлена при системных аутоиммунных заболеваниях. Эта новая теория не может быть обозначена как информационная теория старения, т.к. нами использована исключительно методология информационного подхода, а сама теория должна быть основана на абсолютно доказуемых и проверяемых феноменах изменения информации на разных уровнях ее представленности в организме.
Итак, главным фундаментальным началом, обеспечивающим внутриорганную и общеорганизменную коммутацию и взаимодействие всех структурных компонентов (клеток, тканей, органов и систем жизнеобеспечения) тела человека, является информация. Под информацией, как мы отмечали ранее, мы понимаем исключительно физические процессы и электромагнитные физические явления (волны, частоты, резонансы, осцилляции и т.д.), возникающие в организме человека под воздействием окружающей среды и под воздействием эндогенных физиологических процессов, которые осуществляют взаимодействия, взаимовлияния и коммутацию различных систем организма в одно целое и регуляцию и управление всех процессов в организме человека и млекопитающего. Кстати, уже существует информационная теория старения, которая отводит информации в этом процессе главную роль, но мы не будем на ней останавливаться и предложим читателю самому ознакомиться с ней на досуге. Для нас информация в организме — это основное связующее и системообразующее звено, обеспечивающее слаженную синхронную и очень системную работу всех компонентов и биологических систем человеческого организма. Известно, что соматосенсорная изоляция человека от информации на длительное время способна привести к тяжелым заболеваниям и даже к смерти. Но, по-видимому, в процессе старости речь идет не о повреждении самой информации, а о повреждении и сокращении количества ее биологических носителей и механизмах их поломки и повреждения. Весь этот процесс носит название клонального кроветворения (гемопоэза). В следующей главе мы к этому еще вернемся и детально обсудим эти положения.
Наиболее очевидной общебиологической информационной шиной этих сложных процессов являются кровь и ее компоненты. Именно в периферической крови разыгрывается основной сценарий «полицейского разворота» (полного разворота для движения в противоположную сторону) позитивного созидательного процесса молекулярно-биологического строительства организма на его медленные и пролонгированные демонтаж и разрушение, приводящие со временем к смерти этого человека или млекопитающего. В биологической основе этого поворота на 180 градусов лежат, на наш взгляд, формирование и расширение моно-и олигоклонального гемопоэза, который имеет определенную патоспецичность (нейроспецифичность, онкоспецифичность, кардиоспецифичность и т.д.).
С теоретических позиций практически невозможно представить, чтобы этот биологический поворот к старению происходил запрограммированно тогда, когда прожита лишь ¼ часть естественной жизни человека и его генетическая программа клеток солидных и эндокринных органов работает на созидание, рост и конструирование его органов и систем до определенного фенотипического стандарта. Все остальные периоды (потенциальные ¾ продолжительности жизни) экспрессия этих генов пролиферации и дифференцировки находится в подавленном (супрессивном) состоянии. В большинстве случаев патологические состояния организма человека могут создать сверхэкспрессию этих подавленных генов, и тогда возникают рак или другие злокачественные опухоли. Возможно и наоборот: они могут усилить подавление (ингибирование) этих генов и вызвать дегенеративный процесс и атрофию высокодифференцированных специализированных клеток. Кровь — главная информационная шина организма млекопитающих, способная взаимодействовать со всеми соматическими и эндокринными клетками и тканями организма. Поэтому первично именно через кровь должно формироваться «системообразующее информационное начало», запускающее системный процесс старения. Кровь составляет примерно 8% от всей массы тела человека, в кровеносных сосудах циркулирует 5–8 л крови; в этом количестве содержится 25–40 млрд эритроцитов и 25–50 млрд лейкоцитов. Этого количества информационных «дискет» вполне достаточно для создания требуемого информационного «шторма», запускающего процесс, обратный росту и развитию, в органах — мишенях организма.
Однако какие же клеточные системы организма человека и как конкретно страдают при формировании процесса старения? Мы считаем, что «системообразующим началом» и «мотором» патологического информационного процесса старения и причиной смерти организма млекопитающего и человека является геномное и постгеномное повреждение собственной ГСК, приводящее к клональному гемопоэзу. Следует вспомнить о том, что ГСК — это самая центровая и важнейшая клетка всех процессов гемопоэза, иммунопоэза и регуляторных процессов у млекопитающих и человека. Одна ГСК способна дать человеку при трансплантации костного мозга весь спектр необходимых (до 36 млрд) клеток его крови и обеспечить полное излечение при целом ряде фатальных заболеваний (гемобластозах, лимфомах, рассеянном склерозе, системной красной волчанке, ревматоидном артрите и еще более чем 250 нозологиях), а 3 ГСК способны подавить деятельность любой РСК самой злокачественной опухоли (Брюховецкий И. С., 2017; Брюховецкий, Хотимченко, 2018).
Другими словами, наличие дополнительных соматических мутаций в ГСК и формирование генетического дефекта этих прогениторных клеток при старении и у пациента с возрастзависимыми БЦ не являются приговором прогрессирования его болезни и преждевременной смерти, т.к. геномы его клеток достаточно стабильны и устойчивы даже несмотря на наличие наследуемых и приобретенных мутаций. Причинами прогрессирования старения и возникновения БЦ являются возрастзависимое критическое накопление ДСМ и формирование генетической и постгеномной почвы для фатальных осложнений, в первую очередь в ГСК. Этой почвой, несомненно, является клональный гемопоэз! Что же тогда лежит в биологической основе фатальных осложнений БЦ? Именно формирование неустойчивости геномов высокодифференцированных тканеспецифических клеток органов и тканей и есть фундаментальная патогенетическая и биологическая основа старения и смертельных осложнений у этого контингента больных. Вот лишь несколько примеров этого феномена.
Неустойчивость, или нестабильность, генома тканеспецифических опухолевых клеток — это доказанная фундаментальная причина возникновения большинства онкологических болезней (Бовери, 1901), обусловленная формированием опухолевых стволовых клеток из тканеспецифических (нейральных, гемопоэтических, мезенхимальных стромальных и др.) клеточных предшественников пациента с БЦ путем присоединения к их геному ДСМ.
Нестабильность генома нейронов головного мозга — фундаментальная причина возникновения большинства нейродегенеративных проявлений и атрофии нервных клеток при наследственных нервных болезнях, которая формируется в результате появления в них ДСМ и возникновения неустойчивости генома высокодифференцированных специализированных нервных клеток (нейронов различной локализации) в результате септического или асептического воспаления, последующего аутоиммунного процесса и как следствие аутоагрессии иммунокомпетентных клеток к нейронам, приводящая к их дегенерации (Брюховецкий А. С., 2003, 2016).
В результате появления неустойчивости, или нестабильности, генома собственных соматических клеток разных органов и желез секреции, имеющих фенотипические мутации, при присоединении дополнительных соматических мутаций развиваются аутоиммунные и сердечно-сосудистые заболевания, а также классический процесс старения.
Очевидно, что из-за неустойчивости геномов высокодифференцированных клеток организма при старении и формировании молекулярно-генетической и постгеномной основы осложнений возрастзависимых БЦ вылечить данные болезни невозможно, т.к. они обусловлены наследуемым из поколения в поколение генетическим дефектом генома и постгеномными изменениями высокодифференцированных тканеспецифичных клеток организма. В результате этих процессов жизнь людей резко ограничена возможной декомпенсацией их соматического состояния, в результате которой у них развиваются фатальные осложнения, приводящие к смертельному исходу. Однако если нельзя вылечить болезнь, то можно попробовать компенсировать соматическое состояние организма стареющего человека. Мы можем предпринять попытку предотвратить развитие рецидива болезни и фатальных осложнений, приводящих к смерти, и увеличить продолжительность его жизни.
Проведенный нами сравнительный анализ большинства известных мировых научных фактов и опубликованных экспериментальных данных о биологии процесса старения и о патогенезе возрастзависимых болезней цивилизации, обобщение существующих научных теорий и концепций старения, изложенных в предыдущей главе, и почти 35-летний личный опыт в изучении и применении различных типов клеточной терапии у человека, позволяют нам прийти к достаточно неожиданному выводу. Его можно сформулировать следующим образом: фундаментальным молекулярно-биологическим «системообразующим началом» и главным биологическим «двигателем» патологического процесса старения и формирования возрастзависимых болезней цивилизации является геномно-постгеномное (эпигеномное, транскриптомное, протеомное и др.) заболевание собственных гемопоэтических стволовых и прогениторных клеток человека и млекопитающих, приводящее к формированию и расширению патоспецифических клонов аутологичных гемопоэтических стволовых клеток и гемопоэтических клеток — предшественников костного мозга. Мутационные изменения генома и молекулярные повреждения протеома ГСК и ГПК, накапливаемые в процессе жизни человека и животных, приводят к формированию системных прогредиентных патологических процессов биологии старения в виде клонального гемопоэза с неопределенным потенциалом, который со временем трансформируется в определенный (онкоспецифический, нейроспецифический, кардиовазоспецифический и т.д.) доминирующий тип клонального кроветворения. Клональность кроветворения формирует многогранность фенотипических проявлений старения.
Как мы уже отмечали, ГСК как самые долгоживущие клетки организма, накопившие в процессе жизни драматическое количество ДСМ, есть главные системообразующие и главные регуляторные клеточные системы крови человека и млекопитающих, ответственные за старение и приводящие к смерти организма. Именно они являются родоначальниками всех функционально недостаточных иммунокомпетентных клеток иммунной системы организма млекопитающих и человека, а также формируют патоспецифический клональный гемопоэз, который отвечает за процессы возникновения возрастзависимых болезней в организме эукариот, и являются причиной внезапной смерти людей!
Глава 7. Клонально-кроветворная теория старения
В данной главе мы попытались сформулировать и обосновать свою авторскую точку зрения на процесс старения у человека и млекопитающих и возникновение возрастзависимых болезней цивилизации, а также научно аргументировать предложенную нами клонально-кроветворную теорию старения. Начнем изложение данной теории с установленного нами в предыдущей главе научного факта, полученного путем проведенного научно-теоретического анализа по выявлению молекулярно-биологического системообразующего фактора, формирующего и неуклонно поддерживающего процесс старения органов и тканей в организме человека и млекопитающих. Нами был сделан однозначный вывод о том, что этим фундаментальным требованиям системной биологии старения наилучшим образом удовлетворяют преимущественно собственные гемопоэтические стволовые клетки и гемопоэтические клетки-предшественники организма человека и животных. Именно эти долгоживущие клеточные системы формируют, поддерживают и усугубляют хроническое патологическое состояние кроветворения, называемое генетиками во всем мире клональным гемопоэзом (Jaiswal et al., 2022). Очевидно, что клональный гемопоэз формирует патоспецифические системные иммунные реакции организма человека на патологические антигены, трансформированные, поврежденные или пострадавшие собственные клетки и ткани организма млекопитающих, является ведущей причиной возникновения и прогрессирования основных возрастзависимых заболеваний человека и стал основной причиной внезапной смерти людей в 40% случаев (Jaiswal et al., 2014).
Очевидно, что ГСК и ГКП в организме эукариот, с одной стороны, являются родоначальниками всех клеток крови, создают и формируют весь многомиллиардный объем клеточных систем циркулирующей в организме человека и млекопитающих крови, а с другой стороны, отвечают за создание клеточно-гуморального врожденного и приобретенного иммунитета человека и формирование всех иммуноспецифических защитных и адаптивных реакций организма человека и животных на возможную смертельную угрозу (бактерии, вирусы, простейшие, химические антигены и т.д.). Именно они обеспечивают выживание живого организма, а также организуют регенерацию тканей организма и системную коррекцию внутриклеточных нарушений, возникающих в ответ на стресс, повреждение и неопластическую трансформацию в дифференцированных клетках организма.
ГСК и ГПК несут центральную системообразующую функцию по организации системы защиты всех поврежденных клеток органов и тканей организма. Эта функция ГСК обусловлена подготовкой, формированием и реализацией ими специализированного иммунного ответа на любой патогенный фактор или полученное соматической клеткой повреждение. Роль и участие ГСК и ГПК являются важнейшими в судьбе каждой поврежденной специализированной клетки организма человека и млекопитающих.
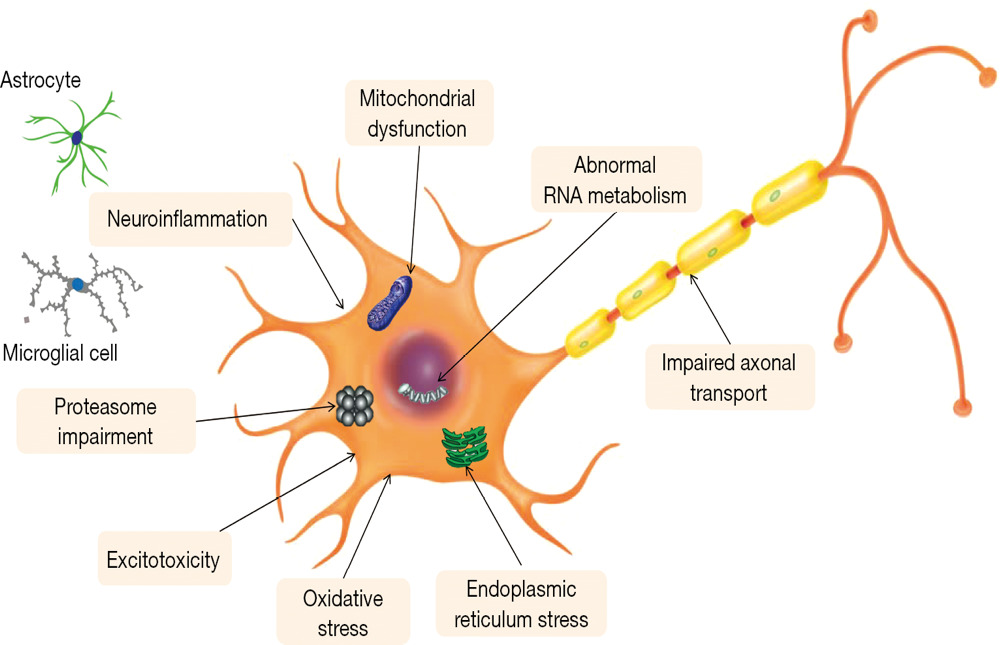
в дифференцированной клетке (нейроне), возникающие в результате стресса и (или) повреждения: нейровоспаление, митохондриальная
дисфункция, ненормальный метаболизм РНК, нарушение аксонального транспорта, стресс эндоплазматического ретикулума, оксидативный стресс, эксайтотоксичность, протеасомные нарушения и т. д.
Возникает резонный вопрос: как ГСК участвуют в судьбе каждой поврежденной клетки? Оказывается, что самым непосредственным образом! В результате стрессового воздействия различных экстремальных факторов внешней и внутренней среды на дифференцированные клетки в процессе всей жизни живого организма возникают достаточно типичные внутриклеточные молекулярно-биологические нарушения (рис. 2), которые, как правило, ведут к формированию дополнительных соматических мутаций их генов. Мутирующие гены характеризуются избыточной патологической экспрессией транскриптов (иРНК, тРНК и др.) и появлением в цитоплазме клетки патологических тканеспецифических (онкоспецифических, нейроспецифических, кардиовазоспецифических, аутоиммунных и т.д.) белков (в зависимости от локализации патологического процесса), которые в результате накопления в цитоплазме клетки приводят к нарушению работы внутриклеточной машинерии этой клетки. Скопившиеся в клетке патологические белки, называемые еще белками накопления, практически не могут быть выведены из специализированной тканеспецифической клетки обычными инструментами внутриклеточного и межклеточного транспорта, что приводит к неустойчивости генома этих дифференцированных клеток. Именно формирование геномной неустойчивости специализированных дифференцированных клеток в итоге и предопределяет их встречу с ГСК и ГПК в поврежденной ткани, которая вершит их судьбу и определяет конечный финал всех пострадавших клеточных систем и систем их микроокружения. Попытки сбалансировать неустойчивый геном пострадавшей специализированной клетки в ткани сначала принимают на себя специализированные иммунокомпетентные клетки (НК-клетки, НКТ-клетки, гамма-дельта Т-клетки, макрофаги и различные типы Т-клеток) крови. Они выходят из сосудов через сосудисто-тканевые барьеры в поврежденную ткань и формируют воспаление вокруг них. При неэффективности ИКК стабилизировать неустойчивость генома в этих клеточных системах на градиент концентрации воспаления в ткани приходят сначала собственные тканеспецифические СК (нейральные, мезенхимальные, печеночные и т.д.), и если они не справляются, то основную регуляторную роль берут на себя ГСК и ГПК, которые или запускают апоптоз в этих клетках, или нормализуют их работу путем регуляторного воздействия каскада собственных цитокинов. В случае неэффективности прямого управляющего и регуляторного воздействия собственных ГСК и ГПК на поврежденную специализированную клетку, они уходят в свои ниши и формируют системный иммунный ответ организма относительно этих поврежденных специализированных клеток. Таким системным ответом ГСК и ГПК на поврежденные клетки становятся или иммунотолерантность собственной иммунной системы к патологическим антигенам этой клетки или к самим клеткам, или иммуноагрессивность к этим клеткам, направленная на антигены этих клеточных систем или на сами клетки.
Особенно наглядно роль и значение ГСК в судьбе поврежденных и стареющих специализированных клеток иллюстрируют взаимоотношения их с опухолевыми клетками в процессе канцерогенеза, обусловленного накоплением онкоспецифических белков в цитоплазме ОК. Мы уже начали обсуждать этот аспект в предыдущей главе, а в этой главе хотелось бы остановиться на нем более доказательно, с опорой на научные факты. Неустойчивость хромосом тканеспецифических ОК при раке была отмечена еще в нач. ХХ Теодором Бовери. Другие исследователи рака тоже показали, что накопление мутаций в генах приводит к нестабильности генов (Urh et al., 2005). В дальнейшем было подтверждено, что анеуплоидии (дополнительные хромосомы или отсутствие хромосом) непременно ведут к неустойчивости кариотипа (Hassold et al., 2007). Установлено, что появление случайных мутаций в опухолевых СК приводит к генерации дефектных белков (Loeb, 1976), а хромосомная нестабильность приводит к появлению мутаций в онкогенах и генах-онкосупрессорах в опухолевых клетках органов и тканей (Reya et al., 2001). Дифференцированные тканеспецифические клетки с неустойчивым геномом становятся подобными эмбриональным СК, которые крайне нестабильны и способны трансформироваться в раковые клетки (Snyder et al., 2001).
Почему специализированные клетки организма человека и высших млекопитающих реагируют на стресс неустойчивостью генома собственных высокодифференцированных клеток? Это сбой системы или способ выживания? Есть мнение, что неустойчивость генома поврежденных дифференцированных клеток, например в случае канцерогенеза, вообще может рассматриваться как одна из форм нового видообразования живых существ на Земле. Эта точка зрения была впервые сформулирована Peter Duesburg из University of California Berkeley CA, USA (Duesberg et al., 2011) в статье Is carcinogenesis a form of speciation? в журнале Cell Cycle. Исследователями было доказано, что неустойчивость генома и кариотипа опухолевых клеток это путь к образованию нового вида клеточных систем эукариот или к канцерогенезу, завершающемуся летальной анеуплодией этих клеток (рис. 2).
В других случаях неустойчивость генома поврежденных высокодифференцированных клеток может завершиться его стабилизацией и компенсацией за счет механизма саногенеза клетки, обусловленного молекулярным ремонтом повреждения. Некоторые исследователи считают, что именно нестабильность генома поврежденных дифференцированных клеток позволяет осуществить обратимость трансформации опухолевых клеток при дифференцировке в нормальные клетки, именно из-за нестабильности дефектных белков (Васильев, 1986). Другими словами, в каждой дифференцированной клетке есть программа самореставрации, которая способна устранить неустойчивость генома и любая поврежденная клетка имеет потенциал «вернуться в строй» и продолжить свое нормальное функционирование. В ряде случаев поврежденная дифференцированная клетка уйдет в программную клеточную гибель (апоптоз) и самоликвидируется, а ее останки будут утилизированы очистными системами организма.
Мы не собираемся обсуждать в этой книге роль и значение неустойчивости генома в многообразии видообразования живых существ на нашей планете или правомерность концепции Питера Дьюсберга, а лишь подчеркнем общепризнанность факта неустойчивости генома в судьбе поврежденных дифференцированных клеток и роль данного факта для понимания молекулярных процессов в этих клетках. Однако независимо от исхода поврежденной клетки ведущая роль в формировании судьбы этой стандартной модификации клеточной системы принадлежит не столько самим этим клеткам, сколько клеткам иммунной системы организма. Именно иммунный ответ организма на любое повреждение определяет судьбу поврежденных клеток. Таким образом, старение — это иммуноассоциированное и иммуноопосредованное постгеномное заболевание гемопоэтических предшественников организма, обусловленное формированием патоспецифического (онкоспецифического, нейроспецифического, кардиовазоспецифического и др.) возрастного клонального гемопоэза. Именно клетки иммунной системы и ГСК, являющиеся их родоначальниками, в конечном итоге определяют судьбу и исход постаревшей, перенесшей стресс или поврежденной высокодифференцированной специализированной клетки. Именно иммунокомпетентные клетки периферической крови и ГСК костного мозга человека и животных взаимодействуют с дифференцированной клеткой, находящейся в патологическом стрессовом состоянии или имеющей повреждение, и именно они обусловливают ее судьбу.
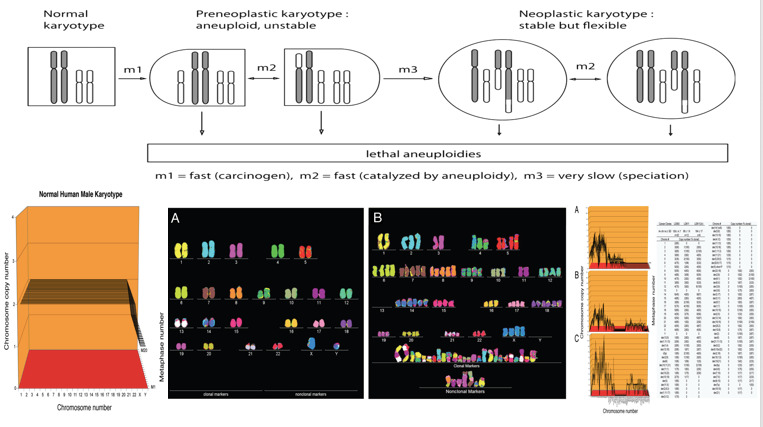
(цит. по: Duesberg et al., 2011)
От активности собственных гемопоэтических предшественников зависят выживаемость этих клеток и их дальнейшая судьба. Агрессивная реакция (иммуноагрессивность) иммунной системы организма на эти клетки приведет к атаке собственных специализированных иммунокомпетентных клеток на них, формированию нейровоспаления вокруг них с последующей дегенерацией и в конечном счете к их смерти путем апоптоза (рис. 3).
В других случаях именно иммунный ответ, организованный собственными ГСК в виде направленного узкоспециализированного каскада клеточно-гуморальных ответов, формирует иммунотолерантность основных иммунокомпетентных клеток и приводит к тому, что патологическая клетка трансформируется в опухолевую клетку или опухолевую стволовую клетку, бурно размножается и пролиферирует при полном «попустительстве» собственной иммунной системы. Таким образом, в настоящее время доказано, что неустойчивость генома возникает в поврежденной или находящейся в стрессе высокодифференцированной клетке млекопитающих и человека и проявляется в различных повреждениях хроматина ядра этой клетки. При этом хорошо известны и уже описаны природные механизмы саногенеза и защиты стволовых клеток при различных повреждениях (al Zouabi, Bardin, 2020). На рис. 4 схематически представлены основные известные механизмы защиты СК при повреждении.
А на рис. 5 представлены схема основных молекулярных повреждений в дифференцированной клетке и пути репарации любой клетки в ответ на стресс, приводящий к дополнительным соматическим мутациям. Эти повреждения ДНК могут быть санированы само́й пострадавшей клеткой за счет активации внутриклеточных природных механизмов саногенеза.
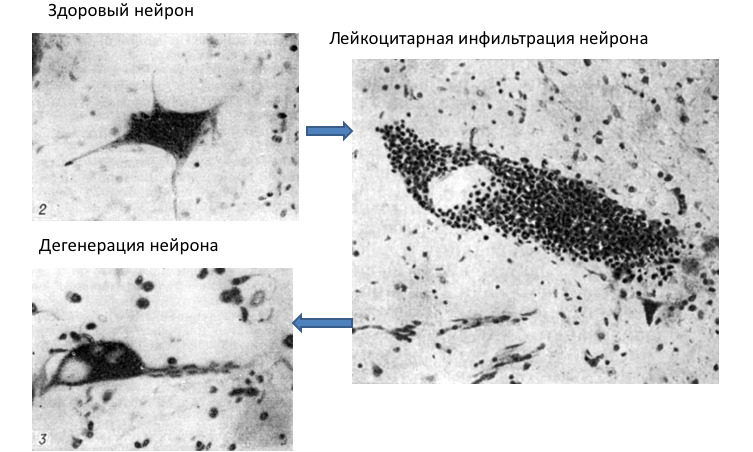
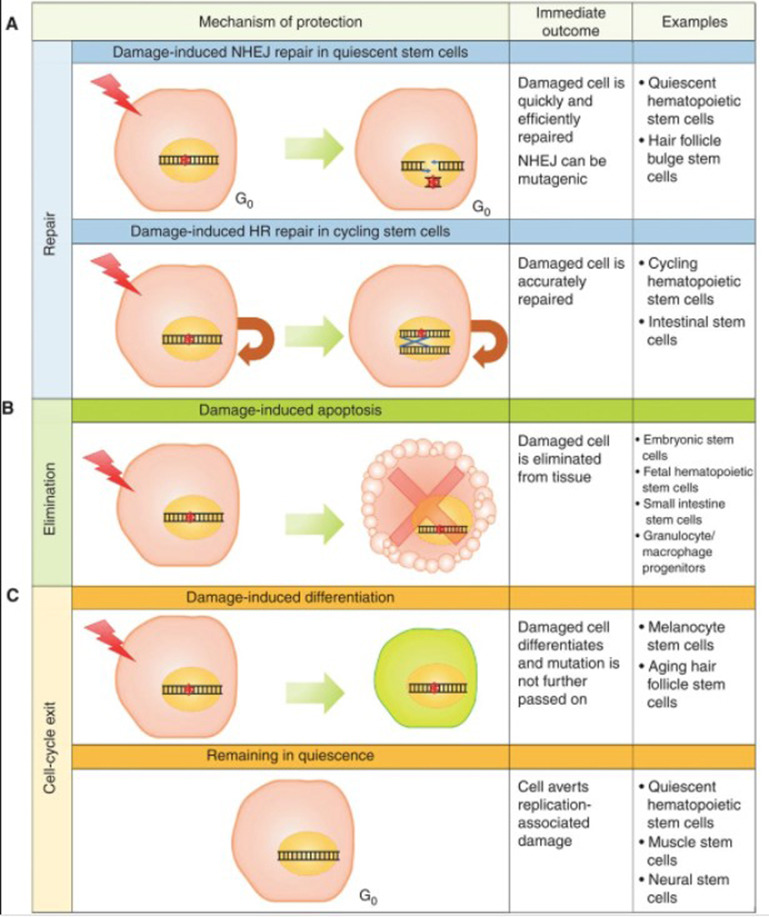
(цит. по: L. al Zouabi and A.J. Bardinб 2020).
A — ремонт: в зависимости от состояния клеточного цикла клетки клетка подвергается ремонту либо за счет негомологичного соединения концов (NHEJ) (верхняя панель), либо за счет гомологичной рекомбинации (HR) (нижняя панель). NHEJ — это быстрый и эффективный механизм, используемый покоящимися стволовыми клетками, когда они сталкиваются с повреждениями. Он включает лигирование разорванных концов и часто приводит к появлению небольших делеций, но также может приводить к транслокации и перестройкам генома. HR используется, если клетка циклически повторяется и проходит S-фазу, дублируя свои хромосомы, обеспечивая шаблон для восстановления поврежденной хромосомы. Обычно это более точная репарация, чем NHEJ, хотя ошибочный выбор гомологичной хромосомы, а не сестры может привести к потере гетерозиготности (LOH).
B — выведение апоптозом. Некоторые клетки скорее подвергаются апоптозу, чем ремонтируются. Если этот механизм используется преимущественно в стволовых клетках, существует более высокая вероятность истощения стволовых клеток. C — выход из клеточного цикла: дифференцировка (верхняя панель) при повреждении ДНК или пребывание в состоянии покоя.
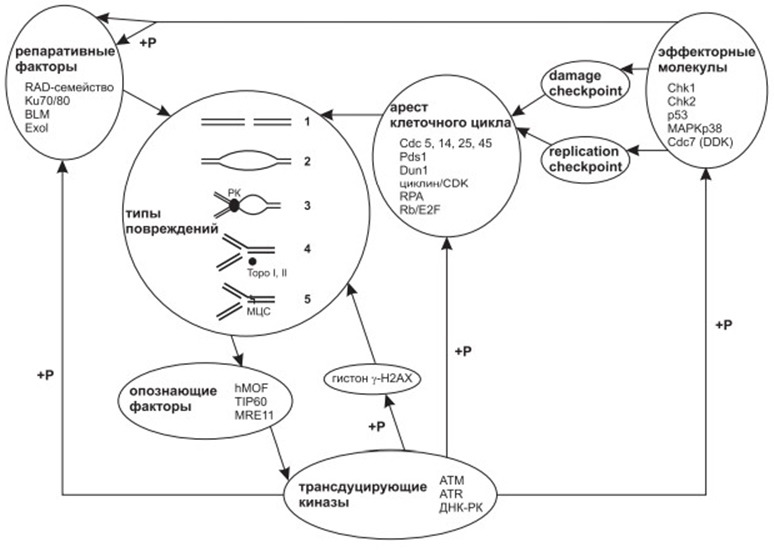
2 — изменение структуры хроматина высших порядков; 3 — сталлирование репликативной вилки; 4 — ингибирование активности топоизомераз;
5 — генотоксическое воздействим химических реагентов. РК — репликативный комплекс; Topo I, II — топоизомераза I, II; +Р — фосфорилирование (цит. по: Богачев, Шурдов, 2008)
Очевидно, что окончательный исход поврежденной специализированной клеточной системы предопределен не только ее потенциальными способностями к самореставрации и саногенезу, но еще и выраженностью нейровоспаления, сформированного доминирующими клонами гемопоэза и их системными иммунными реакциями в виде иммуноагрессивности или иммунотолерантности к этим пострадавшим клеткам.
Объясняют эти феномены иммунной памятью иммунокомпетентных (плазматические клетки, В-клетки памяти, Т-клетки памяти) клеток периферической крови (Киселевский, 2015). Однако совсем недавно на модели искусственных бактерий группой немецких исследователей под руководством проф. Michael H. Sieweke из Дрезденского университета (Германия) было доказано, что в иммунной памяти определяющее место занимают не столько иммунные плазмоцитарные клетки памяти и другие иммунокомпетентные клетки памяти периферической крови, сколько именно ГСК и ГПК, которые являются ответственными за формирование полноценного адаптивного (гуморально-опосредованного и клеточно-опосредованного) иммунного ответа в отношении бактерий, вирусов, поврежденных высокодифференцированных клеток и демонстрируют стойкую иммунную память всего организма. По мнению немецких ученых, именно ГСК формируют специализированный иммунный ответ на ранее встреченные антигены на уровне врожденного иммунитета (Laval et al., 2020). Накопление в процессе жизни человека и животных дополнительных соматических мутаций в ГСК и гемопоэтических предшественниках, а также накопление ДСМ в ГСК в результате взаимодействия с различными патогенами инфекционных и вирусных болезней, онкогенами и канцерогенами, возникающими в клетках в результате экстремальных воздействий окружающей среды, техногенных факторов и катастроф или эндогенных воздействий самого организма, приводят к формированию моментальных системных клеточно-гуморальных иммунных ответов на повторную встречу с уже известным антигеном. Как утверждают проф. Michael H. Sieweke и его команда из Дрезденского университета (Там же), в основе этого иммунного инструмента лежит формирование эпигенетической закладки над ДНК гемопоэтических прогениторов с маркером CD34+ в виде C/EBPb-белка. Эпигенетически зависимая от C/EBPb-белка иммунная память ГСК поддерживает пожизненную продукцию иммунных клеток и может напрямую реагировать на инфекцию, онкогены и другие неспецифические антигены. Они показали, что острая иммунная стимуляция искусственной бактерией (липополисахаридом — ЛПС) индуцировала только временные изменения количества, состава, потомства и экспрессии генов ГСК, но происходили устойчивые изменения доступности специфических энхансеров миелоидной линии, что повышало чувствительность ассоциированных иммунных генов к секрециям путем вторичной стимуляции. Функционально это было связано с усилением миелопоэза предварительно экспонированных ГСК и улучшением врожденного иммунитета. Доступные миелоидные энхансеры были обогащены мишенями C/EBPb, а делеция C/EBPb стерла долговременную запись ЛПС-индуцированных эпигенетических меток и экспрессии генов. Таким образом, кратковременная иммунная передача сигналов может индуцировать C/EBPb-зависимую доступность хроматина, что приводит к формированию иммунитета, обученного ГСК, во время вторичной инфекции или повторной встречи с любым другим известным антигеном. Это устанавливает новый механизм иммунитета и того, как история инфекции может быть эпигенетически вписана в память ГСК как неотъемлемая функция памяти врожденного иммунитета.
Механизм регуляции и управления ГСК любой из поврежденных известных 230 типов высокодифференцированных клеток различных тканей организма человека основан на межклеточном взаимодействии ГСК и ГКП с этими клетками. Путем горизонтального (внутри ткани и (или) органа) и (или) вертикального (между органами) информационного переноса и микровезикулярного транспорта экзосом, ГСК и ГПК обмениваются посредством экзосом с патологическими клетками-мишенями внутриклеточным содержимым (биологически активными веществами, белками и РНК). Эпигенетические и постгеномные (преимущественно протеомные) изменения молекулярно-биологической структуры ГСК, формируемые в результате межклеточного взаимодействия с патологическими клетками, приводят в одном случае к ремонту поврежденных клеток, в другом — к их выведению в апоптоз или, в третьем случае, их переводу в состояние покоя (Go-фаза клеточного цикла). Патоспецифические (онкоспецифические, нейроспецифические, кардиоспецифические и т.д.) белки, попадая в цитоплазму ГСК, могут привести к формированию раковых стволовых клеток, формирующих различные лейкозы, микроиммунизировать ГСК и генетически трансформировать их, а также запустить в них апоптоз или сформировать патологические клоны кроветворения, которые с течением времени будут неуклонно расширяться в размере молекулярно-биологических изменений, объеме клона ГСК и в увеличении количества потомков клона ГСК в циркулирующей крови человека и животных.
Формирование определенного клона стволовых клеток — это победа определенной группы тканеспецифических СК в соревновании с другими подобными СК на выживание и реальная возможность беспрепятственной репродукции. Это получение этими СК «золотой медали» за «выигрыш» на правах самого сильного: «Победитель получает все!» «Победивший в соревновании» клон СК приобретает эгоистические функции физического и биологического доминирования над другими подобными и более низкими по рангу тканеспецифическими СК организма, имеет неограниченные возможности для расширения в существующих тканевых нишах и получает преимущественное право на беспрепятственное размножение своего клона в периферической крови. А «проигравший» клон или клоны СК вынуждены отойти в сторону (в ниши) «на покой» и находиться большую часть своей жизни в Go-состоянии. Если «побеждает» определенный патоспецифический (онкоспецифический, нейроспецифический, кардиоспецифический) клон, то он формирует клиническую картину соответствующей болезни: злокачественной опухоли, нейродегенерации, системного атеросклероза, цирроза, диабета и т. д. Если «побеждает» клон СК с незначительными молекулярно-биологическими нарушениями, он определяет системную инволюцию клеток и тканей, характерную для обычного старения определенных тканей или органов. Возможна «победа» 2–3 и более клонов, имеющих как патологическую сердечно-сосудистую направленность, так и дегенеративно-дистрофическую составляющую.
Формирование доминирующего клона (клонов) ГСК в костном мозге и увеличение количества их потомков в циркулирующей крови человека и высшего млекопитающего приводят к моно- и олигоклональности гемопоэза, определяют преимущество данного клона (клонов) ГСК и его потомков перед другими ГСК в кроветворении организма, и он (они) постепенно и системно начинает преобладать физически и функционально в микроциркуляторном русле человека или животных. Клональность кроветворения ставит доминирующие патоспецифичные клоны ГСК на вершину иерархии всех клеток организма, их функциональность становится определяющей и управляющей в биологическом состоянии гомеостаза организма, и именно клональный гемопоэз формирует патогенез болезней цивилизации или возрастзависимых болезней. Это подтверждено новыми знаниями о ГСК и ГКП (Pui-Yu Ho et al., 2022).
Как мы уже отмечали, даже в здоровом состоянии все существующие клоны ГСК являются самыми «медленными» клетками в организме человека: их клеточный цикл составляет от 22 до 50 нед., или почти 360 дней. В соответствии с математической теорией систем (Винер, 1989; Неймарк, 1985) «управляющей в любом системном процессе является самая медленная фаза». Поэтому ГСК как самая «медленная» в организме клетка формирует все регуляторные иммунные реакции и управляет всеми системообразующими процессами. При насыщении определенных групп клонов ГСК патоспецифическими белками они начинают быть в континууме всех существующих в организме человека 50–200 тыс. ГСК и гемопоэтических предшественников еще более «медленными» клеточными системами среди всех клонов ГСК.
Они начинают управлять, доминировать в костном мозге, а их потомки — в циркулирующей крови, а также ингибировать другие клоны ГСК, нарушая поликлональность кроветворения. Сегодня очевидно, что именно поликлональность кроветворения — это залог здоровья и долголетия млекопитающего и человека. Расширение объема доминирующего клона ГСК и увеличение количества его потомков в центральной и периферической крови ставят все другие клоны ГСК в подсистему к доминирующим клонам ГСК, и это создает доминирующему клону самые благоприятные условия для репродукции и выживания в организме человека или высшего млекопитающего. Поэтому формирование клонального гемопоэза — это способ доминирования ряда клонов ГСК среди равных клонов клеточных участников кроветворения.
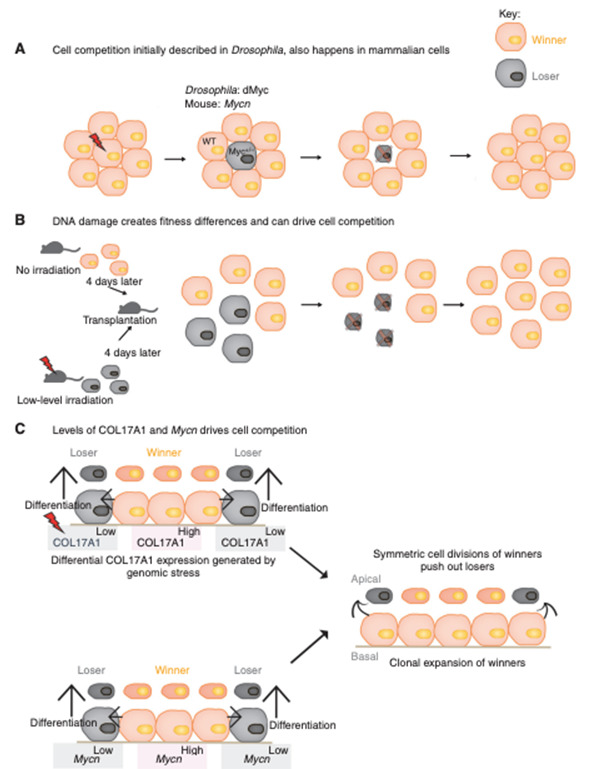
A — дифференциальные уровни Myc вызывают конкуренцию клеток как у дрозофилы (предшественники в диске), так и в клетках млекопитающих (развивающиеся эпидермальные клетки мыши и эпидермис взрослого человека). Этот рисунок показывает, что мутанты Myc являются «проигравшими» и уступают место соседним клеткам дикого типа (WT). Дополнительные уровни Myc также делают клетки «победителями» по сравнению с клетками WT (не показаны). B — повреждение ДНК создает различия в приспособленности, и это может стимулировать клеточную конкуренцию. Облучение гемопоэтических стволовых клеток и клеток-предшественников мыши вызывает повреждение ДНК, что приводит к повышению уровня Trp53. Когда эти клетки трансплантируются мышам с необлученными клетками (через 4 дня после облучения), облученные клетки вытесняются необлученными клетками, которые имеют более низкие уровни Trp53 и более высокую экспрессию более конкурентных сигнальных молекул. Таким образом, повреждение ДНК посредством облучения создает длительный статус клетки «проигравшего», вызывая опосредованный p53 апоптоз или остановку клеточного цикла.
C — клоны стволовых клеток с более высокими уровнями COL17A1 и Mycn становятся «победителями» в эпидермисе кожи мыши.
Геномный стресс приводит к протеолитической деградации COL17A1 и таким образом приводит к разным уровням экспрессии COL17A1 в эпидермисе. Клетки с более высокими уровнями COL17A1 превосходят клетки, экспрессирующие более низкие уровни, посредством
симметричного деления клеток и устранения проигравших.
Более высокая экспрессия COL17A1 поддерживает фенотип здоровой
кожи, тогда как дефицит COL17A1 вызывает атрофию, ломкость,
диспигментацию и алопецию кожи
Кроме получения режима благоприятствования в функциях саморепродукции клеток крови доминирующий клон (клоны) ГСК принимает самое активное участие в продуцировании и формировании функциональности большей части иммунокомпетентных клеток циркулирующей крови, а также моделировании специфичных ответных иммунных реакций на различные раздражители внешней и внутренней среды. Иммунокомпетентные потомки доминирующего клона ГСК становятся главными регуляторными и управляющими системами организма всех млекопитающих, и под их управлением начинают находиться все известные типы клеток организма человека.
Клональность кроветворения формируется патоспецифическими изменениями геномной и протеомной структуры ГСК, происходящей за счет мутаций в генах клональности, и это в результате приводит к накоплению новых критических дополнительных соматических мутаций в них. Это явление приводит к формированию патоспецифических свойств клонов ГСК и ГКП, а их потомки всецело доминируют в циркуляторном русле организма (Jaiswal, Ebert, 2019; Mitchell et al., 2022).
Как отмечает в своем научном обзоре, посвященном клональности гемопоэза, S. Jaiswal (2020), революция в области анализа отдельных клеток выявила гетерогенность популяций определенных типов клеток и сегодня признается, что клональная экспансия отдельных клеток лежит в основе этиопатогенеза целого ряда заболеваний, таких как рак, сосудистые заболевания, цирроз и нейродегенерации (Chappell et al., 2016; Dobnikar et al., 2018; Misra et al., 2018; Sheikh et al., 2015).
При этом формирование клональности стволовых клеток и клеток-предшественников — это общее возрастное системное явление для всех долгоживущих клеточных систем в организме. Парадокс заключается в том, что, например, множественные предшественники гладкомышечных клеток дают начало нормальной артериальной стенке во время развития и ремонта повреждения стенки сосуда, но несколько избранных предшественников патоспецифического клона внутри стенки участвуют в формировании атеросклеротических бляшек (Chappell et al., 2016; Jacobsen et al., 2017; Misra et al., 2018; Kabir et al., 2022). Кроме того, при возрастном клональном кроветворении стволовые клетки, несущие соматические мутации, дают доминантные варианты лейкоцитов, а появление патоспецифических клонов связано с повышенным риском серьезных заболеваний, ассоциированных с атеросклерозом, инфарктом миокарда и ишемическим инсультом (Jaiswal, Lybbi, 2020; Jaiswal et al., 2017; Kabir et al., 2022). Завершенные исследования на людях указывают на подобное прогрессирующее накопление мутантных соматических клонов в эпителиальных клетках различных органов, что характерно и для нормального старения (Martincorena et al., 2015, 2018; Moore et al., 2020; Yoshida et al., 2020). Показано, что ДСМ со временем накапливаются во всех клетках (Welch et al., 2012; Martincorena, Campbell, 2015; Blokzijl et al., 2016; Hoang et al., 2016). Эти ДСМ чаще всего представляют собой замены оснований (известные как однонуклеотидные варианты), небольшие вставки или делеции (indels) или изменения числа копий больших хромосомных областей (известные как структурные варианты). По оценкам, ГСК приобретают примерно 20 соматических мутаций в год во всем геноме (Lee-Six et al., 2018; Osorio et al., 2018) и примерно 0,1 мутации в год в экзонах, кодирующих белок (Welch et al., 2012), подавляющее большинство из которых являются однонуклеотидными вариантами.
В костном мозге только долгоживущие ГСК обладают способностью к самообновлению на протяжении всей жизни организма (Reya et al., 2001). Поэтому в большинстве случаев только мутации, возникающие в ГСК, сохраняются на протяжении всей жизни человека. Учитывая, что на человека приходится примерно от 50 до 200 тыс. ГСК, считается, что к 70 годам у людей насчитывается от 350 тыс. до 1,4 млн кодирующих мутаций в пуле ГСК. Если хотя бы одна из этих мутаций способна обеспечить селективное преимущество в отношении ГСК, в котором она возникает, клональная экспансия в крови должна быть обычным явлением при старении (Jaiswal, Ebert, 2019). Действительно, это явление, называемое клональным гематопоэзом, тесно связано со старением и показано в нескольких исследованиях лиц, отобранных для исследования гематологических нарушений (Xie et al., 2014; Genovese et al., 2014; Jaiswal et al., 2014; McKerrell et al., 2015; Acuna-Hidalgo et al., 2017; Coombs et al., 2017).
Необходимо отличать нормальное кроветворение от клонального гемопоэза. Периферическая кровь поддерживается на протяжении всей жизни человека гемопоэтическими стволовыми клетками костного мозга, которые определяются их способностью к устойчивому самообновлению и многолинейной дифференцировке (Orkin, Zon, 2008). В стационарных условиях разнообразный пул клонов HSC поддерживается в гомеостатическом равновесии и способствует поликлональному кроветворению. При нормальном старении диверсификация соматического генома в отдельных ГСК происходит с низкой, но обнаруживаемой частотой и распространяется во время самообновления ГСК. В нормальных ГСК соматические мутации имеют возрастную характеристику, которая состоит из переходов C> T в тринуклеотидных последовательностях NCG, возникающих в результате спонтанного дезаминирования 5-метилцитозина до тимина (Osorio et al., 2018). Эти замены оснований накапливаются в геномах ГСК со скоростью ~ 14 мутаций в год, включая экзонные мутации со скоростью ~ 1 каждые 10 лет (Welch et al., 2012; Osorio et al., 2018); стационарное поликлональное кроветворение отражает сбалансированный состав многих индивидуальных клонов, каждый из которых теоретически определяется отдельным набором соматических генетических изменений. Клональный гемопоэз (CH) определяется несбалансированным вкладом одного клона ГСК в периферическую кровь и может возникать в результате нейтрального дрейфа или направленного отбора. При нейтральном дрейфе все клоны имеют равные шансы внести свой вклад в пул самообновляющихся ГСК, но случайные процессы, такие как истощение стволовых клеток, приводят к фиксации одних клонов и потере других. При положительном отборе соматические изменения опосредуют преимущества селективного роста конкретных клонов ГСК по сравнению с другими, что приводит к клональному доминированию.
По мнению одного из ведущих специалистов по клональному гемопоэзу в мире S. Jaiswal (2020), в большинстве исследований мутации, используемые для определения клонального кроветворения, аналогичны мутациям, обнаруживаемым при гематологическом раке (Jaiswal et al., 2014; Coombs et al., 2017). Наиболее часто мутирующие гены в клональном кроветворении включают DNMT3A, TET2, ASXL1, JAK2, TP53 и SF3B1, которые так же часто мутируют при остром миелоидном лейкозе (Lindsley et al., 2015), миелодиспластическом синдроме (МДС) (Bejar et al., 2011; Papaemmanuil et al., 2013) и миелопролиферативных новообразованиях (Nangalia et al., 2013). Следовательно, неудивительно, что у людей с клональным гематопоэзом эти виды рака развиваются с большей скоростью, чем у людей без мутаций (Genovese et al., 2014; Abelson et al., 2018; Jaiswal et al., 2014; Desai et al., 2018). Однако мутации, вызывающие клональное кроветворение, также могут быть обнаружены в циркулирующих иммунных клетках, таких как гранулоциты, моноциты и лимфоциты. Это открытие повышает вероятность того, что клональное кроветворение может привести к измененным иммунным ответам, которые потенциально могут влиять на сам процесс старения и многие болезни старения (Mitchell et al., 2022).
Бесплатный фрагмент закончился.
Купите книгу, чтобы продолжить чтение.
